Die Abklärung und Betreuung von Patienten mit chronischen Bauchschmerzen stellen hohe Anforderungen an alle Beteiligten, sowohl in der Grundversorgung wie auch in der gastroenterologischen Ambulanz. In diesem Artikel werden eine mögliche Herangehensweise vorgeschlagen und aktuelle Aspekte beleuchtet.
Chronische Bauchschmerzen stehen im Spannungsfeld von organischen und funktionellen Erkrankungen in dem Sinne, dass die Wahrscheinlichkeit für das Vorliegen von funktionellen Erkrankungen mit zunehmender Krankheitsdauer zwar zunimmt, aber die Möglichkeit von organischen Erkrankungen nie ausgeschlossen ist. Dieser Umstand kann gerade bei anfälligen Patienten ständiger Anlass für entsprechende Befürchtungen und Forderung nach neuen Abklärungen sein. Eine etablierte Definition für die Chronizität von Schmerzen liegt nicht vor, vielmehr liegt es in der klinischen Beurteilung, abzuschätzen, ob ein progredienter Prozess, ein intermittierender langdauernder Prozess, eine Exazerbation eines chronischen Problems oder aber ein neues unabhängiges Problem besteht. Aber immerhin wird in den neuen ROME IV-Kriterien gefordert, dass Symptome mindestens 6 Monate bestehen müssen, um die Diagnose eines abdominalen Schmerzsyndroms stellen zu können (1).
Erste Schritte (2)
Funktionelle Erkrankungen positiv identifizieren
In Anbetracht der hohen Prävalenz von funktionellen Verdauungsstörungen (FGID) könnte man zur raschen Annahme verleitet werden, dass ein Patient, der sich mit chronischen Bauschmerzen präsentiert, an einer Form einer funktionellen Magen-Darmkrankheit leidet, wie z.B. einem IBS oder einem zentral vermittelten abdominalen Schmerzsyndrom. Diese Annahme kann aber trügerisch sein und man sollte versuchen, funktionelle Erkrankungen positiv zu identifizieren und nicht einfach im Ausschlussverfahren unter dem Motto «Sie haben nichts» zu diagnostizieren. Dazu dient eine psychosoziale Anamnese mit Fragen wie «Warum kommen Sie gerade jetzt in die Sprechstunde», «Sind traumatische Erlebnisse vorgefallen», «Wie interpretieren Sie Ihre Beschwerden», «Leidet Ihre Lebensqualität unter den Beschwerden» und eine Abklärung von assoziierten psychiatrischen Diagnosen, der Rolle von Familie und Kultur (3). Bei der körperlichen Untersuchung beachtet man das für funktionelle Erkrankungen typische Fehlen von vegetativen Zeichen wie Tachykardie, Blutdruckanstieg oder Schwitzen bei Schmerzprovokation, das Vorhandensein multipler Narben ohne klare Indikation, die Äusserung von Schmerzen mit geschlossenen Augen und die Abnahme von Schmerzäusserungen, wenn die Druckschmerzhaftigkeit mit dem Stethoskop geprüft wird. Zum Nachweis von nicht seltenen Bauchwandschmerzen eignet sich der Carnett’s Test, bei dem zuerst in Ruhe die Region der maximalen Schmerzhaftigkeit ertastet wird. Wenn der Schmerz dann bei gleichzeitigem Anspannen der Bauchmuskulatur zunimmt, spricht man von einem positiven Test, der als Argument gegen einen viszeralen Schmerz gewertet werden kann (3). Ob den Beschwerden primär Blähungen und ein vermehrter abdominaler Gasgehalt zugrunde liegt, kann anamnestisch und klinisch geklärt werden.
Ausschluss von organischen Erkrankungen
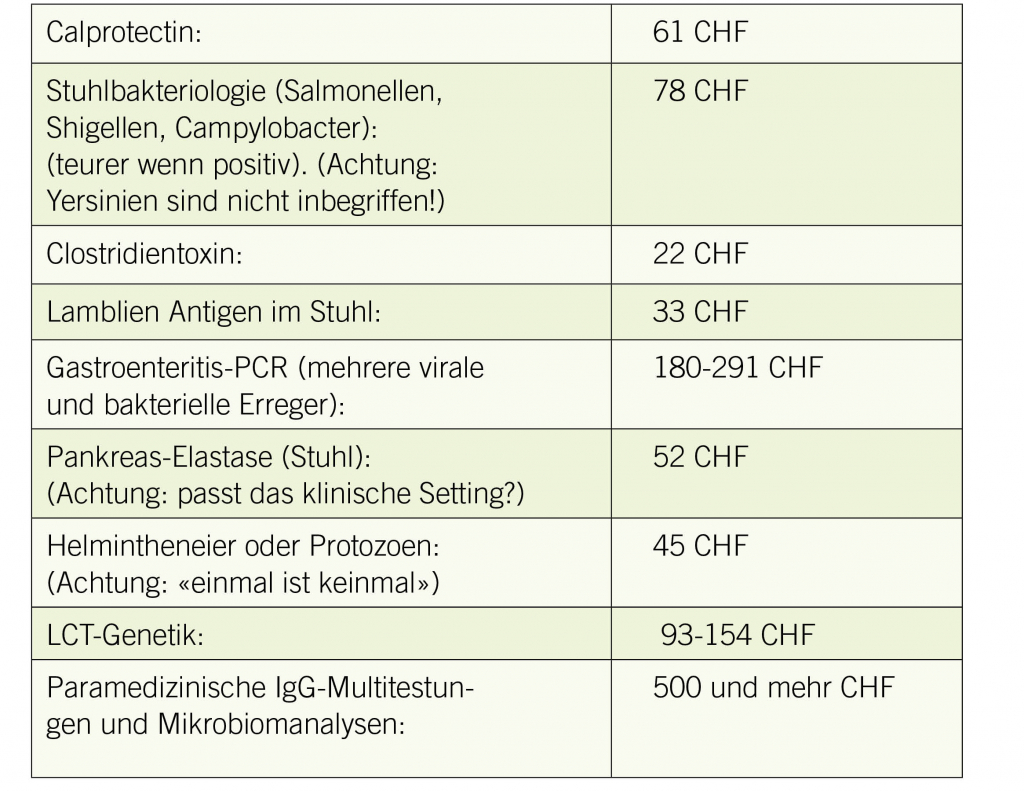
Zum Ausschluss von organischen Erkrankungen gilt es, Alarmsymptome wie Alter über 50 Jahre, rektale Blutung, Gewichtsverlust, kürzliche Veränderung der Darmgewohnheit und ganz allgemein eine Dynamik betreffend der Schmerzdimensionen (also z.B. Änderung in Charakter, Lokalisation oder Intensität der Schmerzen) zu beachten. Folgende Charakteristika sprechen eher für organische Erkrankungen: Kürzere Krankheitsdauer, Beschreibung von sensorischen Qualitäten und nicht von Emotionen, präzisere anatomische Zuordnung zu neuroanatomischen Strukturen, meistens einfachere interpersonelle Beziehung. Nebst einem unauffälligen abdominalen Tastbefund, insbesondere Ausschluss von Massen oder Hepatomegalie, ist eine basale Diagnostik mit Blutstatus, CRP / Calprotectin im Stuhl und eine
Zöliakie-Serologie sinnvoll, ergänzt durch eine Sonographie des Abdomens. Endoskopien sind ausser bei Alarmsymptomen indiziert bei Beschwerden, die einen zeitlichen Zusammenhang mit der Nahrungsaufnahme und/oder Darmtätigkeit aufweisen. Jedoch gilt die Diagnose eines Reizdarmsyndroms anhand der ROME IV-Kriterien bei fehlenden Alarmsymptomen in der Praxis als sicher (2, 3). Weitere Abklärungen erfolgen gezielt nach Klinik.
Grundpfeiler der Behandlung von chronischen funktionellen Bauchbeschwerden
Der Grundpfeiler der Behandlung von chronischen FGIDs ist zuerst die Erstellung einer guten Arzt-Patienten-Beziehung mit Empathie, Ernstnehmen der Beschwerden, Beruhigung, Erziehung und Setzen vernünftiger Behandlungsziele. Sodann das Aufstellen eines für den Patienten spezifischen und verständlichen Behandlungsplans mit Offerte verschiedener Optionen. Dabei kann dem Patienten geholfen werden, Verantwortung zu übernehmen, z.B. im Bereich Lebensstil, Fitnesstraining, Stressreduktion und Schlafmanagement. Die Behandlung soll dem Schweregrad der Symptome und der Behinderung angepasst werden, gegebenenfalls unter Beizug von psychologisch-/psychiatrischer Hilfe. Die eigentliche Behandlung kann diätetischer, medikamentöser und psychologischer Natur sein. Auch kann es für den Patienten von Bedeutung sein, vom Arzt zu erfahren, dass er mit seinen Beschwerden zu einer Mehrheit der Bevölkerung gehört und das «Finden von Nichts» nicht die Ausnahme, sondern eher die Regel bei einer derartigen Klinik darstellt.
Obwohl praktisch alle Patienten mit FGIDs Zusammenhänge zwischen ihrer Diät und den Bauchschmerzen wittern, ist die Evidenz für den effektiven Nutzen einer Ernährungstherapie sehr tief. Am besten haben Studien zur FODMAP-Diät abgeschnitten, der Stellenwert einer Gluten-reduzierten Diät ist nach Ausschluss einer Zöliakie umstritten (4, 5). Nach dem heutigen Kenntnisstand kann eine solche Restriktion nicht empfohlen werden. Wenn der Patient diesbezüglich motiviert ist, muss davon zwar nicht abgeraten werden. Der Erfolg sollte aber mit Unterstützung durch den Arzt vom Patienten möglichst kritisch und genau evaluiert werden.
An Medikamenten haben sich periphere Analgetika und Opioide ebenso wenig bewährt wie Benzodiazepine. Bei gleichzeitiger Verstopfung steht der Einsatz von Quellstoffen zur Diskussion, dabei haben sich lediglich lösliche Quellstoffe als bescheiden wirksam erwiesen. Für Polyethylenglycol besteht keine Evidenz eines Nutzens gegen funktionelle Schmerzen, wohl aber für seine laxierende Wirkung. Spasmolytika können mit tiefer Evidenz kurzfristige Wirkungen entfalten, die aber je nach Substanz durch anticholinerge Nebenwirkungen überschattet werden. Pfefferminzöl scheint mit mittlerem Evidenzgrad nebst einer spasmolytischen Wirkung auch die viszerale Hypersensitivität abschwächen zu können. Der Einsatz von Antidepressiva, sowohl von Trizyklika wie auch von SSRIs, ist insbesondere bei Personen mit einer depressiven Begleitsymptomatik mit hoher Evidenz und mit einer Number Needed to Treat (NNT) von 4 in der Lage, Symptome von funktionellen Erkrankungen zu beeinflussen, wegen der häufigen und für Patienten oft limitierenden Nebenwirkungen ist ihr Einsatz aber nur schwach empfohlen (4). Zudem fühlen sich viele Patienten stigmatisiert durch die Verschreibung eines psychiatrischen Medikamentes, was die schlechte Compliance erklärt (2). Gegen Letzteres hat es sich als sehr hilfreich erwiesen, dem Patienten die Begründung, nämlich Therapie der viszeralen Hypersensitivität und eben nicht einer zentralnervösen Störung, eingehend zu erläutern (Vergleichbar etwa Begründung: Antiepileptika bei neuropathischem Schmerz hat nichts mit der Behandlung einer Epilepsie zu tun).
«Wenn normal bedrohlich wird»
In der Perpetuierung von FGIDs spielen Magen-Darm-Symptom-spezifische Ängste eine wesentliche Rolle. Sie stellen einen wichtigen und dauerhaften Faktor von FGIDs dar und zeichnen sich durch Sorgen und Hypervigilanz um GI-Sensationen aus, die von normalen Körperfunktionen (Hunger, Sättigung, Gas) bis hin zu Symptomen im Zusammenhang mit einem GI-Ereignis (Bauchschmerzen, Durchfall, Dringlichkeit) reichen können. Im weiteren Verlauf verallgemeinern sich die Sorgen und Hypervigilanz in der Regel in Ängste bereits hinsichtlich des Potenzials für das Auftreten von Empfindungen oder Symptomen. Und dann weiter hinsichtlich der Situationen, in denen sie am ehesten auftreten könnten. Magen-Darm-Symptom-spezifische Angstzustände können zu Vermeidung und Verhalten führen, das in keinem Verhältnis zu den Symptomen steht (6). Diese und weitere Mechanismen sind einer psychologischen Behandlung wie z.B. einer Verhaltenstherapie zugänglich und Metaanalysen haben gezeigt, dass psychologische Behandlungen mit einer NNT von 2 bis 4 mindestens mässig effektiv sind zur Symptomlinderung bei FGIDs (6).
Einige Änderungen der ROME-Kriterien von Version III zu IV
Erkrankungen der Interaktion von Gehirn-Darm
Die Benennung von Schmerzen und anderen Symptomen ohne offenkundiges pathologisches anatomisches Korrelat als «funktionell» bedeutet für viele Menschen unter dem Missverständnis «ist halt nur psychisch oder eingebildet» eine Stigmatisierung. Dieses Verständnis erweist sich auch zunehmend als inhaltlich falsch, da wissenschaftliche Forschung gezeigt hat, dass viele sogenannte funktionelle Erkrankungen durch organische Veränderungen charakterisiert sind, sei es im Sinne von niedrig-gradiger Entzündung im Falle eines Reizdarms oder von Veränderungen des Mikrobioms des Darmes oder einer gestörten Motilität oder einer veränderten zentralen Verarbeitung von Afferenzen aus dem Gastrointestinaltrakt. Aus diesem Grunde werden funktionelle gastro-intestinale Beschwerden neu als Erkrankungen der Interaktion von Gehirn-Darm definiert (7, 8) und im Rahmen eines biopsychosozialen Konzeptes beurteilt (6).
Kriterien für die Diagnose von Reizdarm und von einem zentral vermittelten abdominalen Schmerzsyndrom
Neu ist, dass zur Diagnose eines IBS das Symptom «Schmerz» vorhanden sein muss und dass die Subkategorien eines IBS heute eher als Kontinuum angesehen werden mit wechselhaftem Spektrum von Symptomen wie Durchfall oder Verstopfung im Laufe der Zeit. Die aktuellen diagnostischen Kriterien C1 für IBS und D1 für das zentral vermittelte abdominale Schmerzsyndrom sind in der Tabelle zusammengefasst.
Facharzt FMF Innere Medizin und Gastroenterologie
Neuhausstrasse 18
8044 Zürich
Schulthess_hk@swissonline.ch
Der Autor hat in Zusammenhang mit diesem Artikel keine Interessenskonflikte deklariert.
Literatur
1. Keefer L, Drossman DA, Guthrie E, Simrén M, Tillisch K, Olden K et al. Centrally Mediated Disorders of Gastrointestinal Pain. Gastroenterology 2016; 150(6):1408–19. doi: 10.1053/j.gastro.2016.02.034.
2. Camilleri M. Management of patients with chronic abdominal pain in clinical practice. Neurogastroenterol Motil 2006; 18(7):499–506. doi: 10.1111/j.1365-2982.2005.00744.x.
3. Drossman DA. Functional abdominal pain syndrome. Clin Gastroenterol Hepatol 2004; 2(5):353–65.
4. Ford AC, Moayyedi P, Lacy BE, Lembo AJ, Saito YA, Schiller LR et al. American College of Gastroenterology monograph on the management of irritable bowel syndrome and chronic idiopathic constipation. Am J Gastroenterol 2014; 109 Suppl 1:S2-26; quiz S27. doi: 10.1038/ajg.2014.187.
5. Mearin F, Lacy BE, Chang L, Chey WD, Lembo AJ, Simren M et al. Bowel Disorders. Gastroenterology 2016; 150(6):1393–407. doi: 10.1053/j.gastro.2016.02.031.
6. van Oudenhove L, Crowell MD, Drossman DA, Halpert AD, Keefer L, Lackner JM et al. Biopsychosocial Aspects of Functional Gastrointestinal Disorders. Gastroenterology 2016; 150(6):1355–67. doi: 10.1053/j.gastro.2016.02.027.
7. Drossman DA, Hasler WL. Rome IV-Functional GI Disorders: Disorders of Gut-Brain Interaction. Gastroenterology 2016; 150(6):1257–61. doi: 10.1053/j.gastro.2016.03.035.
8. Tack J, Drossman DA. What’s new in Rome IV? Neurogastroenterol Motil 2017; 29(9). doi: 10.1111/nmo.13053.