Die 27-jährige Patientin entwickelte nach einem periumbilikalen Zeckenstich Fieber, Kopfschmerzen und Lichtempfindlichkeit. An der Zeckenstichstelle trat ein zentral verkrustetes Ulkus mit einer begleitenden schmerzhaften Lymphadenopathie inguinal links auf. Zudem entwickelte die Patientin neurokognitive Einschränkungen. Aufgrund stark erhöhter IgM- und IgG-Titer für Francisella tulariensis konnte eine Tularämie mit Beteiligung des zentralen Nervensystems diagnostiziert werden. Nach zehntägiger Therapie mit Gentamicin und Ciprofloxacin waren die Kopfschmerzen rückläufig, die neurokognitive Symptomatik besserte sich nur langsam.
The 27-year-old patient developed fever, headache, and light sensitivity after a tick bite in the periumbilical region. At the site of the tick bite, a centrally crusted ulcer appeared, accompanied by painful inguinal lymphadenopathy on the left side. Additionally, the patient developed neurocognitive impairments. Due to significantly elevated IgM and IgG titers for Francisella tularensis, a diagnosis of tularemia with central nervous system involvement was made. After a ten-day treatment with gentamicin and ciprofloxacin, the headaches subsided, but the neurocognitive symptoms improved only slowly.
Key words: Tularemia with central nervous affection, tick-borne diseases with central nervous affection, Ulcer following tick bite
Anamnese und Befunde
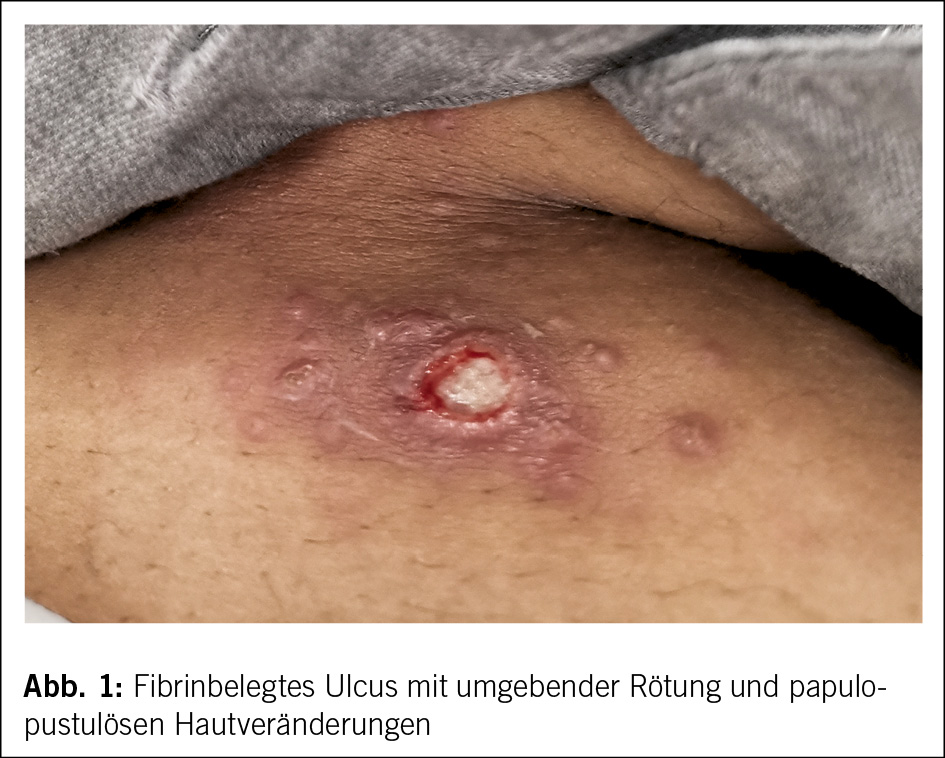
Die 27-jährige Patientin bemerkte eine Zecke links periumbilikal und entfernte diese. Drei Tage später traten Kopfschmerzen, Lichtempfindlichkeit, Übelkeit und Fieber auf. Sie stellte sich in der hausärztlichen Sprechstunde vor. Bei erhöhten Entzündungswerten (CRP 86 mg/l, Leukozyten 7.3 x 103/µl (Normwerte: CRP < 5 mg/l, Leukozyten 3.9–10 x 103/µl) und Rötung um die Stichstelle verschrieb der Hausarzt in Annahme eines Erythema migrans bei Borrelien-Infektion Amoxicillin für sechs Tage. Die Kopfschmerzen besserten unter Ibuprofen nur temporär. Es persistierte ein «nebliges Gefühl im Kopf». Fünf Tage nach der antibiotischen Therapie stellte sich die Patientin mit einem schmerzhaften Ulkus an der Zeckenstichstelle und linksseitigen Leistenschmerzen auf der Notfallstation vor. In der körperlichen Untersuchung zeigte sich an der Zeckenstichstelle eine fibrinbelegte Wunde mit umgebender Rötung und papulopustulösen Hautveränderungen von etwa 4 x 2 cm mit subkutaner Induration (Abb. 1).
In der linken Leiste fand sich ein 7 mm messender, druckdolenter, verschieblicher Lymphknoten, sonographisch vereinbar mit einer reaktiven Lymphadenopathie. Das CRP war mit 67 mg/l erhöht, die Leukozyten mit 6.61 x 103/µl normwertig. Die Patientin wurde mit symptomatischer Therapie entlassen. Eine Woche später stellte sie sich erneut in der hausärztlichen Sprechstunde vor, da sie zunehmend schwach war und ihrer Arbeit nicht nachgehen konnte. Am Bauchnabel persistierte das eiternde Ulkus. Die Entzündungswerte waren leicht erhöht (CRP 29 mg/l, Leukozyten 6.6 x 103/µl). Bei Verdacht auf eine bakterielle Superinfektion nach Zeckenstich wurde die Therapie mit Clindamycin eingeleitet. In der hausärztlichen Kontrolle zwei Tage später waren die Entzündungswerte leicht rückläufig (CRP 21 mg/l, Leukozyten 7 x 103/µl). Die Patientin und ihr Umfeld berichteten jedoch über eine zunehmende psychomotorische Verlangsamung und Wesensveränderung.
Differenzialdiagnostische Überlegungen
Der erlittene Zeckenstich mit konsekutiver Rötung und Entwicklung eines Ulkus an der Einstichstelle mit begleitender schmerzhafter Lymphadenopathie und neurokognitiven Beschwerden lassen primär an folgende mögliche Krankheitsbilder denken:
Lyme Borreliose
Mit 650 000 bis 850 000 Fällen jährlich ist die Lyme-Borreliose die häufigste vektorübertragene Erkrankung in Europa. Hervorgerufen wird sie durch verschiedene Spezies von Borrelia burgdorferi, gramnegative, anaerobe, spiralförmige Bakterien aus der Familie der Spirochäten. 3 bis 30 Tage nach Übertragung kann sich an der Zeckenstichstelle ein Erythema migrans, ein sich ausbreitender Hautausschlag, entwickeln. Begleitend können selten auch vergrößerte Lymphknoten auftreten. Bei unbehandelten Patienten kann es zu einer Dissemination mit Allgemeinsymptomen, weiteren kutanen Manifestationen, früher Neuroborreliose, Karditis und nach Monaten bis Jahren zu Spätmanifestationen wie Arthritis oder späte Neuroborreliose kommen. Die Hautmanifestationen nach Zeckenstich und neurologischen Symptome unserer Patientin könnten auf eine frühe Lyme-Neuroborreliose hindeuten. Jedoch sah das Hautulkus der Patientin nicht wie ein Erythema migrans aus, dessen Diagnose klinisch erfolgt. Zur Diagnose einer Neuroborreliose muss der Serum-Liquor-Index der spezifischen Antikörper bestimmt werden (1).
Frühsommer-Meningoenzephalitis (FSME)
Die Frühsommer-Meningoenzephalitis wird durch das FSME-Virus aus der Gruppe der Flaviviren hervorgerufen. Nur ein Drittel der Infektionen verläuft symptomatisch. Nach einer Inkubationszeit von vier bis 28 Tagen treten Fieber, Muskelschmerzen und Abgeschlagenheit auf. Nach zwei bis sieben Tagen tritt eine symptomarme, afebrile Phase von etwa zehn Tagen auf, auf die eine zweite febrile Phase mit Meningitis oder Meningoenzephalitis folgt. Während der initialen symptomatischen Phase ist die spezifische serologische Diagnostik noch negativ. In dieser Phase wäre ein Virusnachweis im Blut mittels PCR möglich. In der zweiten Phase ist die serologische Diagnostik positiv (2). Die neurologischen Beschwerden der Patientin könnten zu einer FSME passen, jedoch war der Krankheitsverlauf bei unserer Patientin nicht zweigipflig, sie war durchgehend symptomatisch. Ausserdem treten bei der FSME in der Regel keine ausgeprägten Hautveränderungen an der Zeckenstichstelle auf.
Tularämie
Die Tularämie wird durch das gramnegative, aerobe, fakultativ intrazelluläre Bakterium Francisella tularensis hervorgerufen (3). Die Übertragung erfolgt meist vektorgebunden durch Zecken und Stechmücken. Einen weiteren Übertragungsweg stellt der direkte Kontakt mit infizierten Säugetieren, typischerweise Nagetieren, oder Ingestion von rohem Fleisch eines infizierten Tieres dar. Auch durch kontaminiertes Wasser und Inhalation kontaminierter Aerosole, beispielsweise bei landwirtschaftlicher Tätigkeit, kann die Infektion erfolgen (4–7).
Die Tularämie kann sich durch ein breites Spektrum klinischer Symptome äussern; der Schweregrad reicht von asymptomatisch bis tödlich. Nach einer Inkubationszeit von drei bis fünf Tagen kommt es vom Ort der Infektion aus (je nach Infektionsweg von der Insektenstichstelle, den Konjunktiven, dem Gastrointestinal- oder Respirationstrakt) zur Ausbreitung der Bakterien über das Lymphsystem zu den regionalen Lymphknoten, wo die Replikation stattfindet. Anschliessend erfolgt die Dissemination, während der grippeähnliche Symptome auftreten können. Klassischerweise werden sechs Verlaufsformen unterschieden (7): Bei der ulceroglandulären und glandulären Form kommt es zu regionaler Lymphadenopathie mit (ulceroglandulär) oder ohne (glandulär) Hautläsion. Bei der oculoglandulären Form tritt eine Konjunktivitis mit cervicaler Lymphadenopathie auf. Die oropharyngeale Form präsentiert sich mit einer Pharyngitis und teilweise oropharyngealen Ulcera mit cervicaler Lymphadenopathie. Die respiratorische Form äussert sich als akute oder subakute Pneumonie. Die typhoide Form beschreibt einen schweren Verlauf mit Sepsis (4, 8). Es können eine Vielzahl von Komplikationen auftreten. Die Bildung von Lymphknotenabszessen ist mit ca. 30 % der Patienten mit Lymphadenopathie die häufigste. Seltener kommt es zu Beteiligung anderer Organe, beispielsweise Karditis oder zu Meningitis und Meningoencephalitis (4, 8, 9). Mit einem Ulkus an der Zeckenstichstelle und begleitende Lymphadenopathie weist unsere Patientin typische Krankheitszeichen einer ulceroglandulären Tularämie auf. Die neurologischen Symptome könnten Hinweise für eine begleitende Meningoenzephalitis sein. Angesichts dieser differentialdiagnostischen Überlegungen und des schwerwiegenden Krankheitsbildes der Patientin sind weiterführende Untersuchungen zur genaueren Diagnose und Behandlungsplanung dringend empfohlen.
Weitere Abklärungsschritte und Verlauf
Durch den Hausarzt wurden bei Verdacht auf Encephalitis ein Elektroencephalogramm (EEG), eine Liquorpunktion und eine zerebrale Magnetresonanztomographie (MRT) veranlasst. Das EEG zeigte eine regionale Verlangsamung linkshemisphäriell.
Die MRT zeigte keine strukturell pathologischen Befunde im Sinne einer Enzephalitis. In der Lumbalpunktion fand sich eine Zellzahl von drei mononukleären Zellen/µl bei normwertigem Protein und negativem Borrelien- und FSME-Serum-Liquor-Index. Die Patientin wurde zur weiteren Abklärung in die neurologische Sprechstunde zugewiesen. Hier wurde zwei Monate nach Auftreten der ersten Symptome bei stark erhöhten IgG- sowie IgM-Titer für Francisella tulariensis (IgG 123.7 U/ml [Normwert < 10], IgM 241.5 U/ml [Normwert < 10]) eine Tularämie mit zerebraler Beteiligung diagnostiziert. Bei normaler Zellzahl im Liquor waren formal die Kriterien für eine Meningitis nicht erfüllt, wobei die Lumbalpunktion knapp zwei Monate nach den initialen Beschwerden durchgeführt wurde. Die Patientin wurde zur Therapie mit Gentamicin 350 mg intravenös einmal täglich sowie Ciprofloxacin 500 mg peroral zweimal täglich für zehn Tage stationär aufgenommen. In der erneuten MRT ergaben sich weiterhin keine bildmorphologischen Korrelate einer Enzephalitis. Ein wiederholtes EEG zeigte eine fokale Verlangsamung temporo-occipital rechts und in geringerem Ausmass temporo-occipital links. Im Montreal Cognitive Assessment erreichte die Patientin 26 von 30 Punkten. Unter der Therapie waren die Kopfschmerzen komplett rückläufig. Aufgrund der nur langsam regredienten neurokognitiven Symptomatik wurde die Patientin der stationären neurologischen Rehabilitation zugewiesen. Bei Spitalsaustritt bestanden ein subjektives Schwächegefühl der rechten Körperseite ohne klinisch manifeste Parese, Wortfindungsschwierigkeiten, phonematische Paraphasien bei verlangsamter Spontansprache und deutliche Defizite in attentionalen, mnestischen und exekutiven Funktionen. Die Symptome besserten sich im Laufe der neurologischen Rehabilitation. Zwei Monate später bestanden weiterhin kognitive Einschränkungen im Sinne einer erhöhten geistigen Erschöpfbarkeit im Alltag, welche ein reduziertes Arbeitspensum bedingen. Somatische Beschwerden waren keine mehr vorhanden.
Kommentar
Die beschriebene Patientin wies initial einen typischen Verlauf einer ulzeroglandulären Tularämie mit Ausbildung eines Ulkus an der Einstichstelle und schmerzhafte Lymphadenopathie mit ausgeprägtem Krankheitsgefühl auf. Aufgrund der Seltenheit der Tularämie konnte die Diagnose trotz wiederholter Arztkontakte erst spät gestellt werden. Bei klinischem Verdacht auf eine Tularämie ist es essenziell, die entsprechende Diagnostik in die Wege zu leiten und die entsprechende antibiotische Therapie zu beginnen, um Komplikationen zu verhindern. Für die Diagnose wird ein über vierfacher Titeranstieg der spezifischen Antikörper, ein einmalig sehr hoher Titer, wie bei unserer Patientin, oder ein direkter Erregernachweis aus Patientenmaterial wie Blut, Ulkus- oder Lymphknotengewebe per PCR oder Kultur gefordert. Der kulturelle Nachweis gelingt selten, da das Bakterium rasch transportiert werden muss und spezielle Nährmedien benötigt (3, 10, 11). Eine zentralnervöse Beteiligung bei Tularämie ist selten (12). Eine Meningitis drei bis 30 Tage nach der initialen febrilen Erkrankung bei ulceroglandulärer und typhoidaler Form ist beschrieben (12–14). Auch Fälle von Meningitis nach inhalativer Exposition werden berichtet (12). Weitere seltene neurologische Verlaufsformen sind das Guillain-Barre-Syndrom sowie die Manifestation an einzelnen kranialen Nerven (15, 16). Zur Therapie der Tularämie kommen Chinolone, Tetracycline und bei schweren Verläufen Aminoglycoside zum Einsatz (17). Seit 2004 ist die Tularämie beim Menschen meldepflichtig. 2022 wurden 114 Fälle gemeldet, was einer Inzidenz von 1.3 Fällen pro 100 000 Einwohnern entspricht. Seit 2011 wird eine Zunahme der Fallzahlen verzeichnet, wobei die Fallzahl seit 2017 in etwa stabil geblieben ist. Die Zunahme wird zumindest teilweise auf vermehrte Testung zurückgeführt (18). Aufgrund der typischen Klinik der Patientin, die sich nach einem Zeckenstich entwickelt hat und den sehr hohen Titern für Francisella tularensis, ist die Diagnose bei unserer Patientin gesichert. Auf die Therapie mit Gentamicin und Ciprofloxacin hat sie gut angesprochen, auch wenn die neurokognitiven Einschränkungen nicht komplett regredient waren.
Abkürzungen
FSME Frühsommer-Meningoencephalitis
PCR Polymerase Chain Reaktion
MRT Magnetresonanztomographie
EEG Elektroencephalographie
ZNS Zentralnervensystem
Copyright Aerzteverlag medinfo AG
Allgemeine Innere Medizin
Kantonsspital Graubünden
Loestrasse 170
7000 Chur
Neurologie
Kantonsspital Graubünden
Loestrasse 170
7000 Chur
Leitende Ärztin für Infektiologie
Kantonsspital Graubünden
Loëstrasse 170
7000 Chur
alexia.cusini@ksgr.ch
Die Autorschaft hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Zajkowska JM, Eldin C, Talagrand-Reboul E, Raffetin A, Zachary P, Jaulhac B. Immunoserological Diagnosis of Human Borrelioses: Current Knowledge and Perspectives. Front Cell Infect Microbiol. 2020;1:241.
2. Wendt S, Trawinski H, von Braun A, Lübbert C. Durch Zecken übertragbare Erkrankungen: Von der Lyme-Borreliose über das Q-Fieber bis zur FSME. CME (Berl). 2019;16:53–71.
3. Ellis J, Oyston PCF, Green M, Titball RW. Tularemia. Clin Microbiol Rev. 2002;15:631–46.
4. Maurin M, Gyuranecz M. Tularaemia: clinical aspects in Europe. Lancet Infect Dis. 2016;16:113–24.
5. Yeni DK, Büyük F, Ashraf A, Shah MS ud D. Tularemia: a re-emerging tick-borne infectious disease. Folia Microbiol (Praha). 2021;66.
6. Zellner B, Huntley JF. Ticks and Tularemia: Do We Know What We Don’t Know? Front Cell Infect Microbiol. 2019;9.
7. World Health Organization. WHO guidelines on tularaemia : epidemic and pandemic alert and response. World Health Organization; 2007.
8. Evans M, Gregory D, Schaffner W, McGee Z. Tularemia: a 30-year experience with 88 cases. Medicine (Baltimore). 1985;64:251–69.
9. Maurin M. Francisella tularensis, Tularemia and Serological Diagnosis. Front Cell Infect Microbiol. 2020;10.
10. Tärnvik A, Chu MC. New approaches to diagnosis and therapy of tularemia. Ann N Y Acad Sci. 2007;1105:378–404.
11. Porsch-Özcürümez M, Kischel N, Priebe H, Splettstösser W, Finke EJ, Grunow R. Comparison of enzyme-linked immunosorbent assay, Western blotting, microagglutination, indirect immunofluorescence assay, and flow cytometry for serological diagnosis of tularemia. Clin Diagn Lab Immunol. 2004;11:1008–15.
12. Venkatesan S, Johnston C, Mehrizi MZ. A rare case of tularemic meningitis in the United States from aerosolized Francisella tularensis. J Am Coll Emerg Physicians Open. 2020;1:238.
13. Ducatez N, Melboucy S, Bentayeb H, Dayen C, Suguenot R, Lecuyer E, et al. A case of Francisella tularensis meningitis in a 64-year-old man treated with quinolones. Infect Dis Now. 2022;52:107–9.
14. Hofinger DM, Cardona L, Mertz GJ, Davis LE. Tularemic meningitis in the United States. Arch Neurol. 2009;66:523–7.
15. Ylipalosaari P, Ala-Kokko TI, Tuominen H, Syrjälä H. Guillain-Barré syndrome and ulceroglandular tularemia. Infection. 2013;41:881–3.
16. Blech B, Christiansen M, Asbury K, Orenstein R, Ross M, Grill M. Polyneuritis cranialis after acute tularemia infection: A case study. Muscle Nerve. 2020;61:E1–2.
17. Kohlmann R, Geis G, Gatermann SG. Die Tularämie in Deutschland. Deutsche Medizinische Wochenschrift. Georg Thieme Verlag; 2014. p. 1417–22.
18. Bundesamt für Lebensmittelsicherheit und Veterinärwesen BLV, Bundesamt für Gesundheit BAG. Bericht zur Überwachung von Zoonosen und lebensmittelbedingten Krankheitsausbrüchen. 2022.