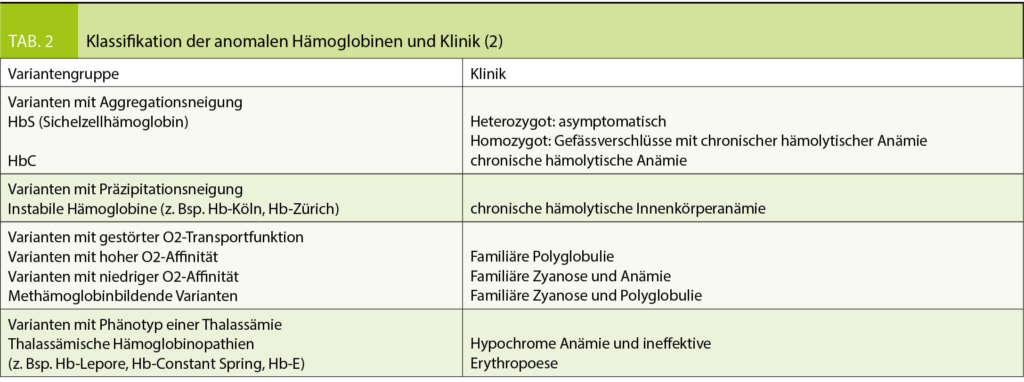
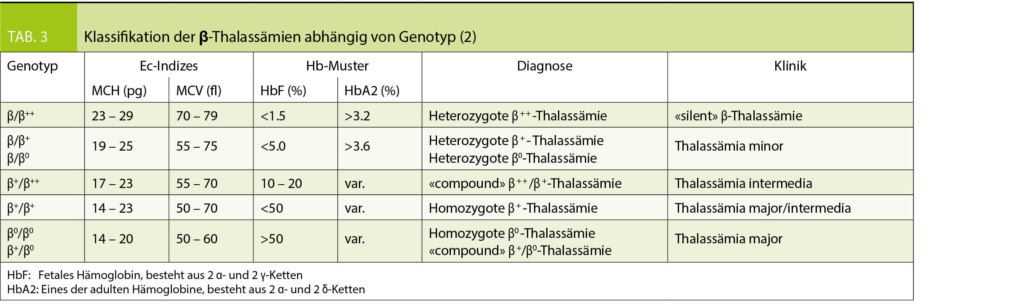
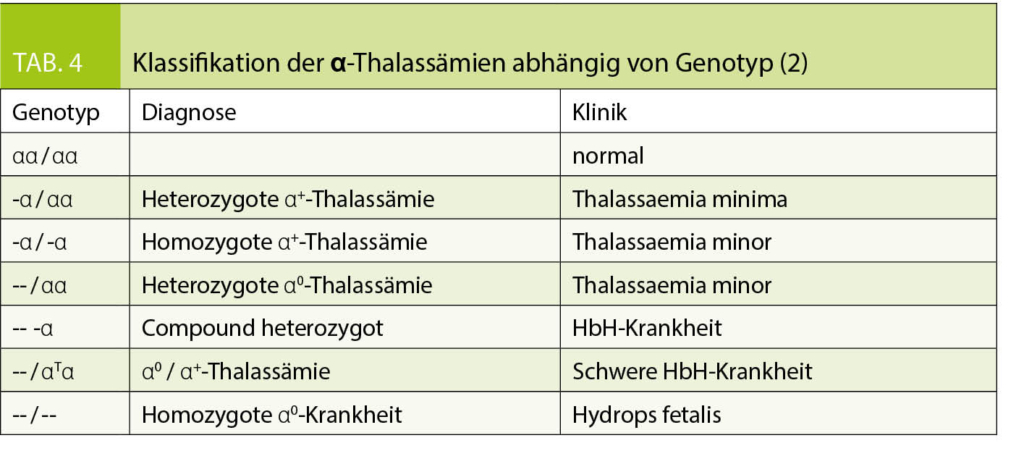
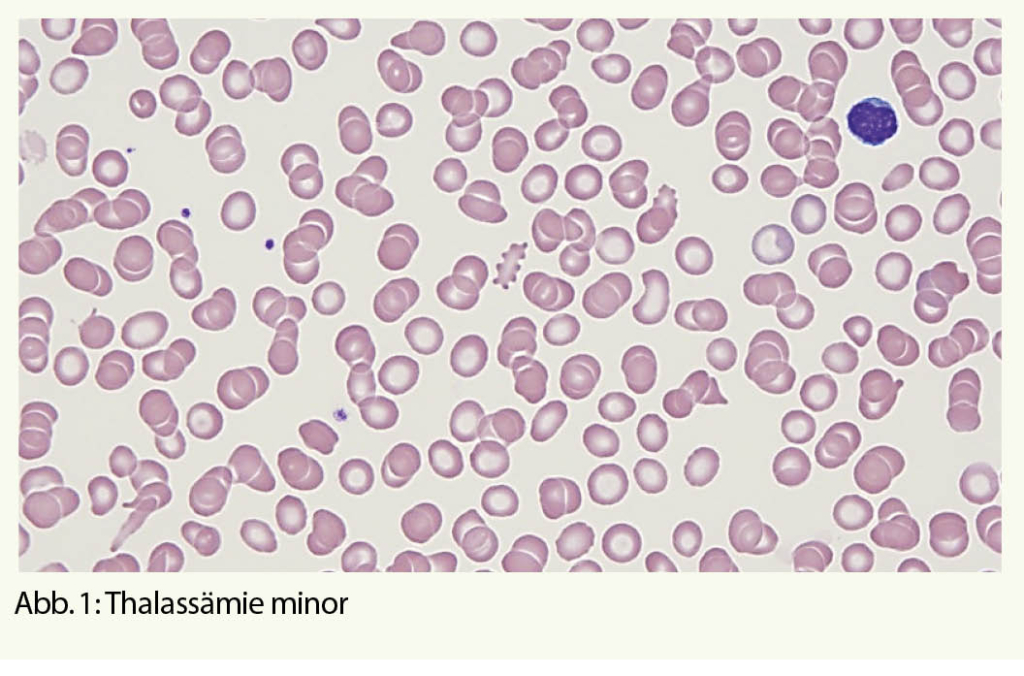
Die immunologischen, endokrinologischen und vaskulären Veränderungen während der Schwangerschaft führen zu verschiedenartigen Hautmanifestationen. Die wichtigstens dermatologischen Pathologien werden heute in vier Gruppen aufgeteilt, was die Nomenklatur beträchtlich vereinfacht hat.
Es können drei Hauptgruppen von Hautveränderungen unterschieden werden: Physiologische Hautveränderungen, schwangerschaftsspezifische Hautveränderungen (Schwangerschaftsdermatosen) sowie präexistente Hauterkrankungen, welche durch die Schwangerschaft positiv oder negativ beeinflusst werden.
Physiologische Hautveränderungen
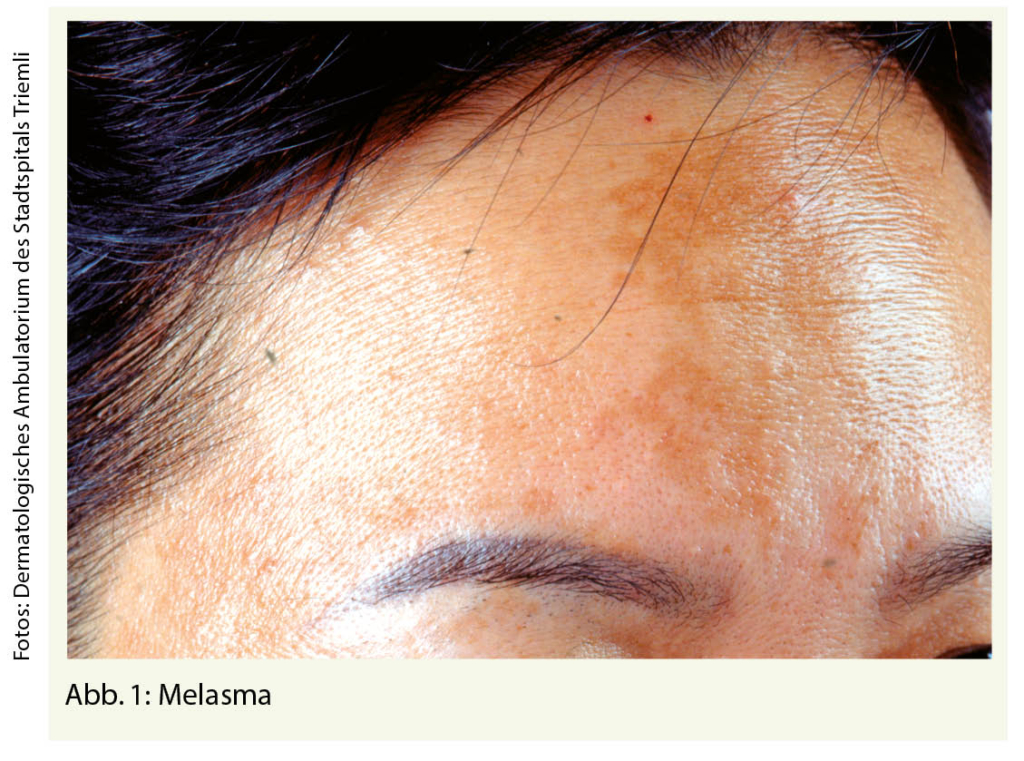
Die häufigsten physiologischen Veränderungen betreffen die Pigmentierung, das Haarwachstum sowie das Gefässsystem. Tab. 1 (1) gibt einen Überblick über diese Erscheinungen. Abbildung 1 zeigt das Melasma.
Spezifische Schwangerschaftsdermatosen
Als Schwangerschaftsdermatosen werden heute 4 Hauterkrankungen bezeichnet. Die aktuelle Klassifikation wurde 2006 von Ambros-Rudolph et al. (2) etabliert und fasst die früher verwendeten Bezeichnungen übersichtlich zusammen. In Tabelle 2 sind die aktuelle Klassifikation und die veralteten Synonyme dargestellt (3).
Pemphigoid gestationis (PG)
Diese Schwangerschaftsdermatose ist selten und kann während aller Trimester auftreten. Eine Manifestation in der Spätschwangerschaft oder unmittelbar postpartal ist aber häufig. Heftiger Juckreiz geht dem Auftreten der Hautveränderungen meist voraus. Typischerweise kommt es im Bereich des Abdomens, unter Einbezug der Periumbilikalregion zu urticariellen Erythemen, Papeln und Plaques sowie prallen Blasen. Ein Fortschreiten zu einem generalisierten bullösen Exanthem ist möglich. Zur Diagnosesicherung ist eine Probebiopsie für Histologie und direkte Immunfluoreszenz wichtig.
Die Erkrankung ist selbstlimitierend und bildet sich in der Regel innerhalb von Wochen bis Monaten nach der Geburt zurück. Auch eine Regredienz bis vor Termin mit nachfolgender Exazerbation zum Zeitpunkt der Geburt und unmittelbar postpartal ist möglich. Rezidive in Folgeschwangerschaften sind häufig. Auch während der Menstruation oder bei Einnahme oraler Kontrazeptiva kann es zu Ausbrüchen kommen. Es besteht eine Assoziation mit Autoimmunerkrankungen (M. Basedow, Hashimoto-Thyreoiditis, perniziöse Anämie). Wegen eines passiven Transfers von mütterlichen Autoantikörpern können in 10% selbstlimitierende Hautsymptome beim Neugeborenen auftreten. Eine erhöhte fetale Letalität besteht nicht, jedoch ist die Frühgeburtsrate und das Auftreten von «small-for-date babies» erhöht. Therapeutisch stehen die Kontrolle des Juckreizes und die Prävention der Blasenbildung im Vordergrund. In milden Fällen sind topische Steroide und Antihistaminika ausreichend, in schweren Fällen ist eine systemische Kortikosteroidtherapie notwendig (Prednison 0.5–1 mg/kg Körpergewicht). Eine Steigerung der Dosis kurz vor Geburt ist empfehlenswert, um eine eventuelle peripartale Exazerbation abzufangen (4).
Polymorphe Schwangerschaftsdermatose/Polymorphic eruption of pregnancy (PEP)
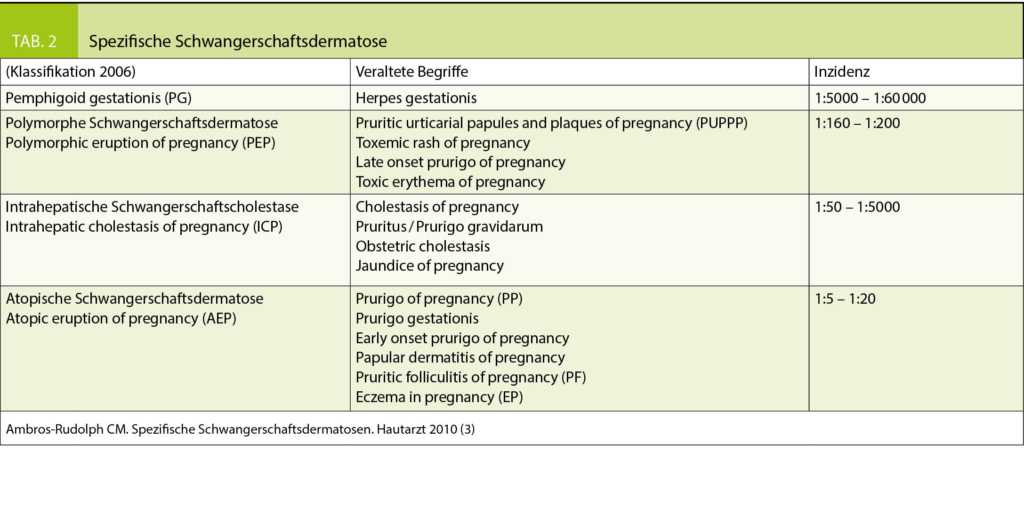
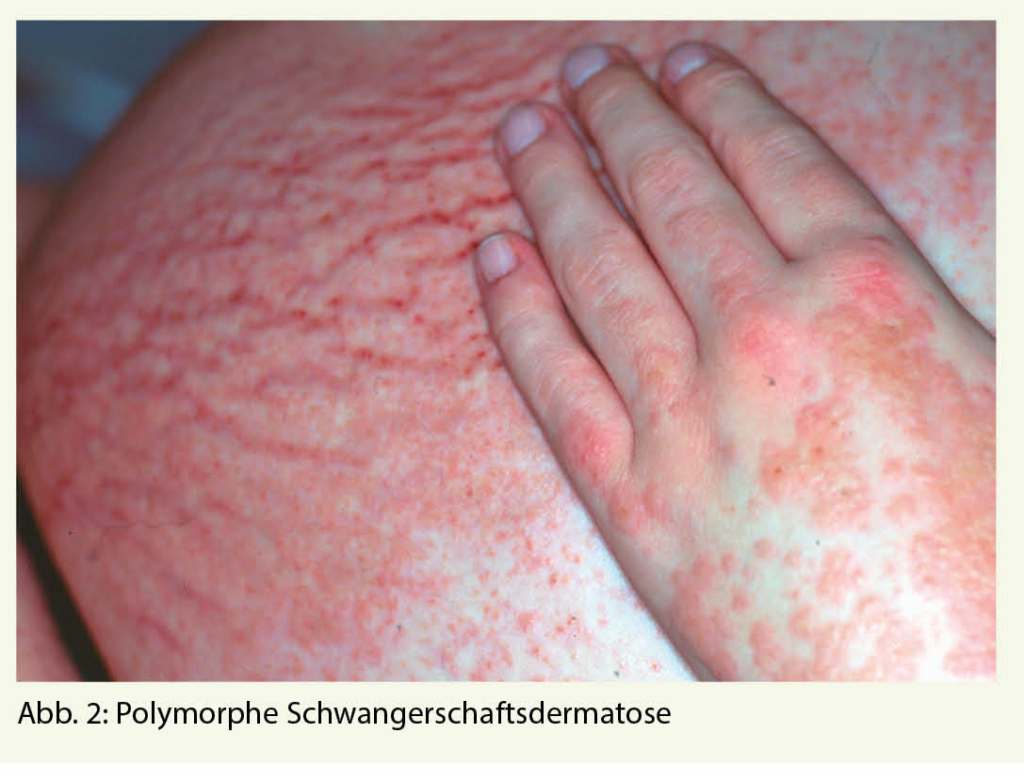
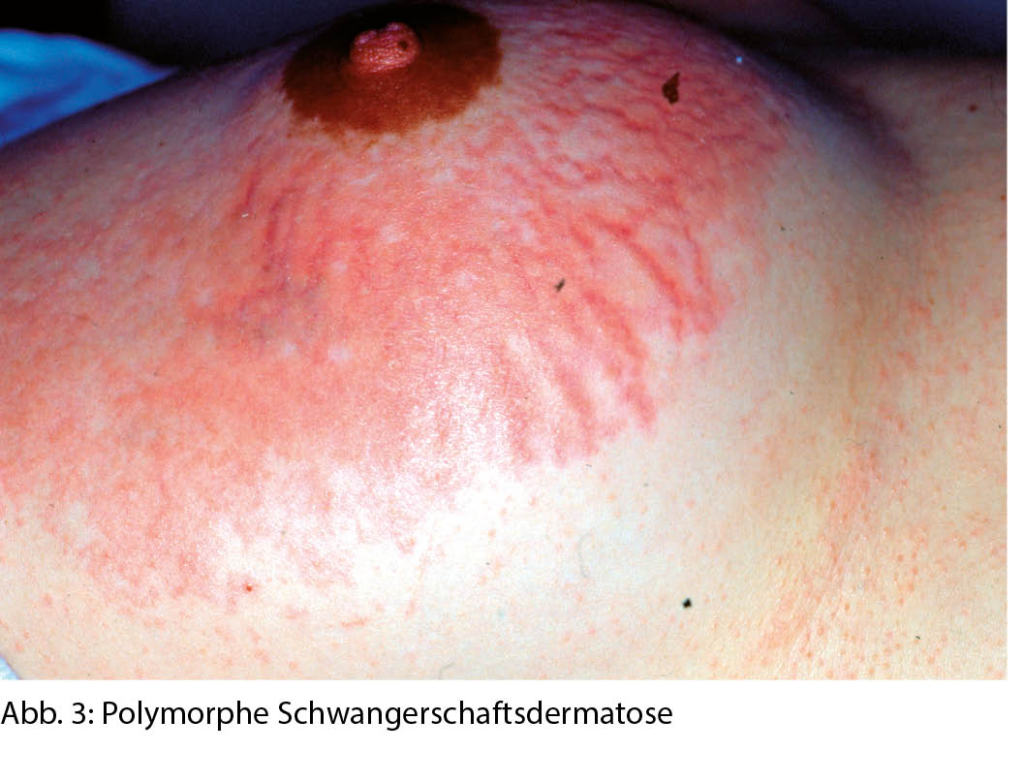
Die PEP ist eine häufige Schwangerschaftsdermatose und kann unterschiedliche klinische Bilder aufweisen. Die meisten Patientinnen weisen «juckende (pruritic) urticarielle Papeln und Plaques» auf, weshalb die Erkrankung früher als PUPPP bezeichnet wurde. Einige Betroffene präsentieren sich aber auch mit flächigen Erythemen und im Krankheitsverlauf kann es zu ekzematösen Läsionen, polyzyklischen Erythemen oder targetoiden bis multiforme-artigen Läsionen kommen. Es sind fast ausschliesslich Erstgebärende mit einem typischen Auftreten in den letzten Schwangerschaftswochen oder sogar postpartal betroffen. Bei Mehrlingsschwangerschaften tritt die Dermatose gehäuft auf. Die PEP beginnt mit starkem Juckreiz und mit erythematösen oder ödematösen Papeln und Plaques innerhalb der Striae distensae. In der Folge kommt es zur Ausbreitung auf Abdomen, Gesäss und Extremitäten (Abb. 2 und 3). Die periumbilikale Region bleibt ausgespart, dies ist ein wichtiges Abgrenzungsmerkmal zum Pemphigoid gestationis. Im Zweifelsfall kann eine Biopsie mit direkter Immunfluoreszenz durchgeführt werden. Hiermit gelingt eine eindeutige Abgrenzung zum PG. Die durchschnittliche Dauer bis zur Abheilung beträgt 4-6 Wochen. Rezidive in folgenden Schwangerschaften sind mit Ausnahme von Mehrlingsschwangerschaften nicht zu erwarten und ein fetales Risiko besteht nicht. Topische Kortikosteroide und systemische Antihistaminika sind in der Regel ausreichend, selten wird ein systemischer Steroidstoss benötigt. Weiter können unterstützend Menthol- oder Polidocanol haltige Externa eingesetzt werden.
Intrahepatische Schwangerschaftscholestase/Intrahepatic cholestasis of pregnancy (ICP)
Die ICP weist 4 Charakteristika auf: a) Juckreiz auf gesunder Haut im dritten Trimenon, b) erhöhte Gallensäurewerte im Serum > 10 µmol/l, c) spontanes Verschwinden der Symptome innert 48 h nach Geburt sowie Normalisierung der Gallensäuren innert 2–3 Wochen und d) Abwesenheit anderer Erkrankungen welche mit Pruritus oder Ikterus einhergehen.
Es liegt eine hormonell getriggerte, reversibile Cholestase bei genetisch prädisponierten Individuen vor. Die Inzidenz variiert stark mit dem ethnischen Hintergrund. So sind in Chile und Bolivien bis 15% der Schwangeren betroffen, während Europäerinnen nur in 1% betroffen sind. Allerdings ist die Inzidenz auch erhöht bei Mehrlingsschwangerschaften, bei Frauen über 35 Jahren, nach in-vitro-Fertilisation, bei ICP in einer vorangegangenen Schwangerschaft sowie bei vorbestehenden Gallenwegserkrankungen. Betroffene Schwangere klagen über massiven generalisierten Juckreiz ohne ein klinisches Korrelat auf der Haut. Zu Hauteffloreszenzen kommt es nur sekundär durch Kratzen. Der Juckreiz ist vor allem abends und an Palmae und Plantae ausgeprägt.
Die Brisanz der Erkrankung liegt in einem erhöhten fetalen Risiko: Frühgeburtlichkeit, Mekoniumaspiration und Totgeburten sind gehäuft, insbesondere wenn der Gallensäurewert im Serum 40µmol/l überschreitet. Somit richtet sich auch die Therapie danach, die fetale Prognose zu verbessern. Dies wird mit Ursodeoxycholsäure in einer Dosierung 15mg/kg/d erreicht. Diese Therapie verbessert auch die mütterlichen Symptome. Allgemeinmassnahmen wie Eincremen mit Emulsionen mit oder ohne juckreizstillende Zusätze sind ebenfalls hilfreich. Weiter können milde topische
Kortikosteroide eingesetzt werden (5).
Atopische Schwangerschaftdermatose/Atopic eruption of pregnancy (AEP)
Wie in Tabelle 2 ersichtlich, gibt es für diese Hauterkrankung viele Synonyme. Für den klinischen Alltag hat es sich aber bewährt, diese verschiedenen Bezeichnungen unter dem Begriff AEP zusammenzufassen.
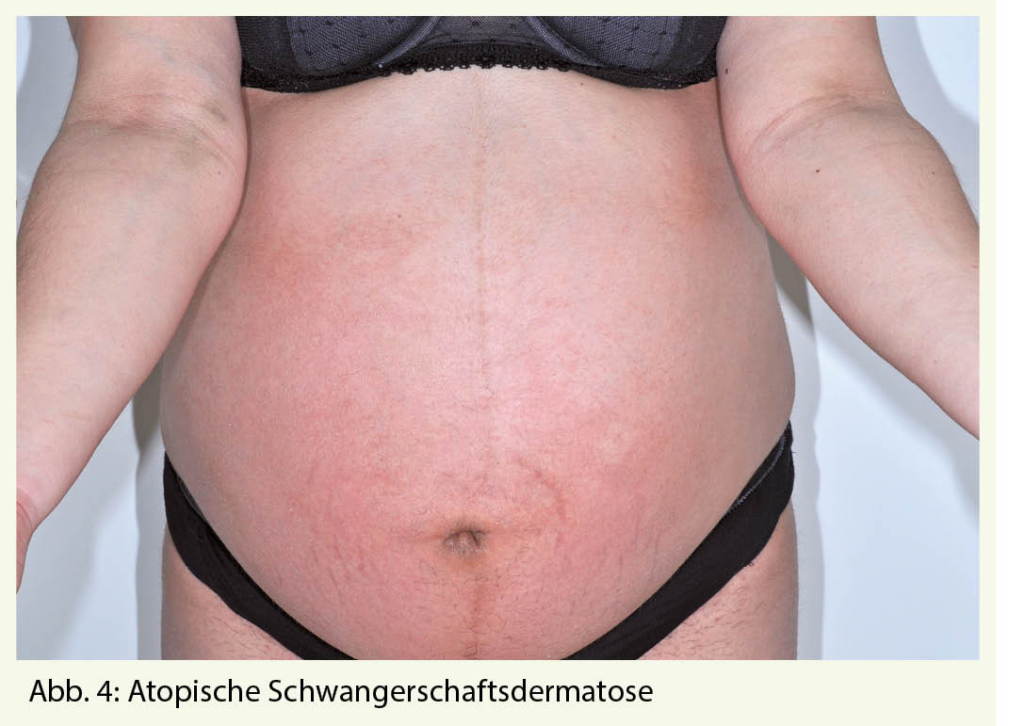
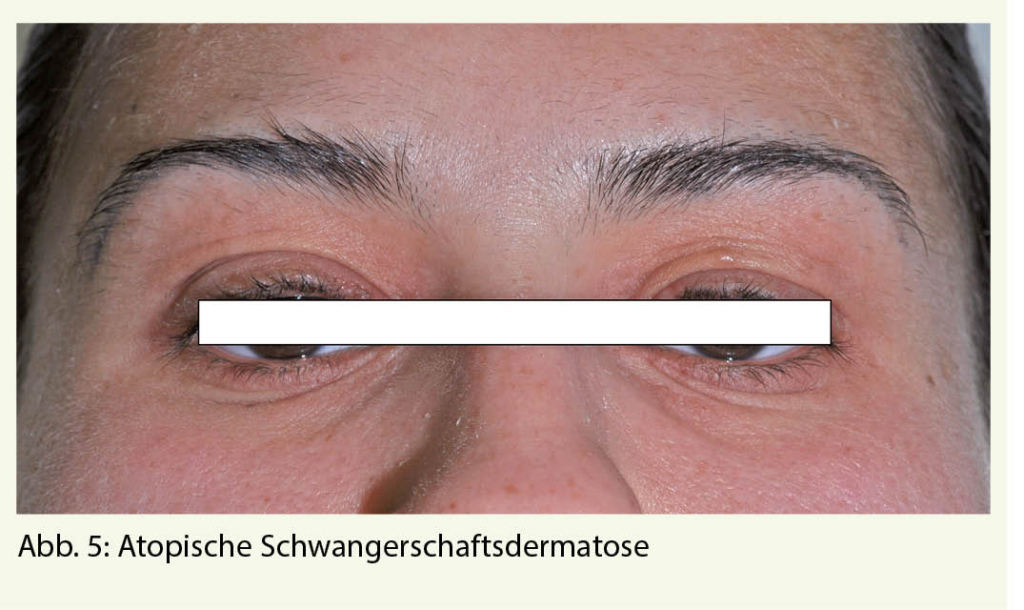
Die Atopische Schwangerschaftsdermatose ist die häufigste Ursache für Pruritus in der Schwangerschaft. Wahrscheinlich handelt es sich um eine Manifestationsform des atopischen Ekzems in der Schwangerschaft. Viele Patientinnen haben eine positive Eigen-oder Familienanamnese für Atopie und einen erhöhten gesamt IgE-Wert im Serum. In einem Fünftel der Fälle handelt es sich wahrscheinlich um eine Exazerbation eines vorbestehenden Atopischen Ekzems, beim Restanteil kommt es allerdings in der Schwangerschaft erstmals zum Auftreten von atopischen Hautveränderungen. Pathophysiologisch spielt die in der Schwangerschaft dominante Th2-Immunantwort eine Rolle. Da die Atopische Dermatitis eine typische Th2 dominante Erkrankung ist, scheint es naheliegend, dass eine solche in der Schwangerschaft ausgelöst werden oder sich verschlechtern kann. Der Beginn liegt meist vor dem dritten Trimester. Die AEP wird in zwei Typen unterteilt: Der E-Typ kommt bei 2/3 der Betroffenen vor und geht mit ekzematösen Hautveränderungen an den für die Atopische Dermatitis typischen Stellen einher. Involviert sind meist Gesicht, Hals und Gelenkbeugen (Abb. 4 und 5). Bei einem Drittel der Fälle liegt der P-Typ vor. Hier finden sich disseminierte kleinpapulöse Läsionen an Extremitäten und Stamm oder Prurigoläsionen insbesondere an den Extremitätenstreckseiten. Nach der Geburt kommt es üblicherweise zur spontanen Abheilung, gelegentlich wird aber auch eine Persistenz über Monate beobachtet. Rezidive in weiteren Schwangerschaften sind aufgrund der persistierenden Atopischen Diathese häufig. Ein assoziiertes kindliches Risiko besteht nicht. Zur Behandlung kommen kühlende hydrophile Lotionen, Crèmes oder Schüttelmixturen evtl. mit 2% Menthol- oder Polidocanol-Zusatz in Frage. Schwache bis mittelstarke lokale Kortikosteroide können ebenfalls eingesetzt werden. Selten ist der Einsatz von systemischen Glukokortikoiden oder H1-Antagonisten nötig. Nach Abheilung ist eine pflegende Rückfettung weiter zu empfehlen, da meist auch eine ausgeprägte Xerodermie besteht.
Pustulöse Psoriasis in der Schwangerschaft (PPP)
Einige Autoren postulieren die Pustulöse Psoriasis in der Schwangerschaft, früher auch als Impetigo herpetiformis bezeichnet, als fünfte Schwangerschaftsdermatose. Bei dieser Hauterkrankung handelt es sich um eine sehr seltene Variante einer generalisierten pustulösen Psoriasis während der Schwangerschaft, welche aufgrund ihrer erheblichen fetalen und maternalen Morbidität nennenswert ist. Sie manifestiert sich üblicherweise im 3. Trimenon.
Es liegt ein schweres Krankheitsbild vor mit initial intertriginösen Erythemen, die sich auf proximale Extremitätenabschnitte und den Rumpf ausdehnen. Rasch bilden sich darauf konfluierende Pusteln. Es bestehen zudem Allgemeinsymptome wie Fieber und Malaise, laborchemisch finden sich erhöhte Entzündungszeichen sowie gelegentlich eine Hypokalzämie. Die Symptome persistieren meist bis zur Geburt, gelegentlich auch länger. Sowohl Mutter als auch Kind sind gefährdet. Als Folge der schweren Erkrankung der Mutter sind intrauteriner Fruchttod oder Frühgeburten aufgrund einer Plazentainsuffizienz möglich. Therapeutisch werden Prednison oder Cyclosporin verabreicht, bei Superinfektion eine adäquate antibiotische Therapie. Bei schweren therapieresistenten Fällen muss eine Beendigung der Schwangerschaft in Betracht gezogen werden (6).
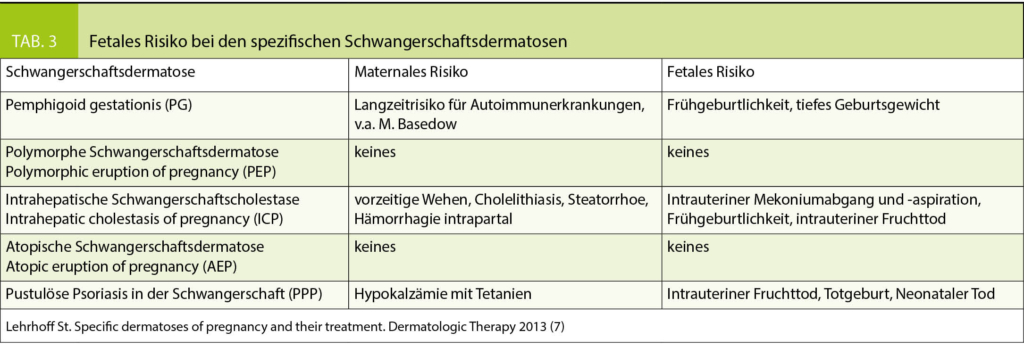
Tabelle 3 fasst das maternale und fetale Risiko bei den spezifischen Schwangerschaftsdermatosen zusammen (7).
Copyright bei Aerzteverlag medinfo AG
Dermatologie Bad Ragaz
Fläscherstrasse 21
7310 Bad Ragaz
derma.ragaz@hin.ch
Chefarzt
Institut für Dermatologie und Venerologie
Stadtspital Zürich
Herman Greulich-Str. 70
8004 Zürich
stephan.lautenschlager@triemli.zuerich.ch
Die Autoren haben im Zusammenhang mit diesem Artikel keine Interessenskonflikte deklariert.
1. Ambros-Rudolph CM. Dermatoses of pregnancy – clues to diagnosis, fetal risk and therapy. Ann Dermatol. 2011; 3:265-75
2. Ambros-Rudolph CM et al. The specific dermatoses of pregnancy revisited and reclassified: results of a retrospective two-centre study on 505 pregnant patients. J Am Acad Dermatol. 2006; 54:395-404
3. Ambros-Rudolph CM, Sticherling M. Spezifische Schwangerschaftsdermatosen. Hautarzt 2017;68: 87-94
4. Warshauer E, Mercurio M. Update on dermatoses of pregnancy. Int J Dermatol. 2013; 52:6-13
5. Ghosh S, Chaudhuri S. Intra-hepatic cholestasis of pregnancy: A comprehensive review. Indian J Dermatol. 2013; 58: 327
6. Roth M-M. Pegnancy Dermatoses. Diagnosis, Management and Controversies. Am J Clin Dermatol. 2011;12: 25-41
7. Lehrhoff St, Keltz Pomeranz M. Specific dermatoses of pregnancy and their treatment. Dermatologic Therapy. 2013;26:274-284