Gehen und Stehen ist für uns Menschen essentiell, 25-55% unserer Lebenszeit verbringen wir auf den Füssen. Doch nicht selten machen Schmerzen im Vorfuss den Alltag zur Qual. Einfache Einlagen führen nicht immer zu der gewünschten Besserung der Beschwerden, eine genaue Anamneseerhebung und Untersuchung ist differentialdiagnostisch von grosser Bedeutung.
Differentialdiagnose Vorfuss-Schmerz – worum handelt es sich?
Morton-Neuralgie
Hierbei handelt es sich um eine Neuropathie eines oder mehrerer Intermetatarsalnerven (Nervi digitales plantares communes). Es kann sich um eine einfache Neuritis handeln, in den meisten Fällen liegt jedoch eine strukturelle Veränderung des Nervs, eine sogenannte perineurale Fibrose bzw. ein Morton-Neurom, vor.
Die Neuritis wird durch eine Fehlbelastung verursacht. In der Folge kommt es zu einer mechanischen Reizung des Intermetatarsalnervs am distalen Ende, wo er eingebettet zwischen zwei Metatarsalia und dem sogenannten Intermetatarsal-Ligament, welches sich wie ein Dach über ihn spannt, liegt. Die Neuritis spricht in der Regel sehr gut auf Steroidinfiltrationen an.
Die neurale Fibrose oder das Morton-Neurom wird wahrscheinlich durch eine kontinuierliche Einengung des Nervs zwischen den beiden Metatarsalia und dem Ligamentum intermetatarsale verursacht, wobei die Ätiologie hier noch nicht endgültig geklärt ist. Im Falle einer Fibrosierung sind Steroidinfiltrationen deutlich weniger wirksam als bei einer einfachen Neuritis.
Sowohl bei der Neuritis als auch der perineuralen Fibrose löst eine Kompression des Nervs Schmerzen aus. Das Tragen von (zumeist engen) Schuhen führt zu einer Einengung des Intermetatarsalraumes, der zusätzliche Druck vom Boden bei Belastung zu einer weiteren Einklemmung des Nervs unterhalb des Ligamentum intermetatarsale.
Metatarsalgie
Der Metatarsalgie liegt eine mechanische Pathogenese zugrunde. Induziert durch verschiedenste Mechanismen kommt es zu einer Überbelastung eines oder mehrerer Metatarsaliaköpfchen, welche zu den entsprechenden Schmerzen führt. Häufig ist das Vorliegen eines Hallux valgus und/oder eine Verkürzung der Wadenmuskulatur hierfür verantwortlich.
Metatarsalgie bei Hallux valgus: Durch die Fehlstellung des ersten Metatarsale beim Hallux valgus kommt es zu einer Dezentrierung von Sehnenapparat und Plantaraponeurose, welche zu einem Verlust der Stützfunktion der Grosszehe führt. Die Bodenkräfte werden auf die benachbarten Metatarsalia verlagert, es kommt zu einer sogenannten Transfer-Metatarsalgie. Dabei ist der zweite Strahl am häufigsten betroffen, nicht selten auch das Metatarsale 3. Nur in Ausnahmefällen kommt es zu einer Metatarsalgie des vierten und fünften Strahls.
Metatarsalgie und verkürzte Wadenmuskulatur: Der Fuss ist über die Achillessehne mit der Wadenmuskulatur verbunden. Ist diese gut dehnbar, kann die Dorsalextension beim Abrollvorgang ohne grossen Widerstand erfolgen. Ist sie nicht ausreichend dehnbar bzw. verkürzt, kommt es durch den grösseren Widerstand und die dadurch verminderte Dorsalextension des Fusses zu einem erhöhten Druck auf die Metatarsalia-Köpfchen.
Auch eine Steilstellung der Metatarsalia bei Hohlfüssigkeit, eine Fettatrophie der Zehenballen beim älteren Menschen, die isolierte Hyperflexion eines Mittelfussknochens (kongenital, posttraumatisch, iatrogen) oder ossäre Destruktionen im Rahmen rheumatologischer oder vaskulärer Erkrankungen stellen seltenere Ursachen einer Metatarsalgie dar.
Ermüdungsfrakturen
Ermüdungsfrakturen entstehen in Folge einer dauerhaften Überbelastung des Knochens. In der Regel sind hiervon sportlich aktive Menschen betroffen, welche wöchentlich eine hohe Belastung auf sich nehmen – insbesondere Läufer. Das überbeanspruchte Gewebe erhält nicht genügend Zeit zur Regeneration, anatomische Skelettvarianten mit daraus resultierender Fehlbelastung des Fusses unterstützen diesen Prozess.
Eine Sonderform stellen die sogenannten pathologischen Frakturen dar, welche durch eine vorbestehende Schwächung des Knochens verursacht werden – durch die Einnahme von Medikamenten, im Rahmen tumoröser Erkrankungen oder als Folge der natürlichen Knochendichteminderung im Alter.
Periphere Polyneuropathie
Bei einer peripheren Polyneuropathie ist das Nervensystem ausserhalb des Hirns und Rückenmarks in seiner Funktion gestört. Dies kann angeboren oder Folge einer bestimmten Erkrankung wie z.B. Diabetes mellitus, Niereninsuffizienz, Infektionen oder Alkohol-abusus sein. Häufig bleibt die Ursache jedoch unklar.
Morbus Köhler II
Der Morbus Köhler II ist eine aseptische Knochennekrose des zweiten, seltener auch dritten Mittelfussköpfchens als Folge einer Durchblutungsstörung unklarer Genese. Primär betroffen sind in der Regel junge Mädchen im Alter von 12 bis 14 Jahren, häufig tritt diese Erkrankung bilateral auf. Wird im akuten Stadium nicht therapiert, kommt es im Verlauf zu einer Verformung des Köpfchens, welche durch die daraus resultierende Inkongruenz zu einer sekundären Arthrose des zweiten bzw. dritten Metatarsophalangeal-Gelenkes führen kann.
Anamnese – was berichtet der Patient?
Lokalisation der Schmerzen
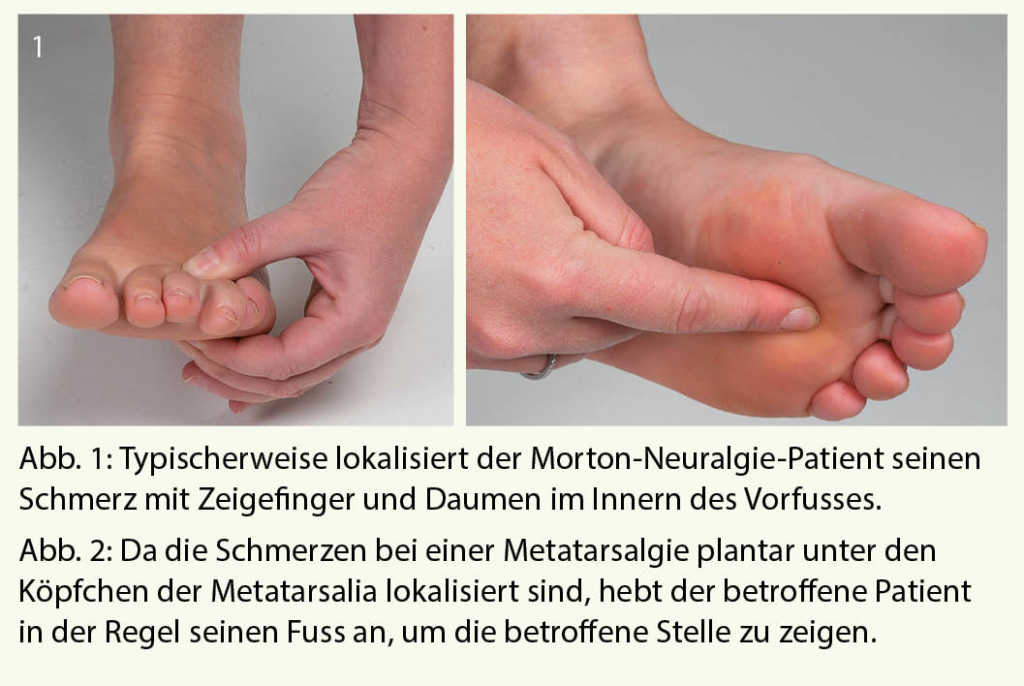
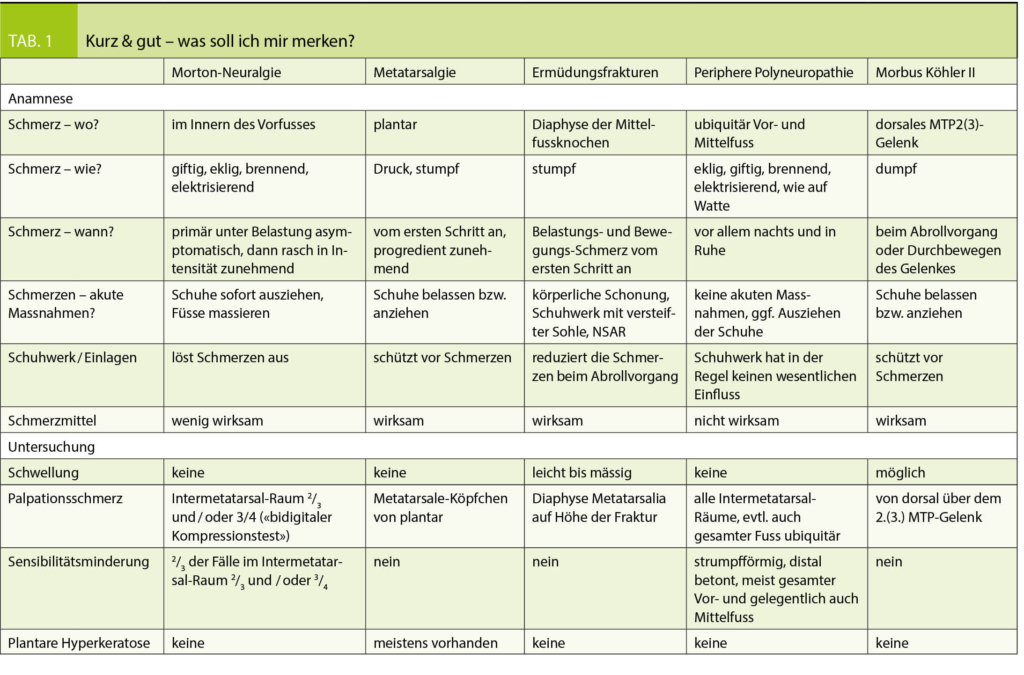
Morton-Neuralgie: Entsprechend der anatomischen Lage des Nervs werden die Schmerzen bei einer Morton-Neuralgie typischerweise im Innern des Vorfusses angegeben. Einen typischen Handgriff des Patienten beim Lokalisieren zeigt Abbildung 1. Häufig kommt es auch entlang der Nervenfasern nach distal zu einer Schmerzausstrahlung in die Zehen oder nach proximal in den Mittelfussbereich. Selten klagen Patienten über isolierte Schmerzen einer einzelnen Zehe (meistens Digitus 4), welche bei der klinischen Untersuchung palpatorisch nicht provoziert werden können.
Metatarsalgie: Da bei einer Metatarsalgie eine Druckproblematik im Bereich der Metatarsalia-Köpfchen vorliegt, werden die Schmerzen an der Planta pedis, das heisst unter dem Vorfuss angegeben. Der Patient hebt in typischer Weise seinen Fuss, um den Schmerz zu zeigen (Abbildung 2). Nicht selten beobachtet man auch eine plantare Hyperkeratose in diesem Bereich als Zeichen einer chronischen Überbelastung der Haut.
Den Ermüdungsfrakturen geht in der Regel eine körperliche Mehrbelastung voran. Häufig sind die über der Diaphyse des jeweiligen Mittelfussknochens lokalisierten Schmerzen zu Beginn nur gering ausgeprägt, die Symptomatik entwickelt sich schleichend. Nicht selten findet man auch eine diskrete Schwellung im schmerzhaften Bereich.
Die periphere Polyneuropathie verursacht Schmerzen, die denen der Morton-Neuralgie recht ähnlich sein können. Meist sind jedoch sämtliche Zehen oder sogar der gesamte Fuss/Unterschenkel betroffen. Auch wird mit zunehmendem Krankheitsverlauf ein Unsicherheitsgefühlt («Laufen wie auf Watte») beschrieben.
Bei Vorliegen eines Morbus Köhler II gibt der Patient Bewegungsschmerzen im Bereich des zweiten oder seltener auch dritten Metatarsophalangealgelenkes als Folge der Gelenkflächeninkongruenz und der daraus resultierenden Arthrose an. Diese sind in der Regel dorsalseitig lokalisiert.
Schmerzcharakter – wie beschreibt es der Patient?
Morton-Neuralgie: Der durch die Morton-Neuralgie ausgelöste Schmerz ist neuropathischen Charakters und wird somit in der Regel als äusserst intensiv wahrgenommen. Nicht selten fallen Worte wie «giftig», «brennend» oder «stechend». Auch kommt es häufig zu einem Schwellungs- oder Fremdkörpergefühl, welches ähnlich einer Sockenfalte oder eines Reiskornes beschrieben wird. Übliche Schmerzmedikamente helfen in der Regel wenig oder gar nicht.
Metatarsalgie: Der mechanischen Ursache entsprechend werden Schmerzen bei einer Metatarsalgie als «dumpf» beschrieben und sprechen in der Regel gut auf Schmerzmedikamente an.
Ähnlich verhält es sich mit den Ermüdungsfrakturen.
Eine periphere Polyneuropathie kann sich durch vielfältige Symptome äussern, vorrangig sind jedoch Missempfindungen im Sinne von Kribbeln, brennenden Schmerzen, Ameisenlaufen, Hypästhesien und sogar Gangunsicherheiten.
Der klassische Morbus Köhler II-Patient beschreibt dorsalseitige Schmerzen im Zehen-Grundgelenk beim Abrollvorgang.
Auslösende Ursachen – wann treten die Schmerzen auf?
Morton-Neuralgie: Da die Schmerzen bei einer Morton-Neuralgie durch eine Kompression des Intermetatarsalnervs ausgelöst werden, treten sie typischerweise in geschlossenem Schuhwerk auf. Der Patient kann in der Regel zunächst eine gewisse Gehstrecke schmerzfrei zurücklegen, bis es zu plötzlich einschiessenden oder in Intensität rasch zunehmenden Schmerzen kommt. Pausieren ist notwendig, das Ausziehen der Schuhe bewirkt eine zügige Linderung der Beschwerden.
Metatarsalgie: Da es sich bei der Metatarsalgie um eine Druckproblematik handelt, werden leichte Schmerzen schon beim ersten Schritt bemerkt. Diese nehmen mit zunehmender Gehstrecke kontinuierlich zu.
Da sich Ermüdungsfrakturen in der Regel schleichend entwickeln, sind zu Beginn nur leichte Schmerzen unter Belastung spürbar. Wird die körperliche Belastung im Verlauf nicht reduziert, kann es zu einer Progredienz der Symptomatik kommen.
Die Symptome einer peripheren Polyneuropathie treten unabhängig von äusseren Einwirkungen wie Belastung oder Kompression auf. Häufig sind sie nachts und in Ruhe vorhanden. Nicht selten tritt beim Mobilisieren sogar eine Besserung der Beschwerden ein.
Die Schmerzen bei Vorliegen eines Morbus Köhler II treten vor allem beim Abrollvorgang und beim Durchbewegen des Gelenkes auf. Primär ist die Dorsalextension davon betroffen.
Welchen Einfluss hat das Schuhwerk?
Morton-Neuralgie: Da geschlossenes Schuhwerk zu einer Kompression der benachbarten Metatarsalia und nachfolgend des Intermetatarsalnervs führt, läuft der klassische Morton-Neuralgie-Patient am liebsten barfuss.
Metatarsalgie: Da entsprechendes Schuhwerk die Mittelfussköpfchen vor einer Druckbelastung des Bodens schützt, trifft man Metatarsalgie-Patienten eher selten barfuss an. Am liebsten werden Schuhe mit weicher Innen- und stabiler Aussensohle getragen. Eine zusätzliche Abrollhilfe führt durch Verteilung der Bodenkräfte beim Abrollvorgang zu einer weiteren Erleichterung für die Patienten.
Auch Patienten mit Ermüdungsfrakturen oder Vorliegen eines
Morbus Köhler II erfahren eine Regredienz der Beschwerden durch Schuhwerk mit stabiler Sohle, da diese beim Abrollvorgang die mechanische Belastung der betroffenen Areale reduziert.
Die periphere Polyneuropathie wird durch Schuhwerk nicht beeinflusst.
Sind Einlagen hilfreich?
Morton-Neuralgie: Da klassische orthopädische Einlagen zu einer weiteren Reduktion des Raumes im Schuh führen, kommt es in der Regel zu einer Zunahme der Schmerzen.
Metatarsalgie: Orthopädische Masseinlagen bilden einen der Pfeiler der konservativen Metatarsalgie-Behandlung, da sie durch die retrokapitale Abstützung den Druck auf die Mittelfussköpfchen eduzieren. Zusätzlich kann der schmerzhafte Bereich entsprechend gepolstert werden.
Ermüdungsfrakturen: Das Tragen von Karbonfasereinlagen reduziert die mechanische Belastung des betroffenen Areals und führt dadurch zu einer Linderung der Schmerzen und Förderung der Knochenheilung. Meist ist jedoch auch gutes Konfektionsschuhwerk mit stabiler Sohle ausreichend.
Einlagen beeinflussen die bei der peripheren Polyneuropathie vorliegenden Missempfindungen in keinerlei Hinsicht.
Morbus Köhler II-Patienten erfahren ebenfalls durch rigide Einlagen eine gewisse Linderung ihrer Beschwerden.
Klinische Untersuchung – wie kann ich meine anam-nestische Verdachtsdiagnose klinisch verifizieren?
Morton-Neuralgie
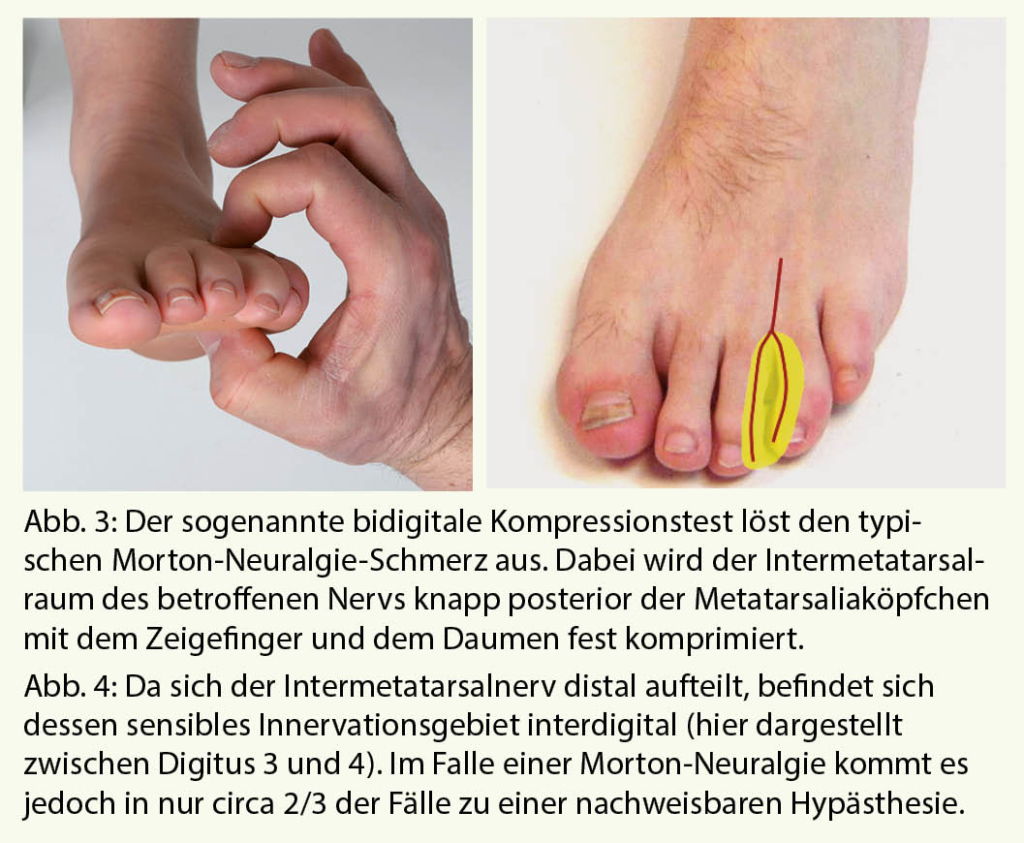
Durch eine gezielte Kompression des betroffenen Intermetatarsalnervs kann der typische Morton-Neuralgie-Schmerz ausgelöst werden. Hierfür wendet man den sogenannten bidigitalen Kompressionstest an (Abb. 3). Die für den Patienten typischen heftigen neuropathischen Schmerzen treten auf.
Des Weiteren lassen sich bei circa zwei Drittel der Fälle Hypästhesien im Versorgungsgebiet des jeweiligen Intermetatarsalnervs nachweisen (Abb. 4). Bei den übrigen 30% der Menschen liegt eine Doppelinnervation dieses Areals von dorsal vor, eine Sensibilitätsstörung ist entsprechend nicht zu finden.
Metatarsalgie
Durch Reproduktion des Bodendruckes auf die Metatarsalia kann der für den Patienten typische Schmerz provoziert werden. Dabei werden die Köpfchen der Mittelfussknochen palpatorisch geortet und Druck auf sie ausgeübt. Die dadurch ausgelösten Schmerzen sind von dumpfem Charakter und bei weitem nicht so intensiv wie die neuropathischen Schmerzen bei einer Morton-Neuralgie. Nicht selten kann man auch eine plantare Hyperkeratose als Ausdruck einer chronischen mechanischen Überbelastung der Haut nachweisen.
Ermüdungsfrakturen
Diese verursachen Schmerzen, welche durch direkte Palpation der Diaphyse des betroffenen Metatarsale ausgelöst werden können. Häufig zeigt sich auch eine diskrete Schwellung in diesem Bereich.
Periphere Polyneuropathie
Die periphere Polyneuropathie verursacht Schmerzen, die denen der Morton-Neuralgie recht ähnlich sind. Da eine Morton-Neuralgie jedoch in 99% der Fälle zwischen den Metatarsalia 2 und 3 bzw. 3 und 4 auftritt, extrem selten zwischen 4 und 5 und niemals zwischen 1 und 2, sollten bei der klinischen Untersuchung immer alle Intermetatarsalräume überprüft werden. Sind Druckdolenzen ubiquitär vorhanden, kommt eine klassische Morton-Neuralgie nicht in Frage. Das Vorliegen einer peripheren Polyneuropathie ist wahrscheinlich.
Morbus Köhler II
Beim Morbus Köhler II lassen sich Schmerzen durch palpatorischen Druck auf das zweite und/oder dritte Metatarsophalangealgelenk von dorsal auslösen, hin und wieder ist hier auch eine diskrete Schwellung vorhanden. Die Beweglichkeit ist schmerzbedingt eingeschränkt, wobei – Impingement-bedingt – primär die Dorsalextension und erst im Verlauf auch zusätzlich die Plantarflexion betroffen ist. Gelegentlich ist auch intraartikuläres Krepitieren nachweisbar.
Welche Zusatzuntersuchungen sind sinnvoll?
Konventionelles Röntgen:
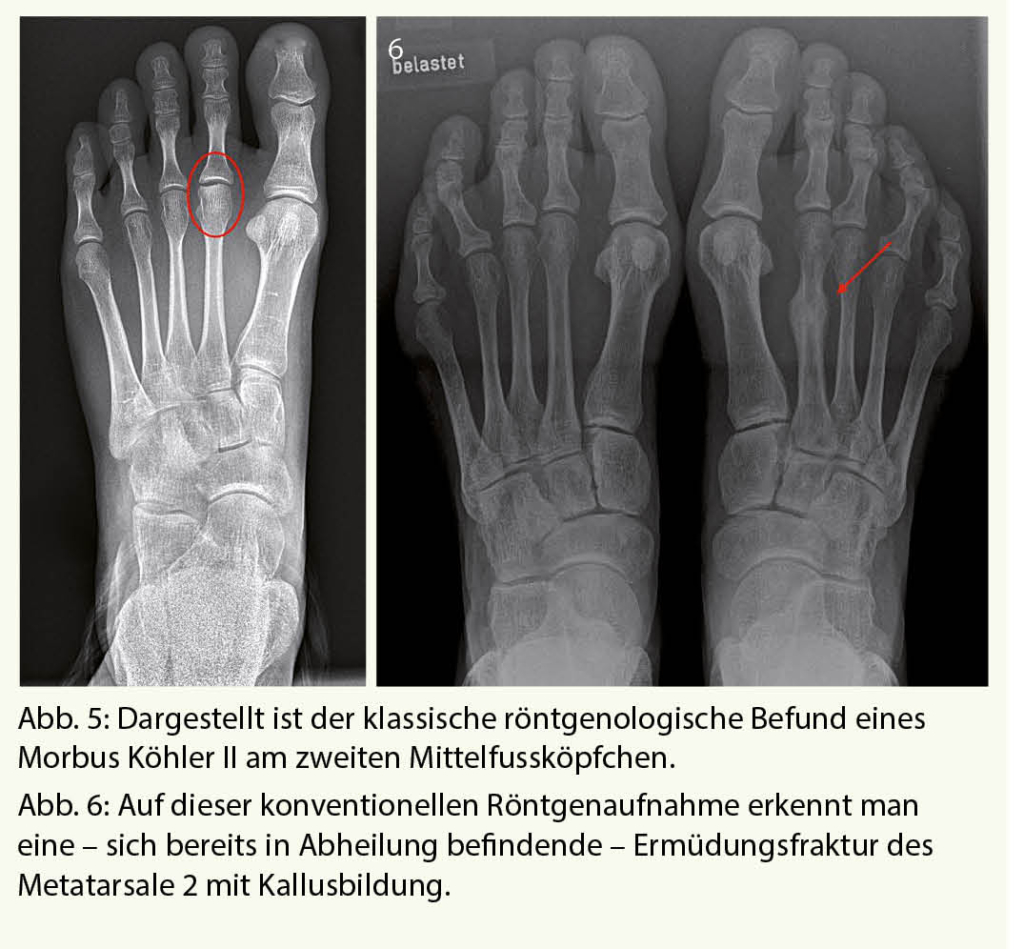
Röntgenaufnahmen unter Belastung gehören zur Standarduntersuchung eines jeden schmerzhaften Vorfusses. Pathologien an den Mittelfussköpfchen oder Ermüdungsfrakturen können hiermit in der Regel zufriedenstellend diagnostiziert werden (Abb. 5 und 6). Dabei muss jedoch beachtet werden, dass Ermüdungsfrakturen oft erst 2-3 Wochen nach Schmerzbeginn anhand der beginnenden Kallusbildung sichtbar werden.
MRI:
Im Anfangsstadium eines Morbus Köhler II oder wenn eine Ermüdungsfraktur im konventionellen Röntgen nicht sicher nachweisbar ist, kann eine MRI-Untersuchung zusätzliche Informationen liefern.
Bei Verdacht auf ein Morton-Neurom macht eine MRI-Untersuchung allerdings nur wenig Sinn. Zum einen kann die Diagnose klinisch und anamnestisch mit einer sehr hohen Treffsicherheit gestellt werden, zum anderen ist der Intermetatarsalnerv – wie unsere zwanzigjährige operative Erfahrung gezeigt hat – in nur circa 50% der Fälle verdickt, was bedeutet, dass die Hälfte der Morton-Neurome im MRI nicht nachweisbar ist. Äusserst problematisch sehen wir auch die Tatsache an, dass nicht selten im schriftlichen Befund der Radiologen «Kein Morton-Neurom» dokumentiert wird. Dies löst die Suche nach einer anderen Pathologie aus und zieht eine für den Patienten unbefriedigende Therapie nach sich. Korrekterweise dürfte der Radiologe in seinem Bericht nur festhalten, dass der Nerv nicht verdickt ist – ob es sich dabei um ein Morton-Neurom handelt oder nicht, kann er anhand der Bilder nicht sagen.
Sonographie:
Hinsichtlich der Verdachtsdiagnose Morton-Neurom gelten die gleichen Überlegungen wie bei der MRI-Untersuchung.
Computertomographie:
Zur Beurteilung der ossären Durchbauung liefert ein CT wegweis-ende Informationen.
Eine elektrophysiologische Untersuchung ist recht aufwendig und schmerzhaft, erbringt wenig zusätzliche Informationen und wird deswegen bei Verdacht auf Morton-Neuralgie nur selten empfohlen. Zur Bestätigung einer vermuteten peripheren Polyneuropathie kann diese allerdings hilfreich sein.
Konservative Therapie – wie kann ich meinem Patienten in der Praxis helfen?
Morton-Neuralgie
Eine lokale Steroidinfiltration ist die konservative Behandlung der Wahl. Wir empfehlen 0,5ml Betamethasoni Dipropionas (Diprophos® 5mg+2mg) gemischt mit 1ml Lokalanästhetikum pro Intermetatarsalraum.
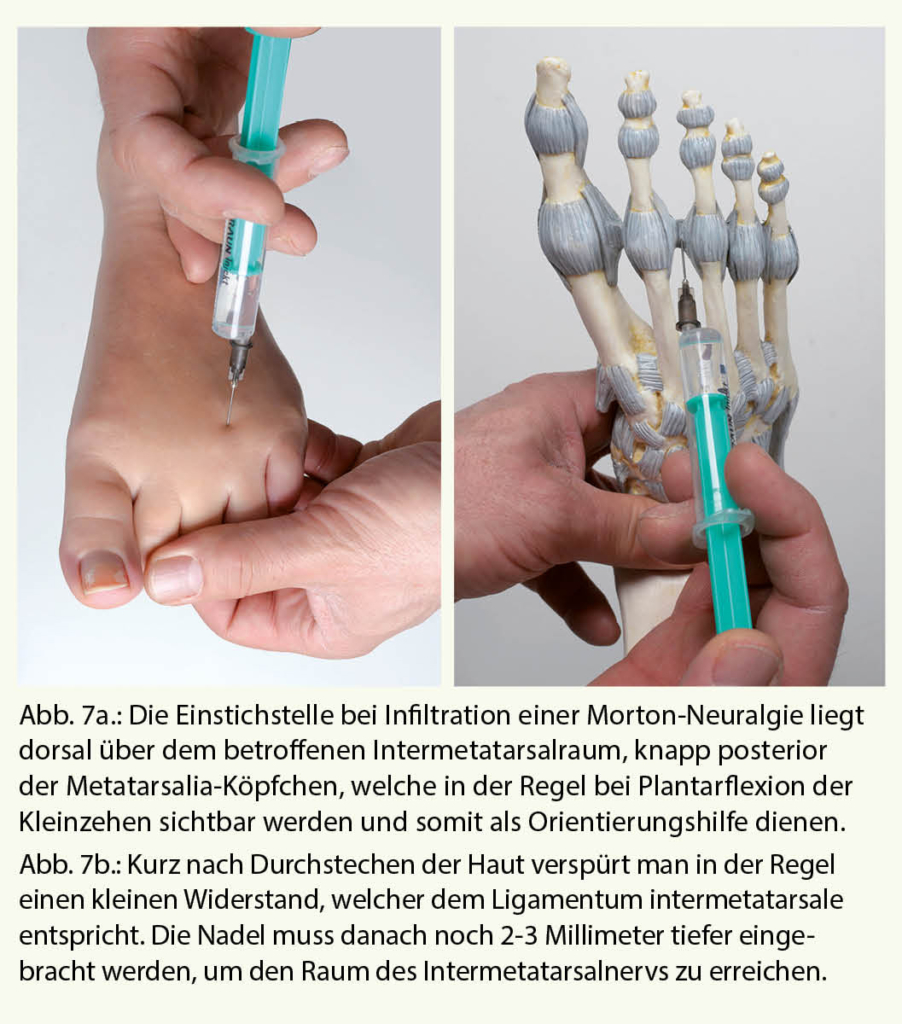
Der Stich erfolgt von dorsal, da eine Infiltration durch die Fusssohle äusserst schmerzhaft ist, die Injektion der Lösung selbst aber erst bei plantarer Position der Nadel, da hier der Nerv lokalisiert ist: Kurz nach Durchstechen der Haut verspürt man einen kleinen Widerstand, welcher dem Ligamentum intermetatarsale entspricht. Die Nadel muss danach noch 2-3 Millimeter tiefer eingebracht werden, um den Raum des Nervus digitalis plantaris communis zu erreichen (Abb. 7a und b).
Falls nach der Steroidinfiltration eine längerfristige, für den Patienten jedoch noch nicht befriedigende Besserung der Beschwerdesymptomatik eintritt, kann eine weitere Infiltration nach vier bis sechs Wochen durchgeführt werden.
Bei nur geringem Ansprechen oder lediglich kurzfristiger Verbesserung der Situation macht eine weitere Infiltration wenig Sinn – eine chirurgische Exzision muss bei gegebenem Leidensdruck diskutiert werden.
Wie bereits erwähnt, sind orthopädische Masseinlagen kontraproduktiv, da sie zu einer weiteren Einengung des Fusses im Schuh führen und dadurch eine Kompression des Nervs begünstigen.
Metatarsalgie und Morbus Köhler II
Liegt eine signifikante Verkürzung der Wadenmuskulatur vor, erfolgt die Therapie primär durch eine konsequente, mehrmals täglich durchgeführte Aufdehnung (Abb. 8).
Zudem kann bei Vorliegen einer klassischen Metatarsalgie durch Einlagen eine wirksame Linderung der Schmerzen erreicht werden. Diese sollen retrokapital abstützen, um den Druck beim Abrollvorgang auf schmerzfreie Areale zu verteilen, und darüber hinaus im Bereich der Metatarsaliaköpfchen gut gepolstert sein.
Das Schuhwerk sollte eine stabile Sohle aufweisen, welche am besten sogar zusätzlich mit einer kleinen Abrollhilfe ausgestattet ist. Dies führt zu einer Verteilung der Bodenkräfte, was wiederum den Druck auf die schmerzhaften Mittelfussköpfchen bei einer Metatarsalgie bzw. das Bewegungsausmass des betroffenen Gelenkes bei einem Morbus Köhler II reduziert. Die meisten guten Turn- oder Wanderschuhe bieten diese Eigenschaften, ein spezieller orthopädischer Schuh ist in der Regel nicht erforderlich.
Ermüdungsfrakturen
Abhängig von der Ursache ist bei Ermüdungsfrakturen in der Regel eine körperliche Schonung sowie das Tragen von Schuhen mit
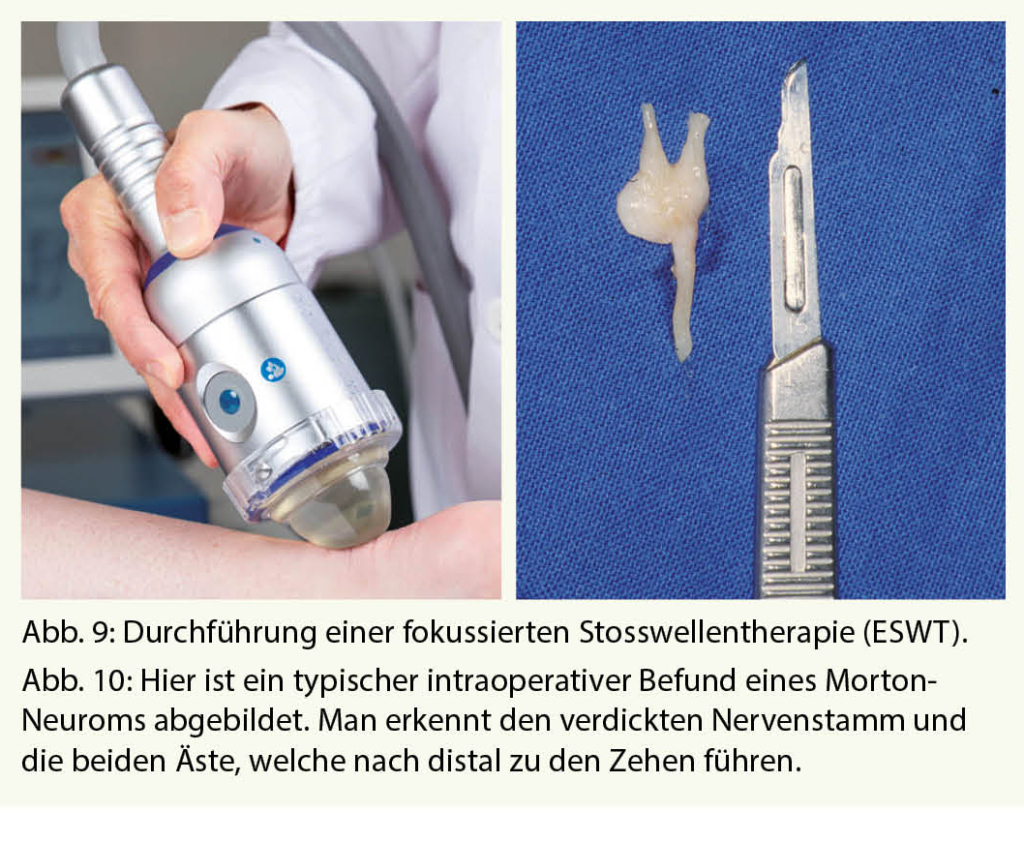
versteifter Sohle bzw. Karbonfasereinlagen für die Dauer von vier bis sechs Wochen ausreichend. Sollte es darunter zu keiner Abheilung kommen, sollten weitere kausale Abklärungen erfolgen. Auch kann die additive Durchführung einer fokussierten extrakorporalen Stosswellentherapie (ESWT) unterstützend hilfreich sein (Abb. 9).
Periphere Polyneuropathie
In der Regel wird die periphere Polyneuropathie kausal behandelt. Ist dies nicht möglich, kommen Medikamente zum Einsatz. Als wirksam haben sich trizyklische Antidepressiva sowie Antikonvulsiva wie Carbamazepin oder Gabapentin erwiesen. Leider werden diese jedoch häufig aufgrund der ausgeprägten Nebenwirkungen nur bedingt vertragen. Eine zusätzliche Bewegungstherapie zur Förderung der gestörten Motorik, Reduktion von Durchblutungsstörungen und Aufrechterhaltung der Mobilität ist zusätzlich ratsam.
Operative Therapie – was tun, wenn konservative Massnahmen nicht ausreichend geholfen haben?
Morton-Neuralgie
Die Resektion des veränderten Nervensegments im distalen Intermetatarsalraum ist die operative Therapie der Wahl, sollten konservative Therapiemassnahmen nicht ausreichend ansprechen (Abb. 10).
Diese kann problemlos in einem supramalleolären Fussblock durchgeführt werden, der Zugang erfolgt von plantar oder dorsal. Da der plantare Zugangsweg den Vorteil einer besseren Darstellung des Nervs hat, ausserhalb der Belastungszone durchgeführt werden kann und in diesem Bereich eine ausgesprochen gute Wundheilung stattfindet, wird in unserer Abteilung dieser dem dorsalen Zugang bevorzugt.
Die Erfolgsquote («Ich würde die Operation auf jeden Fall wieder machen lassen.») liegt bei circa 95%. Restbeschwerden sind meistens bedingt durch eine Narbenbildung im Bereich des Nervenstumpfes oder durch Phantomschmerzen. Die plantare Zugangsnarbe selbst bleibt lediglich für wenige Monate bemerkbar und bereitet danach keinerlei Probleme mehr.
Metatarsalgie
Eine operative Therapie ist nur selten notwendig. Je nach zugrundeliegender Pathologie stellen jedoch diverse Korrektur-Osteotomien und/oder ein chirurgisches Lösen der Wadenmuskulatur Möglichkeiten dar.
Ermüdungsfrakturen
In der Regel ist ein chirurgischer Eingriff bei Ermüdungsfrakturen nicht notwendig. Liegen ursächlich anatomische Skelettvarianten mit Fehlbelastung vor, sollte eine Korrektur dieser diskutiert werden.
Periphere Polyneuropathie
Operative Massnahmen kommen bei einer peripheren Polyneuropathie lediglich zu diagnostischen Zwecken in Frage im Rahmen einer Biopsie.
Morbus Köhler II
Bei einem Morbus Köhler II sind konservative Therapiemassnahmen häufig nicht ausreichend. Es stehen uns Umstellungsosteotomien des Mittelfussköpfchens zur Verfügung, welche zu guten postoperativen Ergebnissen führen.
Fusschirurgie Schulthess Klinik
Lengghalde 2
8008 Zürich
simone.zwicky@kws.ch
Fusschirurgie Schulthess Klinik
Lengghalde 2
8008 Zürich
Die Autoren haben keinen Interessenskonflikt im Zusammenhang mit diesem Artikel deklariert.
1 Yun H, Xie F, Delzell E, Levitan EB, Chen L, Lewis JD, Saag KG, Beukelman T, Winthrop KL, Baddley JW, Curtis JR. Comparative Risk of Hospitalized Infection Associated With Biologic Agents in Rheumatoid Arthritis Patients Enrolled in Medicare. Arthritis Rheumatol. 2016 Jan;68(1):56-66. doi: 10.1002/art.39399.
2 Keystone EC, Taylor PC, Tanaka Y, Gaich C, DeLozier AM, Dudek A, Zamora JV, Cobos JAC, Rooney T, Bono S, Arora V, Linetzky B, Weinblatt ME. Patient-reported outcomes from a phase 3 study of baricitinib versus placebo or adalimumab in rheumatoid arthritis: secondary analyses from the RA-BEAM study. Ann Rheum Dis. 2017 Nov;76(11):1853-1861. doi: 10.1136/annrheumdis-2017-211259. Epub 2017 Aug 10.
3 Cohen SB, Tanaka Y, Mariette X, Curtis JR, Lee EB, Nash P, Winthrop KL, Charles-Schoeman C, Thirunavukkarasu K, DeMasi R, Geier J, Kwok K, Wang L, Riese R, Wollenhaupt J. Long-term safety of tofacitinib for the treatment of rheumatoid arthritis up to 8.5 years: integrated analysis of data from the global clinical trials. Ann Rheum Dis. 2017 Jul;76(7):1253-1262. doi: 10.1136/annrheumdis-2016-210457. Epub 2017 Jan 31.
4 Liu Y, Zhou S, Wan Y, Wu A, Palmisano M. The impact of co-administration of ketoconazole and rifampicin on the pharmacokinetics of apremilast in healthy volunteers. Br J Clin Pharmacol. 2014 Nov;78(5):1050-7. doi: 10.1111/bcp.12448.
5 Strangfeld A, Zink A. Safety of biologic therapy – results from the German biologics register RABBIT. Dtsch Med Wochenschr. 2014 Sep;139(37):1817-20. doi: 10.1055/s-0034-1370252. Epub 2014 Sep 2.
6 Homepage Schweizerische Gesellschaft für Rheumatologie: http://www.rheuma-net.ch/download/Content_attachments/FileBaseDoc/Antirheumatische-Therapie-in-der-Schwangerschaft-Emfehlungen-SGR-01-2016.pdf
7 Götestam Skorpen C, Hoeltzenbein M, Tincani A, Fischer-Betz R, Elefant E, Chambers C, da Silva J, Nelson-Piercy C, Cetin I, Costedoat-Chalumeau N, Dolhain R, Förger F, Khamashta M, Ruiz-Irastorza G, Zink A, Vencovsky J, Cutolo M, Caeyers N, Zumbühl C, Østensen M. The EULAR points to consider for use of antirheumatic drugs before pregnancy, and during pregnancy and lactation. Ann Rheum Dis. 2016 May;75(5):795-810. doi: 10.1136/annrheumdis-2015-208840. Epub 2016 Feb 17.
8 Pottinger EM, Woolf RT, Exton LS, Burden AD, Nelson-Piercy C, Smith CH. Exposure to biologic therapies during conception and pregnancy: a systematic review. Br J Dermatol. 2017 Jul 18. doi: 10.1111/bjd.15802. [Epub ahead of print].
9 Klinkenberg RE, Gelinck LB. Influenza vaccination in immunocompromised patients. Ned Tijdschr Geneeskd. 2014;158:A7574.
10 Hua C, Barnetche T, Combe B, Morel J. Effect of methotrexate, anti-tumor necrosis factor α, and rituximab on the immune response to influenza and pneumococcal vaccines in patients with rheumatoid arthritis: a systematic review and meta-analysis. Arthritis Care Res (Hoboken). 2014 Jul;66(7):1016-26. doi: 10.1002/acr.22246.
11 Wadström H, Frisell T, Askling J; Anti-Rheumatic Therapy in Sweden (ARTIS) Study Group. Malignant Neoplasms in Patients With Rheumatoid Arthritis Treated With Tumor Necrosis Factor Inhibitors, Tocilizumab, Abatacept, or Rituximab in Clinical Practice: A Nationwide Cohort Study From Sweden. JAMA Intern Med. 2017 Nov 1;177(11):1605-1612. doi: 10.1001/jamainternmed.2017.4332.
12 Ramiro S, Sepriano A, Chatzidionysiou K, Nam JL, Smolen JS, van der Heijde D, Dougados M, van Vollenhoven R, Bijlsma JW, Burmester GR, Scholte-Voshaar M, Falzon L, Landewé RBM. Safety of synthetic and biological DMARDs: a systematic literature review informing the 2016 update of the EULAR recommendations for management of rheumatoid arthritis. Ann Rheum Dis. 2017 Jun;76(6):1101-1136. doi: 10.1136/annrheumdis-2016-210708. Epub 2017 Mar 15.