Bei beeinträchtigter Harnblasenentleerung kann die Einlage eines Kunststoff-Katheters in gewissen Situationen unumgänglich sein. Die Indikation zur Einlage eines solchen Katheters in die Harnblase muss aber stets sorgfältig hinterfragt werden, da diese immer Risiken insbesondere infektiöser Natur in sich birgt. Der Artikel fasst Indikationen und praktische Aspekte zur Einlage eines transurethralen Dauerkatheters oder eines Zystostomiekatheters zusammen.
A healthy adult produces about 1-1.5 liters of urine per day depending on the amount of drinking water, which is stored in the urinary bladder and leaves the urinary tract spread over 2-6 bladder emptying per day. If the bladder emptying is impaired, the insertion of a plastic catheter may be unavoidable in certain situations. However, the indication for inserting such a catheter into the bladder must always be scrutinized carefully, as it always entails risks. Both long-term urinary diversion with a transurethral and a suprapubic catheter increases the risk of catheter-associated urinary tract infections, including urosepsis. Urinary tract infections are among the most common nosocomial infections and are catheter-associated in about 80% of cases. After a stay of 5-7 days, permanent catheters are colonized with bacteria and a biofilm is formed. After several weeks, virtually all permanent catheter carriers have catheter-associated bacteriuria (1-3). In order to minimize the development of catheter-associated urinary tract infections, the indication for catheter insertion must be carefully considered, the insertion of a catheter must be done under aseptic conditions and an already lying catheter must be changed at close-meshed intervals.
Furthermore, there are risks due to the insertion of the catheter itself. For example, the insertion of a transurethral indwelling catheter generally entails the risk of urethral injuries with formation of a via falsa and subsequent urethral strictures. Also, the insertion of a suprapubic catheter is associated with risks, this can lead to intra- or perivesical bleeding or by Fehlpunktionen to injuries of adjacent structures (intestines, vessels). Indications for the insertion of a permanent catheter are summarized in Table 1 (4).
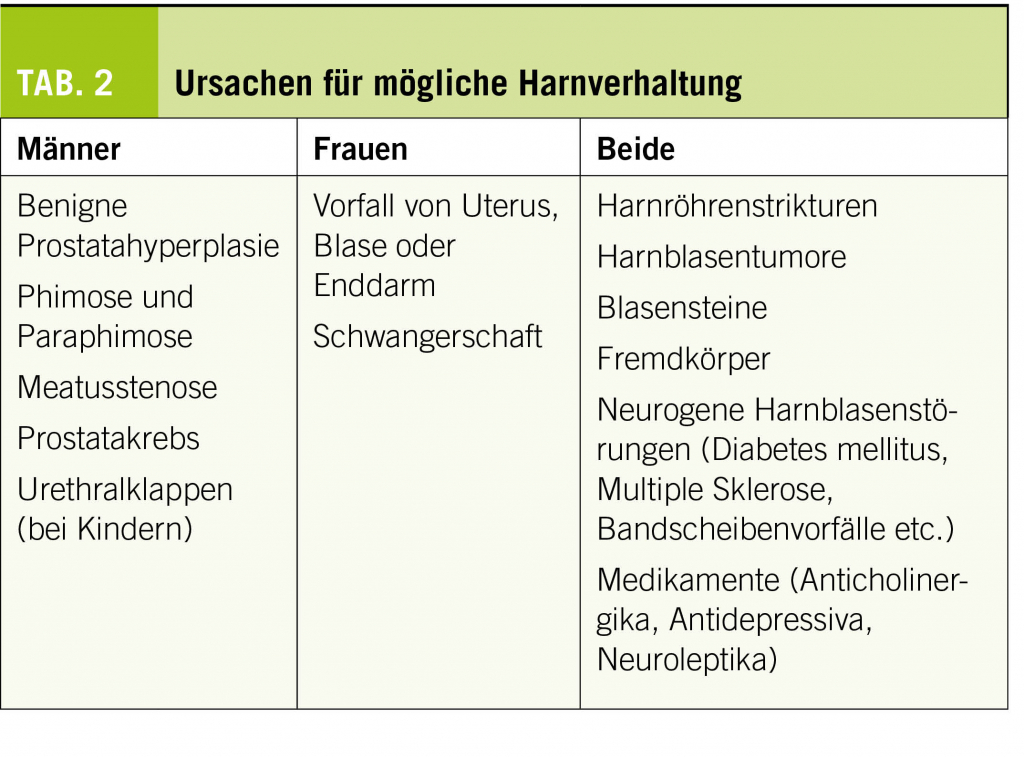
In primary care, the acute urinary retention is probably one of the most common reasons that leads to the insertion of a permanent catheter. The causes, which can lead to an acute urinary retention, are manifold. The most important are shown in Table 2 (adapted according to (5)):
The treatment of acute urinary retention is generally the immediate removal of urine by the insertion of a transurethral catheter or in pregnant women, the one-time catheter. Depending on the suspected cause, it should also be treated if possible. For example, in the case of known benign prostatic hyperplasia, it is possible to start with an alpha-blocker such as tamsulosin without previous drug therapy.
For the first time urinary retention, the indwelling catheter usually remains in the urinary bladder for a few days before an outlet attempt can be made. If the cause of the urinary retention is unclear, a clarification of the cause and a corresponding therapy of the underlying disease must be carried out.
Chronic retention bubble (overflow bladder)
Eine weitere Indikation im ambulanten Setting zur Einlage eines Dauerkatheters ist die chronische Retentionsblase. Im Gegensatz zur akuten Harnverhaltung entwickelt sich die chronische Retentionsblase über längere Zeit und wird von den Patienten selbst oftmals nicht bemerkt. Bei der chronischen Retentionsblase besteht die Unmöglichkeit, die Blase vollständig zu entleeren mit der Ausbildung von Restharn. Ab welchen Restharnmengen man von einer chronischen Retentionsblase mit möglichen nachfolgenden Komplikationen ausgehen kann, ist nicht einheitlich definiert. Die American Urological Association beschreibt eine chronische Retentionsblase als Restharnmengen von > 300 ml, welche in einem Zeitraum von 6 Monaten mindestens zweimal nachgewiesen werden müssen (6).
Eine chronische Retentionsblase entsteht am häufigsten bei obstruktiven oder neurogenen Blasenentleerungsstörungen. Zu einer obstruktiv bedingten chronischen Retentionsblase führt am häufigsten die benigne Prostatahyperplasie. Die neurogen bedingte chronische Retentionsblase kann im Rahmen des Diabetes mellitus, Rückenmarksverletzungen oder neurologischer Erkrankungen wie der Multiplen Sklerose auftreten. Die chronische Retentionsblase kann bis hin zur Überlaufblase führen, bei welcher der unwillkürliche Abgang von kleinen Portionen Urin auftritt. Unbehandelt kann sie je nach Ausmass zu schwerwiegenden Folgen führen, wie der Hydronephrose mit nachfolgendem Funktionsverlust der Nieren.
Wann immer möglich sollte versucht werden, die chronische Retentionsblase mittels intermittierendem (Selbst)Katheterismus zu behandeln. Sollte dies nicht möglich sein, sollte eine dauerhafte Harnableitung angestrebt werden.
Soll nun ein transurethraler Dauerkatheter oder ein suprapubischer Zystostomiekatheter gewählt werden?
Ist vorauszusehen, dass eine Harnableitung über mehrere Wochen bzw. gar dauerhaft notwendig wird, kann die Einlage eines suprapubischen Katheters evaluiert werden. Der suprapubische Katheter ist oftmals für den Patienten angenehmer zu tragen und grundsätzlich ist mit einem suprapubischen Katheter Geschlechtsverkehr möglich, was für manche Patienten ein entscheidender Faktor ist. Zudem ist der suprapubische Katheter im Vergleich zum transurethralen Katheter mit weniger Komplikationen im Bereich der Harnröhre (Strikturen etc.) vergesellschaftet. Hingegen ergibt sich durch die Einlage eines suprapubischen Katheters gemäss neuerer
Literatur keine geringere Inzidenz von Katheter-assoziierten Harnwegsinfekten (7, 8).
Ein suprapubischer Katheter ist auch dann indiziert, wenn ein transurethraler Katheter nicht eingelegt werden kann, z.B. bei unüberwindbaren Strikturen der Harnröhre oder traumatischen Verletzungen der Harnröhre.
Für die Einlage eines suprapubischen Katheters bestehen jedoch auch diverse absolute und relative Kontraindikationen.
Absolute Kontraindikationen:
- Ungenügend gefüllte oder sonographisch nicht oder ungenügend darstellbare Harnblase
- Harnblasentumoren oder Tumoren im kleinen Becken oder im Abdomen, welche die Harnblase verdrängen
- Gerinnungsstörungen
- Hauterkrankungen im Punktionsbereich
Relative Kontraindikationen:
- Voroperationen im Unterbauch
- Adipositas per magna
- Schwangerschaft
Der Entscheid, ob nun ein suprapubischer Katheter in Frage kommt, sollte vom individuellen Fall abhängig gemacht werden und der Patient sollte, wenn möglich, in die Entscheidung miteinbezogen werden. Grundsätzlich müssen die Vorteile, die sich durch die Einlage eines suprapubischen Katheters für den Patienten ergeben mit den möglichen potentiell lebensbedrohlichen Komplikationen, die bei dessen Einlage auftreten können (schwere Blutungen, Darmperforationen) abgewogen werden. Aus urologischer Sicht kann bei guter Verträglichkeit und Patientenakzeptanz eine dauerhafte Harnableitung durchaus auch durch einen transurethralen Katheter erfolgen.
Soll die Harnableitung mittels Beinbeutel oder Ventil erfolgen?
Ist die Notwendigkeit für die Einlage eines Dauerkatheters gegeben, so stellt sich die Frage, ob die Ableitung am Beinbeutel oder per Ventil erfolgen soll. Die Datenlage diesbezüglich ist spärlich. Gemäss der vorliegenden Literatur ist die Patientenzufriedenheit bei der Ableitung per Ventil grösser, obwohl es bei Patienten mit Ableitung per Ventil öfter zu nächtlichem Harndrang und parakathetralem Urinverlust kam. Bezüglich des Auftretens von Harnwegsinfekten ergab sich zwischen den beiden Methoden kein Unterschied (9). Die Ableitung per Ventil setzt jedoch natürlich voraus, dass der Patient in der Lage ist, dieses manuell zu bedienen und den Urin in regelmässigen Abständen abzulassen.
Ist ein regelmässiges Anspülen des Katheters zu empfehlen?
Eine weitere Frage, die sich im Rahmen der Harnableitung mittels Dauerkatheter häufig stellt, ist diejenige, ob der Katheter regelmässig angespült werden soll. Gemäss gängiger Literatur gibt es hierfür keine Evidenz (2, 4). Im Gegenteil kann das regelmässige Anspülen des Katheters sogar das Risiko für Harnwegsinfekte erhöhen, da zum einen bei jedem Dekonnektieren des Systems eine mögliche Eintrittspforte für Mikroorganismen entsteht und es zum anderen durch das Anspülen zu einer mechanischen Irritation der Blasenwand kommen kann, welche ebenfalls das Risiko für Infekte erhöht.
Zusammenfassend kann gesagt werden, dass eine Harnableitung durch einen transurethralen oder superpubischen Katheter nur nach sorgfältiger Indikationsstellung vorgenommen werden sollte. sollte die Notwendigkeit einer längerfristigen oder gar dauerhaften Harnableitung bestehen, so sollte der Katheter, unabhängig ob transurethral oder subpubisch, in regelmässigen 6-8-wöchentlichen Abständen gewechselt werden. Die Versorgung mittels Katheter sollte regelmässig reevaluiert und der Katheter so früh als möglich wieder entfernt werden. Zudem sollte immer auch evaluiert werden, ob in der vorliegenden Situation nicht ein intermittierender (Selbst)Katheterismus als Alternative in Frage kommt.
Urologische Klinik, UniversitätsSpital
Frauenklinikstrasse 10
8091 Zürich
olivia.maerzendorfer@usz.ch
Urologische Klinik, UniversitätsSpital
Frauenklinikstrasse 10
8091 Zürich
Die Autoren haben keine Interessenskonflikte in Zusammenhang mit diesem Beitragt.
Literatur:
1. Group KDIGOKCW. KDIGO 2012 clinical practice guideline for the evaluation and management of chronic kidney disease. Kidney International Suppl. 2013;3(1):150.
2. T W. Kreatin Supplementation und Nierenfunktion: Reines Kreatin ist nicht schädlich für die Nieren! Swiss medical forum. 2013;13(42):3.
3. Cockcroft DW, Gault MH. Prediction of creatinine clearance from serum creatinine. Nephron. 1976;16(1):31-41. Epub 1976/01/01.
4. Levey AS, Bosch JP, Lewis JB, Greene T, Rogers N, Roth D. A more accurate method to estimate glomerular filtration rate from serum creatinine: a new prediction equation. Modification of Diet in Renal Disease Study Group. Annals of internal medicine. 1999;130(6):461-70. Epub 1999/03/13.
5. K/DOQI clinical practice guidelines for chronic kidney disease: evaluation, classification, and stratification. American journal of kidney diseases : the official journal of the National Kidney Foundation. 2002;39(2 Suppl 1):S1-266. Epub 2002/03/21.
6. Inker LA, Schmid CH, Tighiouart H, Eckfeldt JH, Feldman HI, Greene T, et al. Estimating glomerular filtration rate from serum creatinine and cystatin C. The New England journal of medicine. 2012;367(1):20-9. Epub 2012/07/06.
7. Coresh J, Turin TC, Matsushita K, Sang Y, Ballew SH, Appel LJ, et al. Decline in estimated glomerular filtration rate and subsequent risk of end-stage renal disease and mortality. Jama. 2014;311(24):2518-31. Epub 2014/06/04.
8. Gansevoort RT, Matsushita K, van der Velde M, Astor BC, Woodward M, Levey AS, et al. Lower estimated GFR and higher albuminuria are associated with adverse kidney outcomes. A collaborative meta-analysis of general and high-risk population cohorts. Kidney international. 2011;80(1):93-104. Epub 2011/02/04.
9. Astor BC, Matsushita K, Gansevoort RT, van der Velde M, Woodward M, Levey AS, et al. Lower estimated glomerular filtration rate and higher albuminuria are associated with mortality and end-stage renal disease. A collaborative meta-analysis of kidney disease population cohorts. Kidney international. 2011;79(12):1331-40. Epub 2011/02/04.
10. Wetzels JF, Kiemeney LA, Swinkels DW, Willems HL, den Heijer M. Age- and gender-specific reference values of estimated GFR in Caucasians: the Nijmegen Biomedical Study. Kidney international. 2007;72(5):632-7. Epub 2007/06/15.
11. de Brito-Ashurst I, Varagunam M, Raftery MJ, Yaqoob MM. Bicarbonate supplementation slows progression of CKD and improves nutritional status. Journal of the American Society of Nephrology : JASN. 2009;20(9):2075-84. Epub 2009/07/18.
12. Phisitkul S, Khanna A, Simoni J, Broglio K, Sheather S, Rajab MH, et al. Amelioration of metabolic acidosis in patients with low GFR reduced kidney endothelin production and kidney injury, and better preserved GFR. Kidney international. 2010;77(7):617-23. Epub 2010/01/15.
13. Mahajan A, Simoni J, Sheather SJ, Broglio KR, Rajab MH, Wesson DE. Daily oral sodium bicarbonate preserves glomerular filtration rate by slowing its decline in early hypertensive nephropathy. Kidney international. 2010;78(3):303-9. Epub 2010/05/07.
14. KDIGO 2017 CLINICAL PRACTICE GUIDELINE UPDATE FOR THE DIAGNOSIS, EVALUATION, PREVENTION, AND TREATMENT OF CHRONIC KIDNEY DISEASE–MINERAL AND BONE DISORDER (CKD-MBD). Kidney International Suppl. 2017;7(1):60.
15. KDIGO Clinical Practice Guideline for Lipid Management in Chronic Kidney Disease. Kidney International Suppl. 2013;3(3):47.
16. KDIGO Clinical Practice Guideline for the Management of Blood Pressure in Chronic Kidney Disease Kidney International Suppl. 2012;2(5):77.
17th Wenceslas UO. Angiotensin-converting enzyme inhibitors and progression of renal disease: evidence from clinical studies. Contributions to nephrology. 2001 (135): 200-11. Epub 2001/11/14.
18. Wilhelm-Leen E, Montez-Rath ME, Chertow G. Estimating the Risk of Radiocontrast-Associated Nephropathy. Journal of the American Society of Nephrology: JASN. 2017; 28 (2): 653-9. Epub 2016/10/01.
19. Perazella MA. Current status of gadolinium toxicity in patients with kidney disease. Clinical journal of the American Society of Nephrology: CJASN. 2009; 4 (2): 461-9. Epub 2009/02/10.