Kardiovaskuläre Erkrankungen gehören zu den häufigsten Todesursachen weltweit (1,2). Zu den wichtigsten kardiovaskulären Risikofaktoren zählen arterielle Hypertonie, Rauchen, Diabetes mellitus und Hyperlipidämie (1,2). Durch die medikamentöse Therapie dieser kardiovaskulären Risikofaktoren kann die Entstehung (Primärprävention) und Progression von kardiovaskulären Erkrankungen (Sekundärprävention) positiv beeinflusst und die Morbidität und Sterblichkeit reduziert werden (3–5). Eine Vielzahl von physiologischen und pathophysiologischen Prozessen unterliegen tageszeitlichen Schwankungen. Dieses Phänomen wird als zirkadianer Rhythmus bezeichnet (6). Die Synthese der Lipoproteine, die Cholesterin transportieren und zur Entstehung von Atherosklerose beitragen, ist beispielsweise nachts und in den frühen Morgenstunden am ausgeprägtesten (7,8). Die Freisetzung des Stresshormons Cortisol aus den Nebennieren ist ebenfalls morgens am höchsten. Der arterielle Blutdruck hingegen fällt physiologischer Weise in der Nacht um durchschnittlich 10-20% ab (sogenanntes dipping) (9). Beobachtungen aus epidemiologischen Studien legen nahe, dass nächtliche Blutdruckspitzen (sogenanntes non-dipping) zu einer erhöhten Sterblichkeit beitragen (10–13). Ferner gibt es eine Häufung von Myokardinfarkten und plötzlichen Herztodereignissen in den frühen Morgenstunden (14,15). Vor diesem Hintergrund entstand die Hypothese, dass die Einnahme Blutdruck- und Cholesterin-senkender Medikamente an den zirkadianen Rhythmus angepasst und daher abends eingenommen werden sollten. Aktuelle Studien zeigen, dass Medikamente mit langen Halbwertszeiten unabhängig vom Einnahmezeitpunkt effektiv sind. Wichtig ist, dass der Einnahmezeitpunkte so gewählt wird, dass die Therapietreue maximal unterstützt wird. Im Folgenden werden wichtige Aspekte der Chronopharmakologie in der Kardiologie diskutiert.
Cardiovascular diseases remain the most common cause of death (1,2). Important cardiovascular risk factors include hypertension, smoking, diabetes mellitus, and dyslipidemia (1,2). Treating these risk factors has been shown to delay the progression of cardiovascular diseases thereby improving morbidity and mortality (3–5). Physiologic processes in the human body commonly follow a circadian rhythm (6). Cholesterol synthesis in the liver for example peaks at night (7,8), cortisol synthesis in the adrenal gland is highest in the early morning, and blood pressure physiologically decreases during sleep by 10-20% (i.e. dipping) (9). Epidemiologic studies have shown that high nighttime blood pressure (i.e. non-dipping) associates with increased cardiovascular mortality (10–13). Moreover, the incidence of myocardial infarction is highest in the early morning, as is the occurrence of sudden cardiac death (14,15). Consequently, is has been hypothesized that it might be beneficial to adjust the intake of cardiovascular medication, i.e. antihypertensive and lipid-lowering therapy, to the circadian rhythm. Recent studies, however, have shown that drugs with long half-lives are effective independent of the timing of administration. Therefore, antihypertensive, and lipid-lowering drugs should be taken at time points, which associate with the highest rates of adherence and persistence to medication. Herein, we discuss the evidence surrounding chronotherapy of cardiovascular drugs.
Key Words: Adherence, hypertension, prevention, statins, chronotherapy
Antihypertensiva
Der arterielle Blutdruck unterliegt tageszeitlichen Schwankungen. Physiologischerweise fallen der systolische und diastolische Blutdruck im Schlaf um etwa 10-20% ab (16,17). Das Fehlen einer physiologischen Tag-Nacht-Absenkung des Blutdrucks ist mit einem erhöhten Risiko kardiovaskulärer Endorganschäden assoziiert (9–11, 18–20). Die JAMP-Studie (Japan Ambulatory Blood Pressure Monitoring Prospective), an der insgesamt 6.359 Patienten im medianen Alter von 68 Jahren teilnahmen, bei denen wenigstens ein kardiometabolischer Risikofaktor vorlag, untersuchte die prognostische Bedeutung des nächtlichen Blutdrucks und des Blutdruckprofils (21). Ein Anstieg des systolischen Blutdrucks um 20 mmHg war mit einem Anstieg von atherosklerotischen kardiovaskulären Ereignissen um 18 % verbunden. Das Risiko für eine chronische Herzinsuffizienz lag mit 25 % sogar darüber. Die schlechteste Prognose wiesen die sogenannten „riser“ auf, bei denen die nächtlichen Blutdruckwerte die Tageswerte überschritten. Die Hazard Ratio für kardiovaskuläre Erkrankungen lag bei 1,48 und bei 2,45 für das Auftreten einer chronischen Herzinsuffizienz (21).
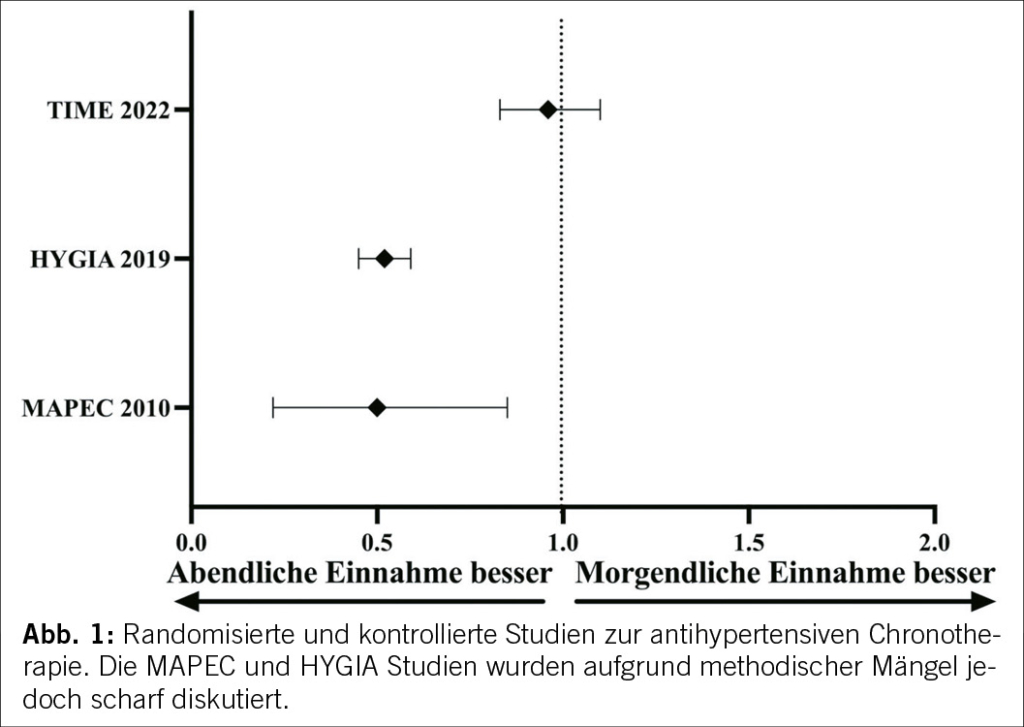
Vor diesem Hintergrund wurde untersucht, ob die abendliche Einnahme von Antihypertensiva zur Senkung der kardiovaskulären Morbidität und Sterblichkeit beitragen kann. Die MAPEC-Studie (Ambulatory Blood Pressure Monitoring for Prediction of Cardiovascular Events) war die erste prospektive, randomisierte Studie, die die abendliche Einnahme mit der morgendlichen Einnahme von Antihypertensiva verglich. Insgesamt 2.156 Patienten mit arterieller Hypertonie und vorbestehender blutdrucksenkender Therapie wurden randomisiert. Langzeitblutdruckmessungen über 48 Stunden wurden durchgeführt und primärer Endpunkt war das Auftreten kardiovaskulärer Ereignisse. Nach einem medianen Follow-Up von 5,2 Jahren traten in der Gruppe, die ihre antihypertensive Medikation abends einnehmen sollte, signifikant weniger kardiovaskuläre Ereignisse (-61%, p<0,001) und grosse Ereignisse (definiert als kardiovaskulärer Tod, nicht-tödlicher Schlaganfall und nicht-tödlicher Herzinfarkt; -67%; p<0,001) auf. Mechanistisch wurde dies mutmasslich durch eine bessere Blutdruckkontrolle erreicht. Die Gruppe mit abendlicher Medikationseinnahme hatte einen signifikant niedrigeren systolischen Blutdruck während des Schlafes (nächtlicher systolischer Blutdruck über 48 Stunden 110,9 mmHg vs. 116,1 mmHg; p<0.001) einen stärkeren Abfall des Blutdrucks beim Schlafen (11,4% vs. 7,0%), weniger non-Dipper (34% versus 62%; p<0,001), und eine höhere Rate an kontrollierten Langzeitblutdrucken (62% versus 53%; p<0,001) (22).
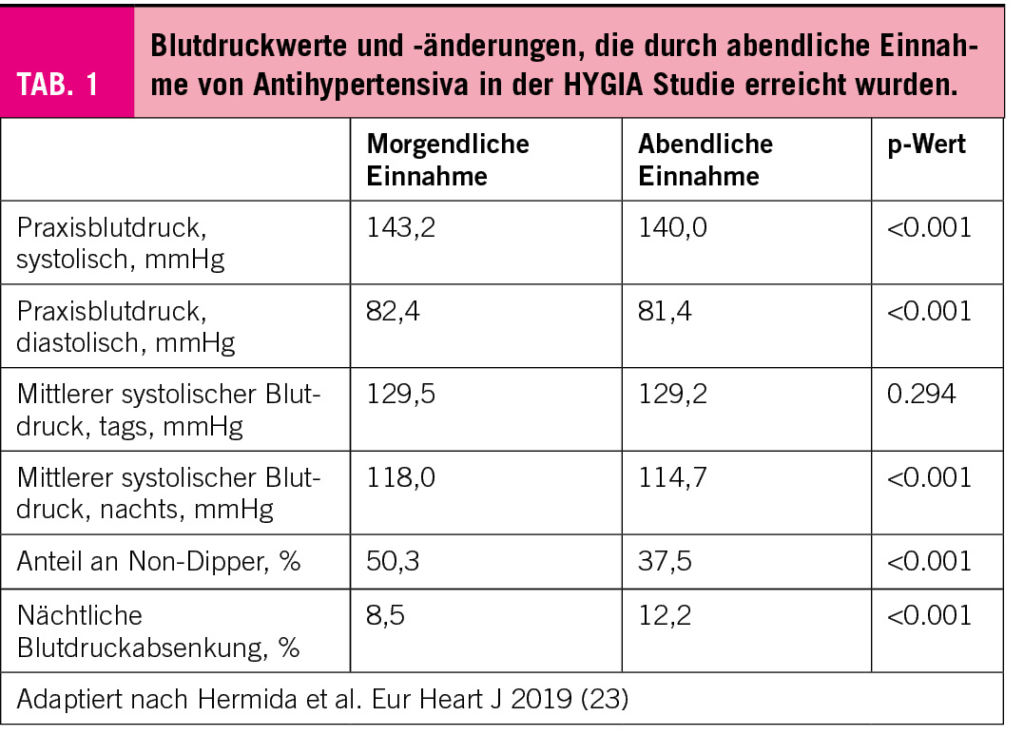
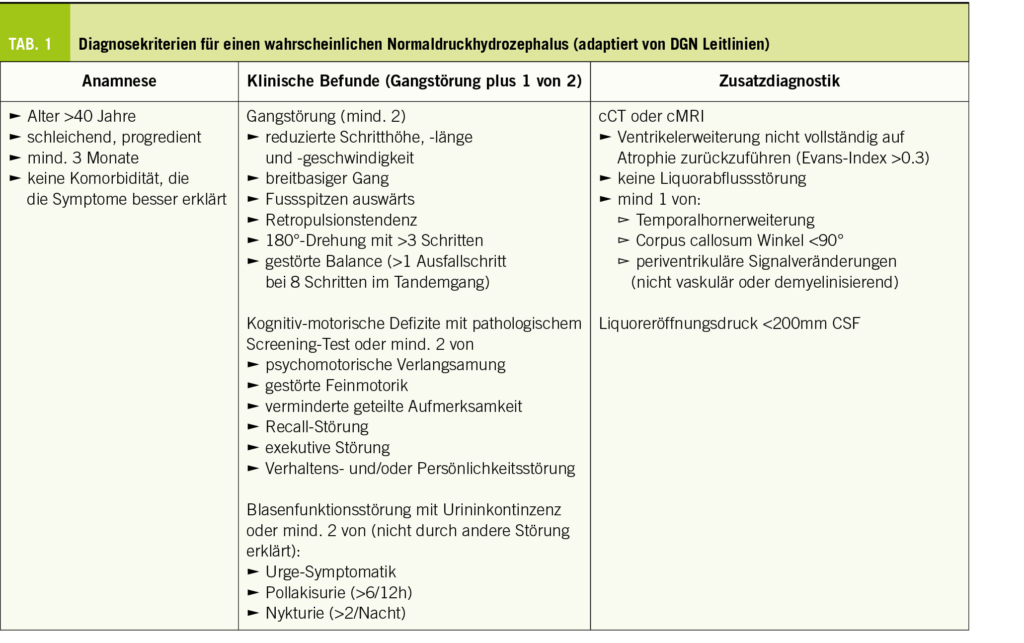
Ähnliche Ergebnisse erbrachte die HYGIA Studie, eine multizentrische, randomisierte, kontrollierte Studie, die 19.084 Patienten mit arterieller Hypertonie randomisierte ihre antihypertensive Therapie entweder morgens oder abends einzunehmen. Auch in dieser Studie wurden 48-Stunden-Langzeitblutdruckmessungen durchgeführt. Nach einem medianen Follow-Up von 6,3 Jahren kam es zu signifikant weniger kardiovaskulären Ereignissen in der Gruppe, die ihre Antihypertensiva abends einnahmen, verglichen mit den Patienten, die alle Medikamente morgens einnahmen (-45%; p<0,001). Interessanterweise wurden alle Einzelkomponenten des Endpunktes (Herzinfarkt, koronare Revaskularisation, neu diagnostizierte Herzinsuffizienz, Schlaganfall) in der Gruppe durch die abendliche Medikamenteneinnahme reduziert. Auch diese enorme Reduktion an klinischen Endpunkten wurde durch eine bessere Blutdruckkontrolle in der Nacht und eine geringe Rate an Non-Dippern erklärt (Tabelle 1) (23). Die MAPEC und HYGIA Studien warfen jedoch einige Fragen und methodologische Limitationen auf, die eine Übertragbarkeit der Ergebnisse in den klinischen Alltag in Frage stellen. Es war unklar, warum, trotz der enormen Risikoreduktion, die Studien nicht frühzeitig beendet wurden und warum 48 Stunden Langzeitblutdruckmessungen angewendet wurden, die nicht von Leitlinien empfohlen werden. Weitere Limitationen der HYGIA-Studie ist das PROBE (prospektiv, randomisiert, offen, verblindeter Endpunkt)-Design, die unterschiedliche medikamentöse Therapie und der nur minimale Unterschied in der Blutdrucksenkung zwischen den Gruppen. Letzteres war zu klein, um die Endpunktreduktion zu erklären. Ferner konnten andere Studien keine Überlegenheit einer Chronotherapie nachweisen (z. B. AASK-Studie).
Die TIME (Treatment in Morning versus Evening) Studie, die im Jahr 2022 veröffentlicht wurde, randomisierte 21.104 Patenten mit arterieller Hypertonie ihre vorbestehende antihypertensive Medikation entweder morgens (zwischen 6:00 und 10:00 Uhr) oder abends (zwischen 20:00 und 00:00 Uhr) einzunehmen. Als primärer Endpunkt wurde ein kombinierter Endpunkt, definiert als vaskulärer Tod oder Krankenhausaufnahme als Folge eines nichttödlichen Herzinfarkts oder Schlaganfalls, untersucht. Nach einer medianen Nachbeobachtung von 5,2 Jahren zeigten sich keine Unterschiede zwischen den beiden Gruppen hinsichtlich des Auftretens des primären Endpunktes. Interessanterweise waren die Patienten in der abendlichen Einnahmegruppe weniger adhärent als die Patienten in der morgendlichen Einnahmegruppe (39,0% versus 22,5%; p<0,0001). Die TIME-Studie war eine pragmatische Studie, bei der Blutdruckwerte von den Teilnehmern selbst berichtet und dadurch nicht von allen Teilnehmern erhoben wurden. Zudem unterschieden sich die antihypertensiven Therapien der Teilnehmer, denn die vorbestehende Therapie wurde weiterhin eingenommen. Diese Ergebnisse widersprechen den erhobenen Ergebnissen der HYGIA und MAPEC Studien.
Rezent wurde die Evidenz zur Chronopharmakotherapie von Antihypertensiva in einer Metaanalyse von 72 randomisierten und kontrollierten Studien zusammengefasst. Es zeigte sich, dass die abendliche Einnahme von Antihypertensiva mit einer signifikanten Senkung des 24 Stunden ambulanten systolischen Blutdrucks und des abendlichen systolischen Blutdrucks einherging, wesentlich getrieben jedoch durch die kontroversen Studien HYGIA und MAPEC. Zu einer signifikanten Reduktion von wichtigen klinischen Endpunkten trug eine abendliche Einnahme laut dieser Metaanalyse jedoch nicht bei (24).
Lipidsenkende Therapie
Die Senkung des LDL-C und der ApoB-Partikel durch Lebensstilmodifikationen und Pharmakotherapie ist eine der wichtigsten Strategien in der Primär- und Sekundärprävention von kardiovaskulären Erkrankungen. Pharmakotherapeutisch kommen vor allem Statine zum Einsatz, die durch Inhibition der beta-3-Hydroxy-3-Methylglutaryl-Coenzym-A-Reduktase (HMG-CoA-Reduktase) die Cholesterinbiosynthese reduzieren und dadurch das LDL-C effektiv senken (25). LDL-C wird vor allem nachts synthetisiert, sodass hypothetisiert wurde, dass die abendliche Gabe von Statinen zu einer effektiveren Senkung des LDL-C führt als eine morgendliche oder mittägliche Einnahme (7,8). Eine Cochrane Meta-Analyse von 8 randomisierten und kontrollierten Studien mit 767 Patienten untersuchte diese Hypothese. Durch die abendliche Einnahme von Statinen kam es nicht zu einer stärkeren Senkung des LDL-C oder des Gesamtcholesterins, jedoch weisen die Autoren auf das hohe Risiko für einen Bias in 4 der 8 untersuchten Studien hin. Die unerwünschten Arzneimittelwirkungen unterschieden sich nicht wesentlich. Eine Analyse von wichtigen klinischen Endpunkten wurde nicht durchgeführt (26).
Eine Metaanalyse, die im Jahr 2023 veröffentlicht wurde und 15 Studien mit insgesamt 1.352 Patienten einschloss zeigte, dass nur Statine mit kurzer Plasmahalbwertszeit statistisch signifikant stärker die LDL-C- und Triglyceridkonzentration senken, wenn sie abends verabreicht werden. Werden hingegen Statine mit langer Plasmahalbwertszeit verabreicht gibt es keine Unterschiede zwischen einer morgendlichen und einer abendlichen Einnahme hinsichtlich der Reduktion der Serumspiegel von LDL-C und Triglyceriden (27). Vor allem die synthetischen Statine Atorvastatin und Rosuvastatin zeichnen sich durch eine lange Plasmahalbwertszeit aus und sollten daher bevorzugt eingesetzt werden (Tabelle 2) (28). Zum gegenwärtigen Zeitpunkt gibt es keine Hinweise, dass eine abendliche Einnahme von cholesterinsenkenden Medikamenten das Überleben oder Auftreten von kardiovaskulären Ereignissen verbessert.
Copyright Aerzteverlag medinfo AG
Dr. med. Felix Götzinger, felix.goetzinger@uks.eu
Dr. med. Michael Kunz
Dr. med. Lucas Lauder
Dr. med. Saaraakeen Kulenthiran
Prof. Dr. med. Felix Mahfoud
Klinik für Innere Medizin III
Kardiologie, Angiologie und Internistische Intensivmedizin
Universitätsklinik Homburg, Universität des Saarlandes
IMED, Geb. 41, Kirrbergerstrasse 100, 66424 Homburg, Deutschland
Tel. +4968411615911
Universitäres Herzzentrum Basel
Universitätsspital Basel
Am Petersgraben 4, 4031 Basel
Klinik für Kardiologie und
Cardiovascular Research Institute Basel (CRIB)
Universitätsspital Basel
Petersgraben 4
4031 Basel
Universitäres Herzzentrum Basel
Universitätsspital Basel
Am Petersgraben 4, 4031 Basel
F.G. hat Vortragshonorare von AstraZeneca erhalten und wird durch die Deutsche Herzstiftung gefördert. M.K gibt keine Interessenskonflikte an. L.L. hat Vortragshonorare von AstraZeneca, ReCor Medical und Medtronic erhalten. S.K. gibt keine Interessenskonflikte an. F.M wird durch die Deutsche Herzstiftung, Deutsche Gesellschaft für Kardiologie und die Deutsche Forschungsgemeinschaft unterstützt (DFG, SFB TRR 219, Projekt ID-322900939) und hat wissenschaftliche Unterstützung oder Vertragshonorare von Bayer, Boehringer Ingelheim, Inari, Medtronic, Merck, und ReCor Medical erhalten.
1. Magnussen C, Ojeda FM, Leong DP, et al. Global effect of modifiable risk factors on cardiovascular disease and mortality. N Engl J Med 2023;389(14):1273–85.
2. Joseph P, Leong D, McKee M, et al. Reducing the global burden of cardiovascular disease, part 1. Circ Res 2017;121(6):677–94.
3. Visseren FLJ, Mach F, Smulders YM, et al. 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice. Eur Heart J 2021;42(34):3227–337.
4. Mach F, Baigent C, Catapano AL, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J 2020;41(1):111–88.
5. Mancia G, Kreutz R, Brunström M, et al. 2023 ESH Guidelines for the management of arterial hypertension The Task Force for the management of arterial hypertension of the European Society of Hypertension Endorsed by the European Renal Association (ERA) and the International Society of Hypertension (ISH). J Hypertens 2023;
6. Crnko S, Du Pré BC, Sluijter JPG, Van Laake LW. Circadian rhythms and the molecular clock in cardiovascular biology and disease. Nat Rev Cardiol 2019;16(7):437–47.
7. Jones PJ, Schoeller DA. Evidence for diurnal periodicity in human cholesterol synthesis. J Lipid Res 1990;31(4):667–73.
8. Schroor, Sennels, Fahrenkrug, Jørgensen, Plat, Mensink. Diurnal variation of markers for cholesterol synthesis, cholesterol absorption, and bile acid synthesis: A systematic review and the Bispebjerg study of diurnal variations. Nutrients 2019;11(7):1439.
9. Fagard RH, Thijs L, Staessen JA, Clement DL, De Buyzere ML, De Bacquer DA. Night–day blood pressure ratio and dipping pattern as predictors of death and cardiovascular events in hypertension. J Hum Hypertens 2009;23(10):645–53.
10. Boggia J, Li Y, Thijs L, et al. Prognostic accuracy of day versus night ambulatory blood pressure: a cohort study. Lancet 2007;370(9594):1219–29.
11. Fagard RH, Celis H, Thijs L, et al. Daytime and nighttime blood pressure as predictors of death and cause-specific cardiovascular events in hypertension. Hypertension 2008;51(1):55–61.
12. Yang W-Y, Melgarejo JD, Thijs L, et al. Association of office and ambulatory blood pressure with mortality and cardiovascular outcomes. JAMA 2019;322(5):409.
13. Staplin N, de la Sierra A, Ruilope LM, et al. Relationship between clinic and ambulatory blood pressure and mortality: an observational cohort study in 59 124 patients. Lancet 2023;401(10393):2041–50.
14. Muller JE, Stone PH, Turi ZG, et al. Circadian variation in the frequency of onset of acute myocardial infarction. N Eng J Med 1985;313(21):1315–22.
15. Muller JE, Ludmer PL, Willich SN, et al. Circadian variation in the frequency of sudden cardiac death. Circulation 1987;75(1):131–8.
16. Stergiou GS, Palatini P, Parati G, et al. 2021 European Society of Hypertension practice guidelines for office and out-of-office blood pressure measurement. J Hypertens 2021;39(7):1293–302.
17. O’Brien E, Sheridan J, O’Malley K. Dippers and non-dippers. Lancet 1988;332(8607):397.
18. Kario K, Hoshide S, Mizuno H, et al. Nighttime hemodynamic phenotype. A novel risk factor for cardiovascular disease, especially heart failure: the practitioner-based nationwide JAMP study. Clin Res Cardiol 2023;112(1):98–110.
19. Salles GF, Reboldi G, Fagard RH, et al. Prognostic effect of the nocturnal blood pressure fall in hypertensive patients. Hypertension 2016;67(4):693–700.
20. Yang W-Y, Melgarejo JD, Thijs L, et al. Association of office and ambulatory blood pressure with mortality and cardiovascular outcomes. JAMA 2019;322(5):409.
21. Kario K, Hoshide S, Mizuno H, et al. Nighttime blood pressure phenotype and cardiovascular prognosis. Circulation 2020;142(19):1810–20.
22. Hermida RC, Ayala DE, Mojón A, Fernández JR. Influence of circadian time of hypertension treatment on cardiovascular risk: results of the MAPEC study. Chronobiol Int 2010;27(8):1629–51.
23. Hermida RC, Crespo JJ, Domínguez-Sardiña M, et al. Bedtime hypertension treatment improves cardiovascular risk reduction: the Hygia Chronotherapy Trial. Eur Heart J 2020;41(48):4565–76.
24. Maqsood MH, Messerli FH, Skolnick AH, Newman JD, Berger JS, Bangalore S. Timing of antihypertensive drug therapy: a systematic review and meta-analysis of randomized clinical trials. Hypertension 2023;80(7):1544–54.
25. Taylor FC, Huffman M, Ebrahim S. Statin therapy for primary prevention of cardiovascular disease. JAMA 2013;310(22):2451.
26. Izquierdo-Palomares JM, Fernandez-Tabera JM, Plana MN, et al. Chronotherapy versus conventional statins therapy for the treatment of hyperlipidaemia. Cochrane Database Syst Rev 2016;2016(11).
27. Wang C, Quan Y, Wang L, Li G. Effect of timing of administration on lipid-lowering efficacy of statins-meta-analysis. Eur J Clin Pharmacol 2023;
28. Laufs U, Weingärtner O, Kassner U, Schatz U. State of the art: Therapie mit Statinen. Dtsch Med Wochenschr 2022;147(01/02):62–8.