Migräne ist nicht nur der häufigste primäre Kopfschmerz, sondern eine der häufigsten neurologischen Erkrankungen überhaupt – und sie betrifft Frauen häufiger als Männer. In diesem Artikel fassen wir Daten über den Verlauf der Migräne in der Schwangerschaft sowie die Therapieoptionen zusammen. Darüber hinaus stellen wir die wichtigsten Differentialdiagnosen von Kopfschmerzen bei Schwangeren vor und wie primäre/ungefährliche Kopfschmerzen in der Akutphase von sekundären/potentiell gefährlichen Kopfschmerzen unterschieden werden können.
Migraine is not only the most common primary headache disorder, but also one of the most common neurological diseases in general, affecting women more frequently than men. In this article, we summarize data on the course of migraine in pregnancy as well as available treatment options, especially regarding the acute treatment of attacks. Furthermore, we discuss the differential diagnosis of headache in pregnant women, especially focusing on the distinction between primary/non-dangerous vs. secondary/potentially dangerous headaches
Key Words: Migräneprophylaxe, Migräne-Akuttherapie, primäre Kopfschmerzen, sekundäre Kopfschmerzen, «Red Flags»
Migräne und Schwangerschaft
Verlauf der Migräne in der Schwangerschaft
Migräne ist nicht nur der häufigste primäre Kopfschmerz, sondern eine der häufigsten neurologischen Erkrankungen überhaupt (1) – mit grossem Einfluss auf die Lebensqualität sowie wesentlichen sozioökomischen Konsequenzen, z.B. durch häufiges Fehlen am Arbeitsplatz (2). Migräne betrifft Frauen ca. dreimal häufiger als Männer (3) und ist oft mit gynäkologischen «Komorbiditäten» (wie z.B. Dysmenorrhoe, Endometriose etc.) assoziiert (4). Somit ist sie für den klinischen Alltag von GynäkologInnen sehr relevant.
Die diagnostischen Kriterien für Migräne ohne und mit Aura nach ICHD-3 sind in Tabelle 1 zusammengefasst. Da Migräne-Attacken nicht immer unilateral sind, ist der klinischen Erfahrung nach für die Diagnosestellung und die Abgrenzung z.B. von Spannungskopfschmerzen vor allem der hohe Leidensdruck der Betroffenen entscheidend. Hierzu zählt, dass Migräneattacken typischerweise mit mittlerer bis starker Schmerzintensität, Rückzugstendenz und Begleitsymptomen einhergehen und sich die Schmerzen bei körperlicher Aktivität verstärken (Tab. 1).
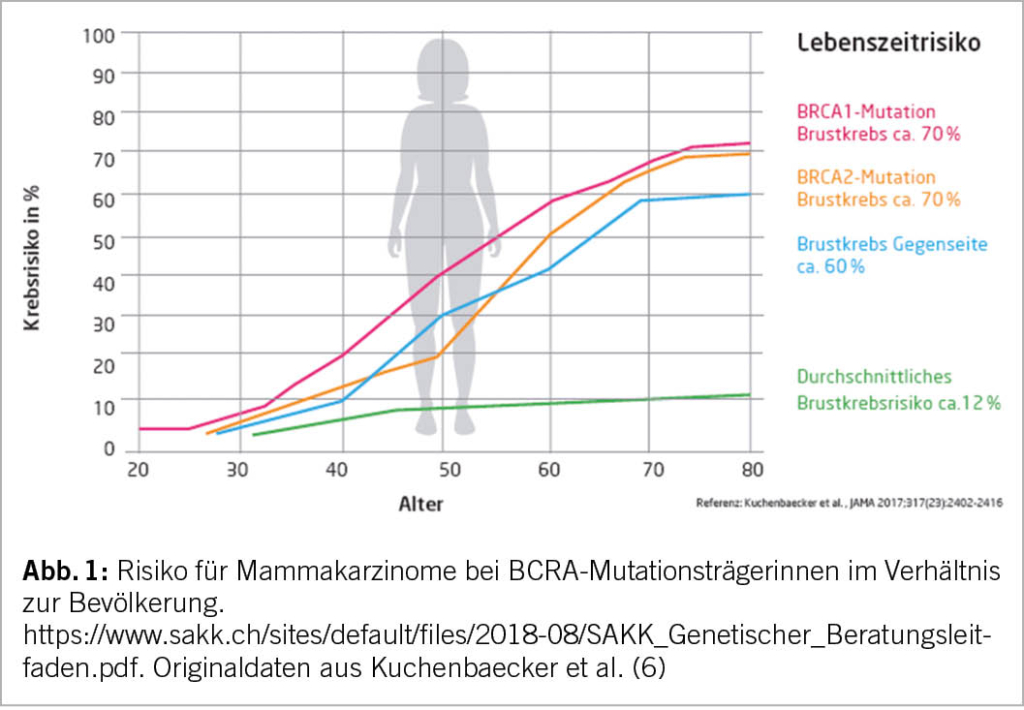
Der Verlauf der Migräne in der Schwangerschaft kann sehr variabel sein, jedoch tritt bei den meisten Migränepatientinnen während der Schwangerschaft eine spontane Besserung der Kopfschmerzen auf. Bei Migräne ohne Aura erleben über 80% der Frauen bis zum Ende des zweiten Trimenons eine Besserung der Kopfschmerzen, wobei am Ende das ersten Trimenons der Anteil der Frauen mit Besserung geringer ist (ca. 50%) (4, 5). Im ersten Trimenon kann es allerdings auch zu einer Verschlechterung der Migräne kommen, z.B. durch die plötzlichen hormonellen Veränderungen, Reduktion des Kaffee-Genusses sowie die reduzierte Einnahme von Akutmedikation (aufgrund von schwangerschaftsbedingter Übelkeit/Erbrechen und/oder aus Angst vor Nebenwirkungen für das Kind). Interessanterweise ist die Wahrscheinlichkeit für eine Besserung einer Migräne mit Aura während der Schwangerschaft insgesamt geringer, wobei eine Aurasymptomatik auch erstmalig in der Schwangerschaft auftreten kann, wahrscheinlich Östrogen-bedingt (6).
Akuttherapie der Migräne in der Schwangerschaft
Die Akuttherapie der Migräneattacken bei schwangeren Patientinnen hat natürlich Besonderheiten, nicht nur, weil einige Medikamente (relativ) kontraindiziert sind, sondern auch, weil die Frauen selbst gegenüber Medikamenten oft sehr zurückhaltend sind. Aus diesem Grund sind nicht-medikamentöse «Tricks» oft sehr hilfreich: die Kühlung der Kopfhaut und das Einreiben von Pfefferminzöl, das Vermeiden der so genannten «Triggerfaktoren» (z.B. bestimmte Gerüche, Überarbeitung/Stress etc.), der rechtzeitige Rückzug bereits bei leichten Kopfschmerzen bzw. bei Auftreten der Aura, Entspannungsübungen und ausreichend Schlaf. Darüber hinaus können TENS-Geräte (z.B. zur Stimulation der Nn. supraorbitalis) in der Schwangerschaft als Akuttherapie von Attacken (sowie prophylaktisch) hilfreich sein (4). Bei stärkeren oder lange anhaltenden Migräneattacken kann auch auf subkutane Occipitalisinfiltrationen (mit Steroiden sowie ggf. niedrig-dosiertem Lidocain) zurückgegriffen werden.
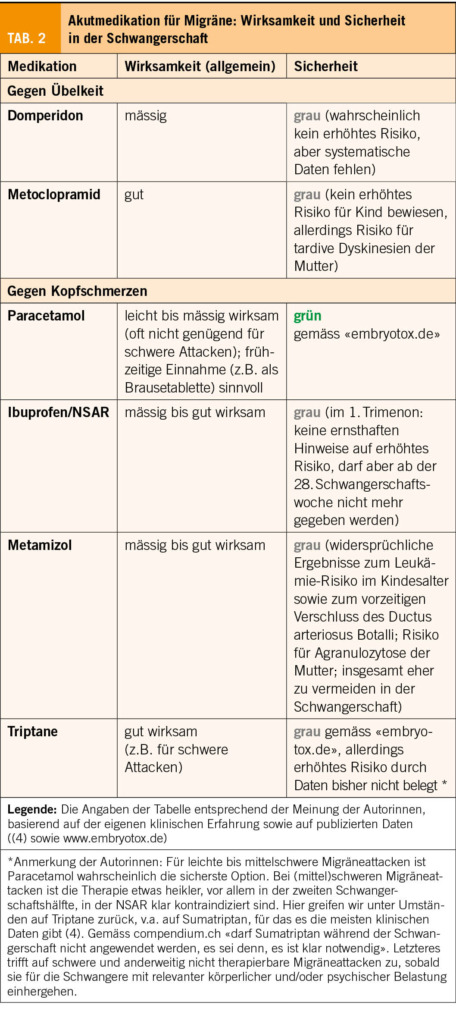
Tabelle 2 zeigt die herkömmlichen Akutmedikamente, die in einer Migräneattacke eingesetzt werden, ihre allgemeine Wirksamkeit sowie ihr Sicherheitsprofil in der Schwangerschaft. Zusammengefasst ist bei leichten und mittleren Migräneattacken Paracetamol in der Schwangerschaft, aufgrund des guten Sicherheitsprofils, das Mittel der ersten Wahl. Bei schweren Migräneattacken kann auch auf Triptane zurückgegriffen werden. Wir nutzen meistens Sumatriptan (als Nasenspray oder Tablette), für das es die meisten Daten bei Schwangeren gibt (4, 7, www.embryotox.de) (Tab. 2).
Prophylaxe der Migräne in der Schwangerschaft
Die Möglichkeiten für eine Migräneprophylaxe sollten bereits vor einer Schwangerschaft mit den behandelnden NeurologInnen besprochen werden. Dies gilt besonders für Migränepatientinnen im gebärfähigen Alter mit häufigen und/oder schweren Migräneattacken. In einem ersten Schritt kommen nicht-medikamentöse Prophylaxemassnahmen zum Einsatz, wie zum Beispiel das Achten auf ausreichend Schlaf, einen regelmässigen Schlaf-Wach-Rhythmus, Stressregulation und die Vermeidung von Triggerfaktoren. Darüber hinaus können Entspannungsübungen, Yoga, Akupunktur, Massage/Physiotherapie, Meditation sowie regelmässiger Ausdauersport wirksam sein (8).
Wenn diese Massnahmen ausgereizt sind, können auch bei Schwangeren bzw. Frauen mit Kinderwunsch zusätzlich medikamentöse Prophylaxemassnahmen in Betracht gezogen werden, die Auswahl an geeigneten Präparaten ist in der Schwangerschaft allerdings erheblich kleiner. Magnesium ist hier aufgrund seines Sicherheitsprofils (9) sowie der günstigen gynäkologischen «Nebeneffekte» (z.B. gegen Muskelkrämpfe und Kontrakturen) eine sehr gute Option. Die nachweislich wirksame Dosis zur Migräneprophylaxe beträgt 600 mg/Tag (am besten in 2 Dosen) (10). Bei störendem Durchfall kann die Dosis reduziert werden. Auch Beta-Blocker (Propranolol, Metoprolol) sind eine sichere – und wahrscheinlich im Vergleich zu Magnesium wirksamere – prophylaktische Option in der Schwangerschaft (4) und insbesondere eine gute Wahl bei Patientinnen mit arterieller Hypertonie/erhöhtem Risiko für (Prä-)Eklampsie. Andere Migräneprophylaktika sind in der Schwangerschaft entweder kontraindiziert (Topiramat und Valproat aufgrund der Teratogenität) oder dürfen nur unter strenger Nutzen-Risiko-Abwägung angewendet werden (z.B. Amitriptylin, Flunarizin). Über die Sicherheit von CGRP-Antikörpern in der Schwangerschaft gibt es bislang zu wenige Daten. Diese neueren Migräneprophylaktika sollten daher bereits drei bis fünf Monate vor Eintritt der Schwangerschaft pausiert werden (4).
Insgesamt ist die Migräneprophylaxe ein deutlich komplexeres Feld als die Akuttherapie. Schwangere mit häufiger/belastender Migräne sollten daher niedrigschwellig neurologisch mitbeurteilt und beraten werden – auch zur diagnostischen Evaluation und zum Ausschluss einer gefährlichen Kopfschmerzursache.
Sekundäre Kopfschmerzen in der Schwangerschaft
«Red Flags»
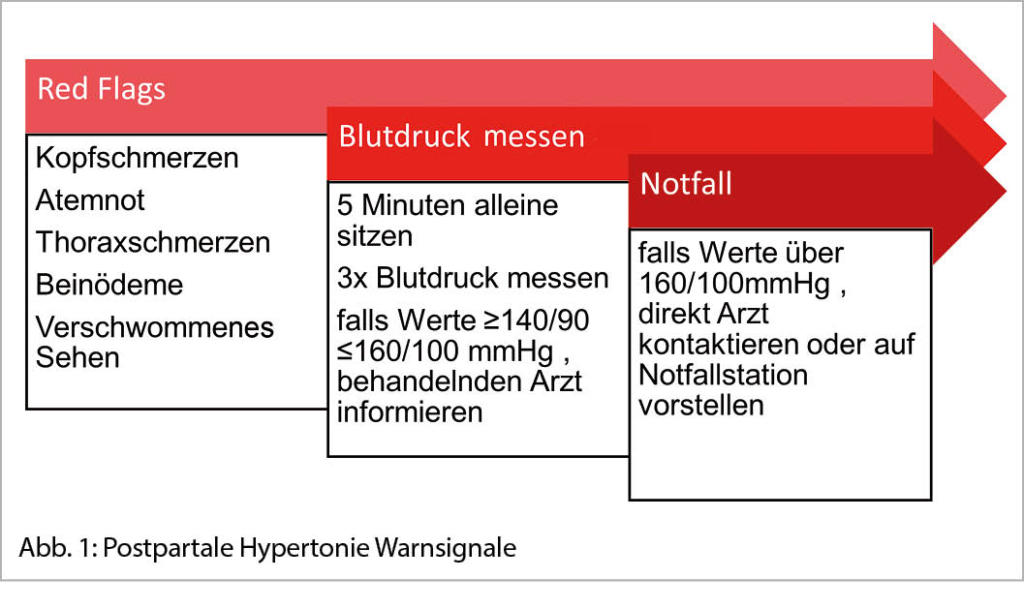
Sekundäre Kopfschmerzen sind insgesamt viel seltener als Migräne oder andere primäre Kopfschmerzen. Da sie jedoch potentiell gefährlich sind, ist eine gründliche Kopfschmerzanamnese besonders wichtig, um diese Kopfschmerzursachen – z.B. eine hypertensive Schwangerschaftserkrankung, eine intrakranielle Hypertension oder eine cerebrale Venenthrombose – nicht zu verpassen (11).
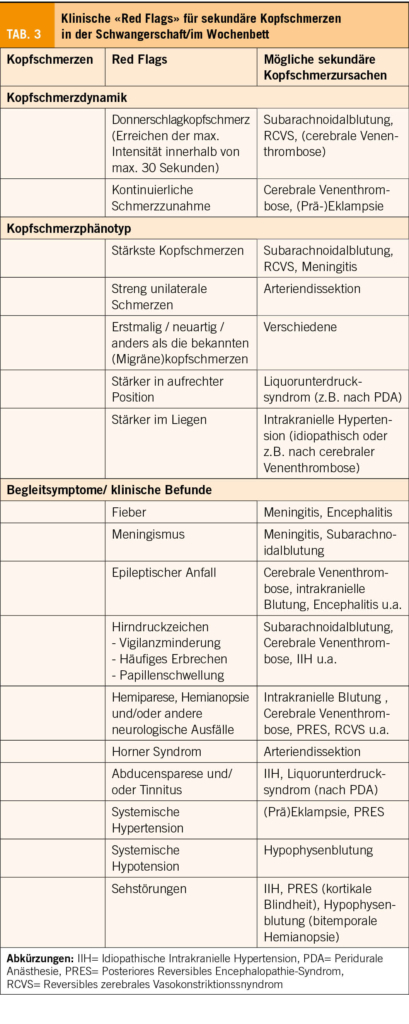
Die wichtigsten klinischen «Red Flags» für sekundäre Kopfschmerzen in der Schwangerschaft/im Wochenbett sind in Tabelle 3 zusammengefasst. Sobald ein solches Warnsymptom vorliegt, sollte eine umgehende neurologische Mitbeurteilung veranlasst werden. Häufig – vor allem bei akutem Kopfschmerzbeginn und neuen neurologischen Symptomen – ist eine sofortige cerebrale MR-Bildgebung (Magnetresonanztomographie) angezeigt. Wenn zusätzlich Infektzeichen bestehen, kann auch eine notfallmässige Lumbalpunktion indiziert sein (Tab. 3). Als Akronym für Warnzeichen bei Kopfschmerzen in der Schwangerschaft wird in der Literatur auch «PREGNANT» benutzt (P=proteinuria, R=rapid onset, E=elevated blood pressure (or temperature), G=gestational age in 3rd trimester, N=neurological signs/symptoms, A= altered level of consciousness, N=no known headache history, T=thrombocytopenia or thrombocytosis) (12).
Beispiele von sekundären Kopfschmerzen in der Schwangerschaft und im Wochenbett
Einige der sekundären Kopfschmerzen treten in der Schwangerschaft und/oder im Wochenbett häufiger auf als in der gleichaltrigen Gesamtbevölkerung. Mit diesen sollten GynäkologInnen daher besonders gut vertraut sein. Wir stellen fünf sekundäre Kopfschmerzen im Folgenden etwas genauer vor:
Hypertensive Schwangerschafterkrankungen und PRES
Über 50% der sekundären Kopfschmerzen bei Schwangeren sind auf eine hypertensive Schwangerschaftserkrankung zurückzuführen (13). Die Präeklampsie ist die häufigste dieser Gestosen; sie betrifft 3 – 5% aller Schwangeren (14). Neben den Leitsymptomen Hypertonie kann sie auch zu neuartigen, progredienten Kopfschmerzen führen (15). Wenn zusätzlich Sehstörungen, Verwirrtheit oder epileptische Anfälle auftreten, sollte eine cerebrale MRI-Bildgebung notfallmässig erfolgen. Nicht selten zeigt sich dort als Komplikation der Grunderkrankung ein Posteriores Reversibles Encephalopathie-Syndrom (PRES). Es handelt sich hierbei um eine Autoregulationsstörung cerebraler Gefässe, die überwiegend das hintere Stromgebiet betrifft, zu epileptischen Anfällen und/oder Sehstörungen bis zur kortikalen Blindheit führen kann und intensivmedizinisch behandelt werden muss (16).
Cerebrale Venenthrombosen
Das Risiko für cerebrale Venenthrombosen ist durch eine Schwangerschaft deutlich erhöht (4, 17); die meisten Fälle treten im dritten Trimenon und im Wochenbett auf, wahrscheinlich Östrogen-assoziiert (18). Das Leitsymptom der cerebralen Venenthrombose ist ein akuter und starker Kopfschmerz, der sich langsam weiter verschlechtert. Auch epileptische Anfälle, fokal-neurologische Symptome und Hirndruckzeichen (Papillenödem, Vigilanzminderung, häufiges Erbrechen) können auftreten (19). Diagnostisch sollte bei progredienten Kopfschmerzen in der Schwangerschaft daher immer auch eine MR-Venographie («TOF», ohne Gadolinium) erfolgen (4). In mehr als einem Drittel der Fälle kommt es durch die venöse Abflussstörung zusätzlich zu intracerebralen Stauungsblutungen (18, 19).
Idiopathische Intrakranielle Hypertension (IIH)
Bei der idiopathischen intrakraniellen Hypertension (IIH) handelt es sich um eine intrakranielle Liquordruckerhöhung unklarer Ursache. Die Leitsymptome der IIH sind chronische Kopfschmerzen und Sehstörungen (Verschwommensehen, Gesichtsfeldeinschränkungen, seltener Doppelbilder etc.). In der Schwangerschaft kann sich eine vorbestehende IIH verschlechtern und im schlimmsten Fall zu einem vollständigen und permanenten Visusverlust führen (20), weshalb bei Kopfschmerzen in Kombination mit Sehstörungen eine rasche ophthalmologische und neurologische Vorstellung mit Frage nach Papillenschwellung und eine Lumbalpunktion mit Druckmessung (in Seitenlage) indiziert sind.
Reversibles Cerebrales Vasokonstriktionssyndrom (RCVS)
Das Reversible Cerebrale Vasokonstriktionssyndrom (RCVS, auch «Postpartale Angiopathie») ist – ähnlich dem PRES – eine vorübergehende Verengung von hirnversorgenden Gefässen, wahrscheinlich als Folge einer Fehlregulation der Gefässwände. Es handelt sich um einen neurologischen Notfall, der je nach Ausmass und Dauer der Gefässverengungen zu Hirninfarkten mit bleibenden neurologischen Ausfällen führen kann (21). Es gibt verschiedene Auslöser für das RCVS, unter anderem kann es in der Spätschwangerschaft – dann meist vergesellschaftet mit (Prä-)Eklampsie – und im Wochenbett auftreten. Klinisch manifestiert es sich typischerweise mit (rezidivierenden) Donnerschlagkopfschmerzen, die z.T. auch von neurologischen Ausfällen begleitet sein können, z.B. einer Hemiparese. Die Diagnose kann mittels MR-Angiographie (in der Schwangerschaft «TOF», ohne Gadolinium) gestellt werden, in der sich klassischerweise Vasospasmen nachweisen lassen.
Liquorunterdrucksyndrom
Als Folge einer periduralen Anästhesie (PDA) im Zuge der Geburt kann im Wochenbett ein Liquorunterdrucksyndrom entstehen. Klinisch äussert sich dieses mit lageabhängigen, helmförmigen Kopfschmerzen ausschliesslich oder verstärkt in aufrechter Position, die rasch nachlassen, sobald sich die Patientin hinlegt. Auch Ohrdruck/Tinnitus, Nackensteife, Lichtempfindlichkeit, Übelkeit, Doppelbilder (i.R. einer Abduzensparese) und Schwindel können auftreten. Wenn die Beschwerden direkt nach einem periduralen Eingriff auftreten und als eindeutig lageabhängig beschrieben werden, ist ein MRI nicht zwingend notwendig. Falls keine Besserung durch konservative Therapie (Bettruhe, Coffein, Analgetika) eintritt, kann die Punktionsstelle mit einem Blutpatch verklebt werden. Folgeschäden durch einen PDA-assoziierten Liquorunterdruck sind selten (22).
Copyright bei Aerzteverlag medinfo AG
Universitätsspital Basel,
Klinik und Poliklinik für Neurologie
Petersgraben 4
4031 Basel
Universitätsspital Basel,
Klinik und Poliklinik für Neurologie
Petersgraben 4
4031 Basel
LD: Die Autorin hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
AP: Advisory Boards (Lundbeck Schweiz, AbbVie AG) und Referentenhonorare (Eli Lilly, Teva).
1. Chin JH, Vora N. The global burden of neurologic diseases. Neurology. 2014 Jul 22;83(4):349-51. doi: 10.1212/WNL.0000000000000610. PMID: 25049303; PMCID: PMC4115599.
2. Ashina M, Katsarava Z, Do TP, Buse DC, Pozo-Rosich P, Özge A, Krymchantowski AV, Lebedeva ER, Ravishankar K, Yu S, Sacco S, Ashina S, Younis S, Steiner TJ, Lipton RB. Migraine: epidemiology and systems of care. Lancet. 2021 Apr 17;397(10283):1485-1495. doi: 10.1016/S0140-6736(20)32160-7. Epub 2021 Mar 25. PMID: 33773613.
3. Stewart WF, Wood C, Reed ML, Roy J, Lipton RB; AMPP Advisory Group. Cumulative lifetime migraine incidence in women and men. Cephalalgia. 2008 Nov;28(11):1170-8. doi: 10.1111/j.1468-2982.2008.01666.x. Epub 2008 Jul 15. PMID: 18644028.
4. Rayhill M. Headache in Pregnancy and Lactation. Continuum (Minneap Minn). 2022 Feb 1;28(1):72-92. doi: 10.1212/CON.0000000000001070. PMID: 35133312.
5. Sances G, Granella F, Nappi RE, Fignon A, Ghiotto N, Polatti F, Nappi G. Course of migraine during pregnancy and postpartum: a prospective study. Cephalalgia. 2003 Apr;23(3):197-205. doi: 10.1046/j.1468-2982.2003.00480.x. PMID: 12662187.
6. Granella F, Sances G, Pucci E, Nappi RE, Ghiotto N, Napp G. Migraine with aura and reproductive life events: a case control study. Cephalalgia. 2000 Oct;20(8):701-7. doi: 10.1111/j.1468-2982.2000.00112.x. PMID: 11167898.
7. Duong S, Bozzo P, Nordeng H, Einarson A. Safety of triptans for migraine headaches during pregnancy and breastfeeding. Can Fam Physician. 2010 Jun;56(6):537-9. PMID: 20547518; PMCID: PMC2902939.
8. Puledda F, Shields K. Non-Pharmacological Approaches for Migraine. Neurotherapeutics. 2018 Apr;15(2):336-345. doi: 10.1007/s13311-018-0623-6. PMID: 29616493; PMCID: PMC5935652.
9. https://compendium.ch
10. Luckner A et al, Magnesium in Migraine Prophylaxis-Is There an Evidence-Based Rationale? A Systematic Review. Headache 2018
11. Schankin C et al, Der Kopfschmerzpatient auf der Notfallstation – wie weiter? Swiss Medical Forum 2017.
12. Sandoe CH and Lay C, Secondary Headaches During Pregnancy: When to Worry, Headache 2019 (PMID: 31011857).
13. Negro, A., et al. „Headache and pregnancy: a systematic review.“ The journal of headache and pain 18 (2017): 1-20.
14. Roberts, J. M., and Desmond W. Cooper. „Pathogenesis and genetics of pre-eclampsia.“ The Lancet 357.9249 (2001): 53-56.
15. Gestational Hypertension and Preeclampsia: ACOG Practice Bulletin, Number 222. Obstet Gynecol 2020;135(6): e237–e260. doi:10.1097/AOG.0000000000003891
16. Sells CM, Feske SK. Stroke in pregnancy. Semin Neurol 2017;37(6):669–678. doi:10.1055/s-0037-1608940
17. Bousser MG, Ferro JM. Cerebral venous thrombosis: an update. Lancet Neurol. 2007 Feb;6(2):162-70. doi: 10.1016/S1474-4422(07)70029-7. PMID: 17239803.
18. Liang ZW, Gao WL, Feng LM. Clinical characteristics and prognosis of cerebral venous thrombosis in Chinese women during pregnancy and puerperium. Sci Rep 2017; 7:43866 doi:10.1038/srep43
19. Cantú C, Barinagarrementeria F. Cerebral venous thrombosis associated with pregnancy and puerperium. Review of 67 cases. Stroke 1993;24(12):1880–1884. doi:10.1161/01. str. 24.12.1880
20. Scott, Caroline, and Chandrasekaran Kaliaperumal. „Idiopathic intracranial hypertension and pregnancy: A comprehensive review of management.“ Clinical Neurology and Neurosurgery217 (2022): 107240.
21. Berlit, P., and S. Schönenberger. „Schwangerschaft und Schlaganfall.“ Aktuelle Neurologie 41.08 (2014): 443-446.
22. Kuczkowski, Krzysztof M. „The management of accidental dural puncture in pregnant women: what does an obstetrician need to know?.“ Archives of gynecology and obstetrics 275 (2007): 125-131.