Eine Vielzahl von Nahrungsmittelmängel, erworbene oder genetische Krankheiten, medikamentöse Therapien oder Intoxikationen können eine Anämie verursachen. Diese ist weltweit sehr prävalent und nimmt im Alter zu. Die Abklärung beginnt mit der Zählung von Retikulozyten im Blut und mit Bestimmung des MCV. Im Anschluss müssen weitere Labortests möglichst gezielt eingesetzt werden. Neuere Marker und Algorithmen helfen vor allem bei der Differenzierung von Eisenmangelanämie (IDA) und Anämie der chronischen Erkrankung (ACD).
Anämie, definiert als verminderte Hämoglobin- oder Erythrozytenkonzentration unterhalb eines Geschlechts-, Alters-, Schwangerschafts- und genetisch abhängigen Referenzwertes, ist weltweit mit einer hohen Prävalenz (30%) zu finden. Dabei genügt die Hämoglobin- oder Erythrozytenmasse nicht mehr, die physiologischen Bedürfnisse (Sauerstoffzufuhr ins Gewebe) zu erfüllen. Anämie ist mit erhöhter Morbidität und Mortalität vergesellschaftet. Anämie ist per se keine Krankheit, sondern das Resultat von angeborenen oder erworbenen Defekten, inklusive deren Kombination. Da die Diagnose von einer relativen Zahl abhängt (Gramm Hämoglobin pro Liter Vollblut) führen Zustände, bei welchen das Plasmavolumen erhöht ist (Dilution) zu einer Pseudoanämie (z.B. Herzinsuffizienz, Infusionen, Schwangerschaft). Die Ursachen von echten Anämien sind sehr vielfältig und teils komplex, insbesondere bei gleichzeitig vorliegenden Ätiologien. Es kann in der Schweiz davon ausgegangen werden, dass die Analytik präzise ist und entsprechend adaptierte Referenzwerte angegeben werden.
Auf der Suche nach der Ätiologie
Wenn immer möglich sollte die Ursache(n) gefunden werden, um eine Prognose stellen zu können und eine Vorhersicht einer kausalen Therapie zu haben. Anamnese (allenfalls auch Familienanamnese) und klinischer Untersuch haben eine grosse Bedeutung. Ernährung, Blutungen, Entzündungen und Infekte, Begleiterkrankungen (Rheuma, Krebs, Darmerkrankung), anämisierende Therapien und zeitlicher Verlauf sind zu erwägen. Zusammen mit der Kenntnis über Prävalenzen (Altersheimbewohner, gesundheitsbewusste Sportlerinnen, soziale Faktoren, etc.) in verschiedenen Bevölkerungsgruppen, helfen die erhobenen klinischen Befunde die richtige Auswahl an weiterführenden Abklärungen zu treffen. Es gibt eine riesige (Un)-Zahl an Labor- und anderen Methoden, um Anämien abzuklären.
Reti und MCV (Index) als Einstieg
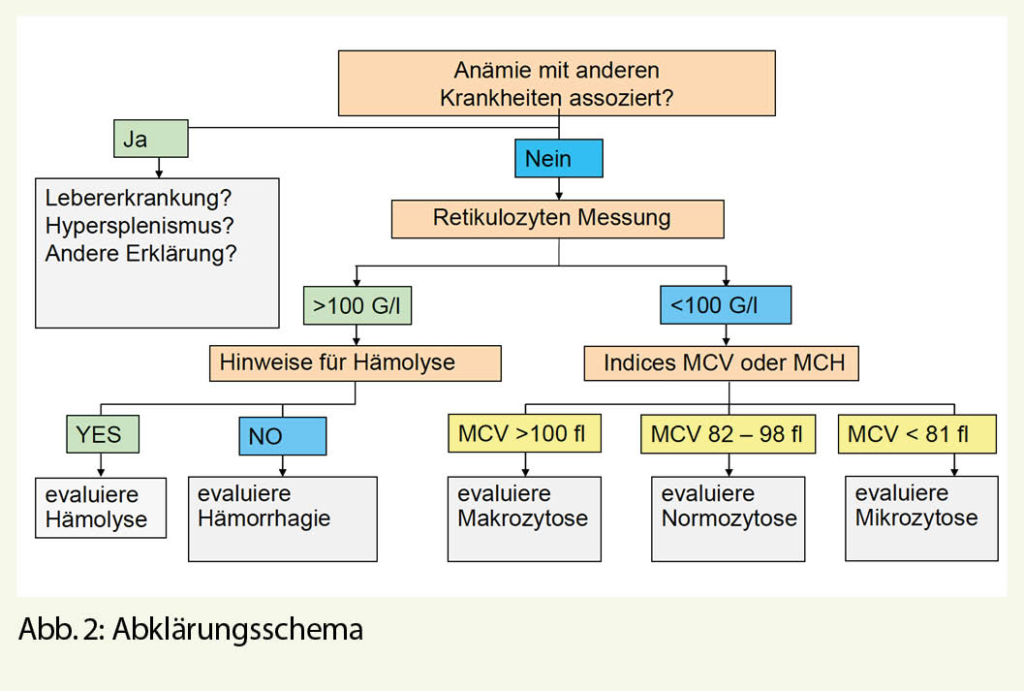
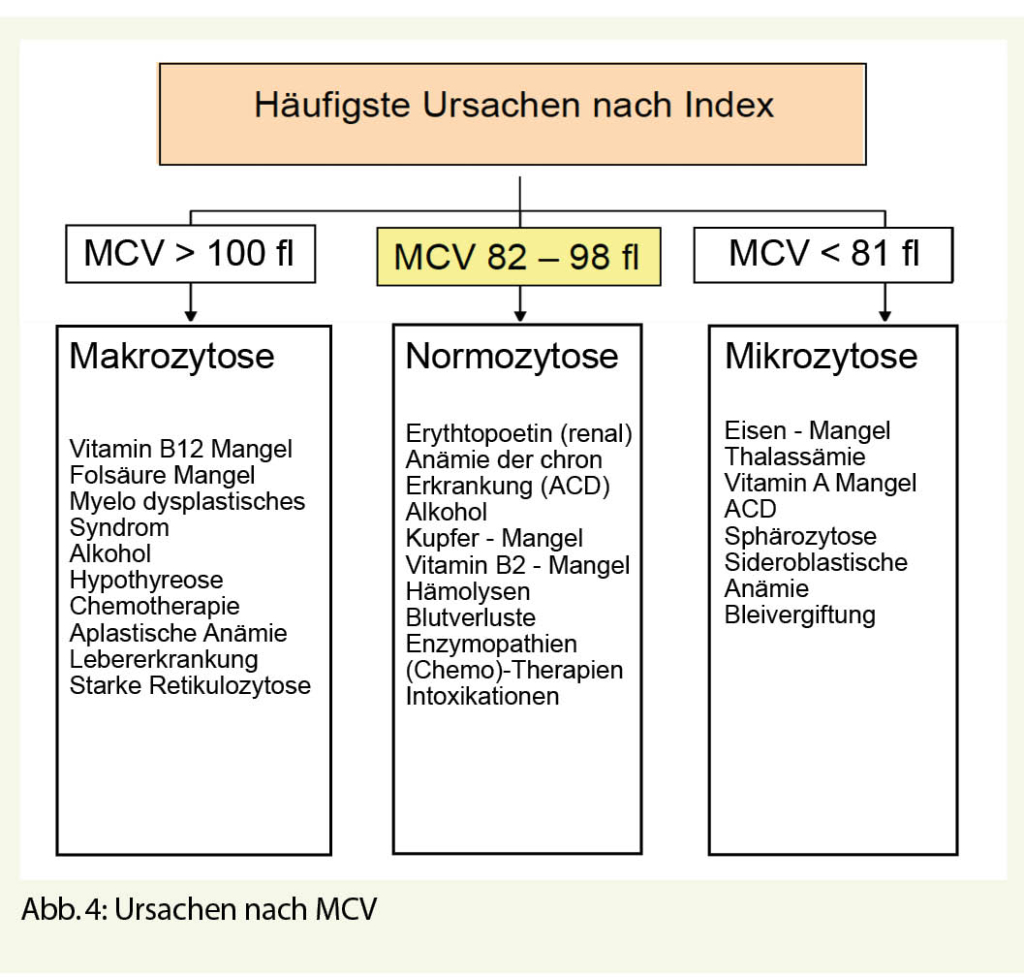
Mit einem einfachen (heute fast immer maschinellen) Hämatogramm erhält man Auskunft über die gemittelte Grösse (Volumen) der vorliegenden Erythrozytenpopulation. Es werden 3 Gruppen definiert, nämlich Mikrozytose, Normozytose und Makrozytose (entspricht in der Regel dem mikroskopischen Befund im Ausstrich). Zusätzlich ist die Messung der unreifen Erythrozyten, die Retikulozyten sehr wichtig. Hiermit werden zum einen gewisse Differenzialdiagnosen gruppiert und zum andern erfasst, ob die Produktion im Knochenmark gebremst oder stimuliert ist. Bei Kombinationszuständen (z.B. Eisenmangel und B12-Mangel) kann die Einteilung nach Zellgrösse versagen. Der optisch analysierte Blutausstrich ist mit etwas Erfahrung bei vielen Anämien pathognomonisch.
Folgeanalysen gezielt anwenden
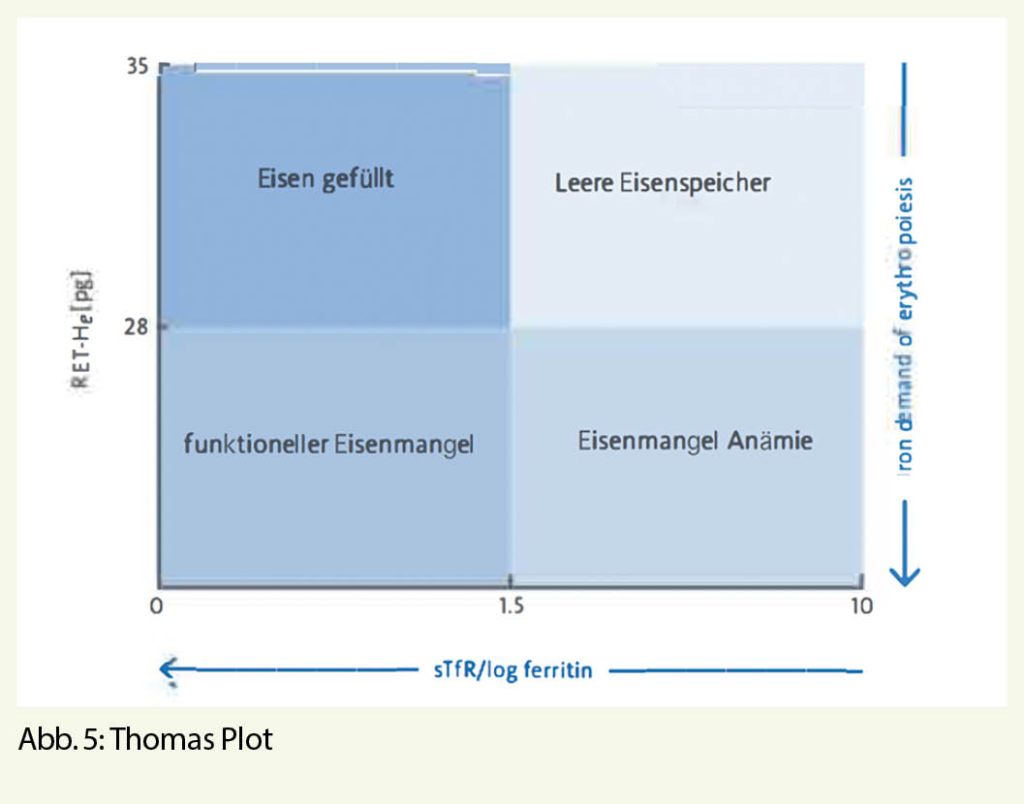
Bei Verdacht auf Störung durch Fehlen von Nahrungsmittel (Zufuhr, Aufnahme) sind die entsprechenden Kandidaten zu messen. Dabei können alle MCV-Gruppen betroffen sein. Ausgerechnet beim häufigsten Mangel – dem Eisenmangel (IDA) – gibt es Fallstricke. Das Ferritin ist ein Akutphasenprotein und steigt bei Entzündungen unspezifisch an. Zudem sagt es nur etwas über die Eisenreserven aus. Bei Verwendung als Eisenersatz-Zielwert sind je nach Begleitkrankheit (Herzinsuffizienz, Niereninsuffizienz, Schwangerschaft) verschiedene Werte zu erreichen. Gelegentlich braucht es zusätzliche Marker wie Transferrin-Sättigung, Zinkprotoporphyrin, löslicher Transferrin Rezeptor, Entzündungsparameter (CRP) oder Hepcidin. Neuere Marker wie Ret He (= durchschnittliche Konzentration von Hämoglobin pro Retikulozyt), %Hypo (Anteil hypochromer Erythrozyten) oder Delta He (Ret He minus Ery He) sind viel spezifischer als z.B. Ferritin zur Abgrenzung von IDA von Anämie der chronischen Erkrankung. Interessant ist auch der Ferritin Index (sTfR/log Ferritin) in Zusammenhang mit Diagnose von Eisenmangel (sog. Thomas Plot). Letztlich empfiehlt es sich allenfalls nach einer erfolglosen probatorischen Therapie, weitere, seltenere Ursachen zu suchen.
Genetisch bedingte Anämien, nämlich Hämoglobinopathien, insbesondere Thalassämien sind auch in unseren Breitengraden gar nicht selten. Das Hämatogramm gibt schon einen Hinweis (Polyglobulie bei milder Anämie). Die Diagnose wird durch Spezialanalytik, bei alpha Thalassämien molekulargenetisch gestellt. G6PD-Mangel und Pyruvatkinase-Mangel sind weitere kongenitale Anämien und zusammen mit Membranerkrankungen (Sphärozytose, etc.) nicht so selten und werden nicht immer im Kindesalter gestellt. Auch hier ist Spezialanalytik gefragt.
Anämien mit maligner klonaler Ursache sind Myelodysplastische Syndrome (MDS), aplastische Anämie (AA) und Leukämien. Hier finden sich neben einer Anämie meist auch Veränderungen der Leukozyten und/oder Thrombozyten. Beim Vorliegen einer makrozytären Anämie im Frühstadium eines MDS kann es schwierig sein die richtige Diagnose zu stellen und es bedarf Erfahrung in Mikroskopie des Blutbildes, Ausschlussanalysen und molekularbiologischen Abklärungen. Anämien treten oft auch im Zusammenhang mit Karzinomen auf ohne oder mit Knochenmarksbefall (Myelophtysis). Die Pathomechanismen sind wohl am ehesten über Entzündungsmediatoren gesteuert. Obendrauf auch durch allfällige (chemo-) Therapien.
Anämie der chronischen Erkrankung (ACD)
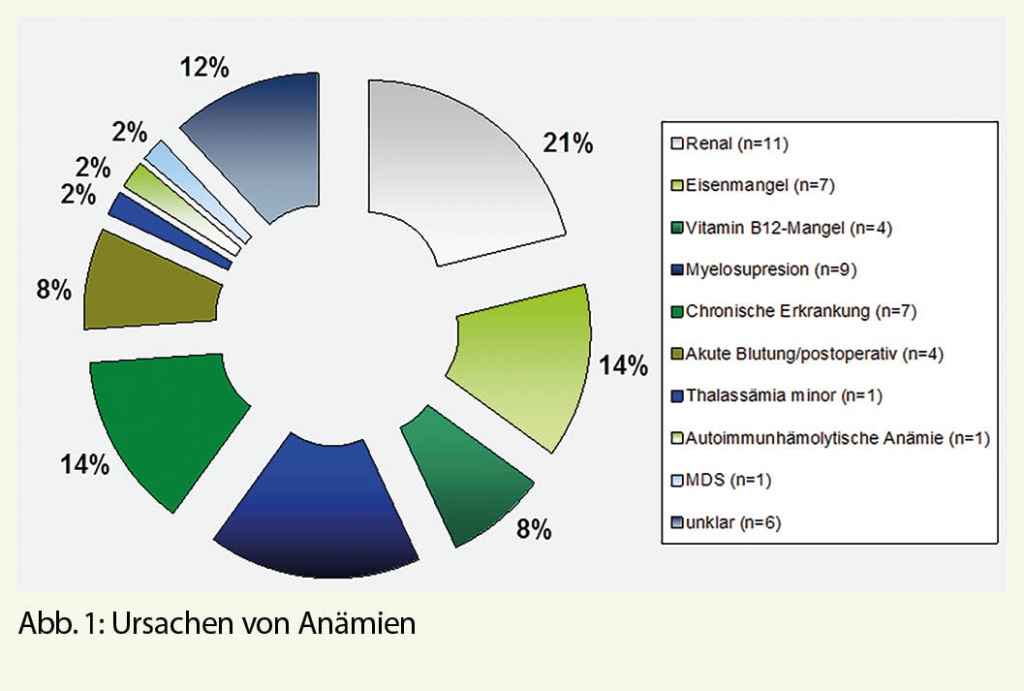
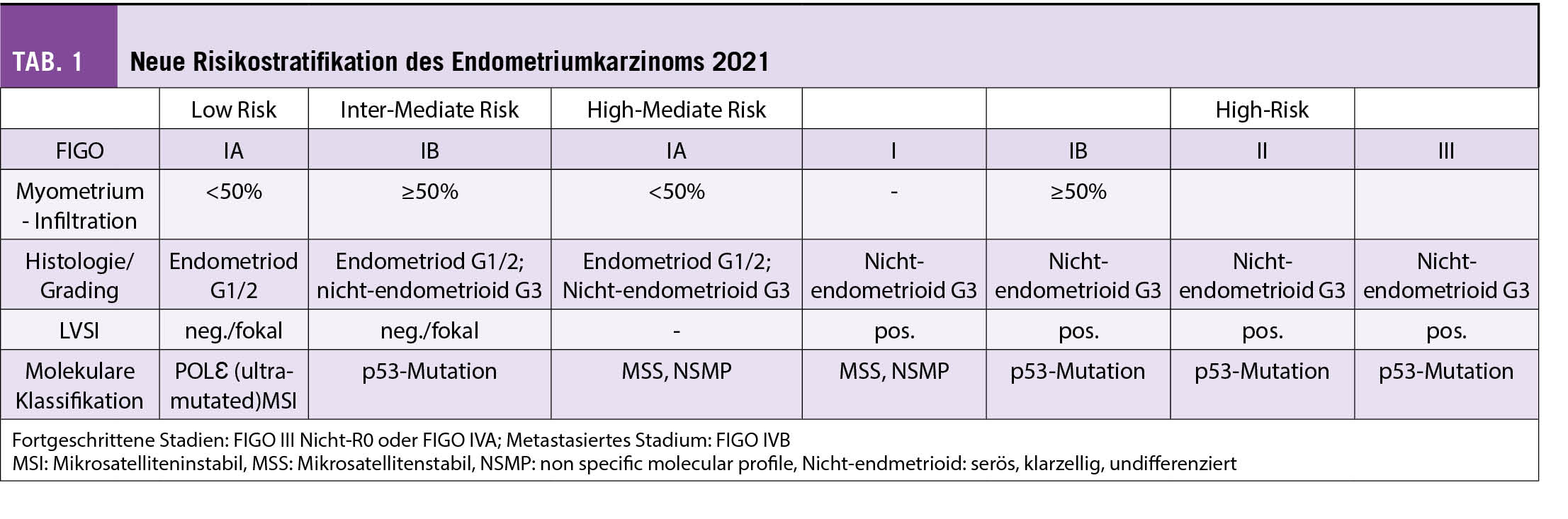
Anämie der chronischen Erkrankung ist die 2. häufigste Anämieform mit Anstieg im Alter. Die Ursachen sind vielgestaltig. Ebenso die Pathomechanismen. Ursächlich finden sich Infektionen, Tumore, Nieren- und Autoimmunerkrankungen (Tab. 1).
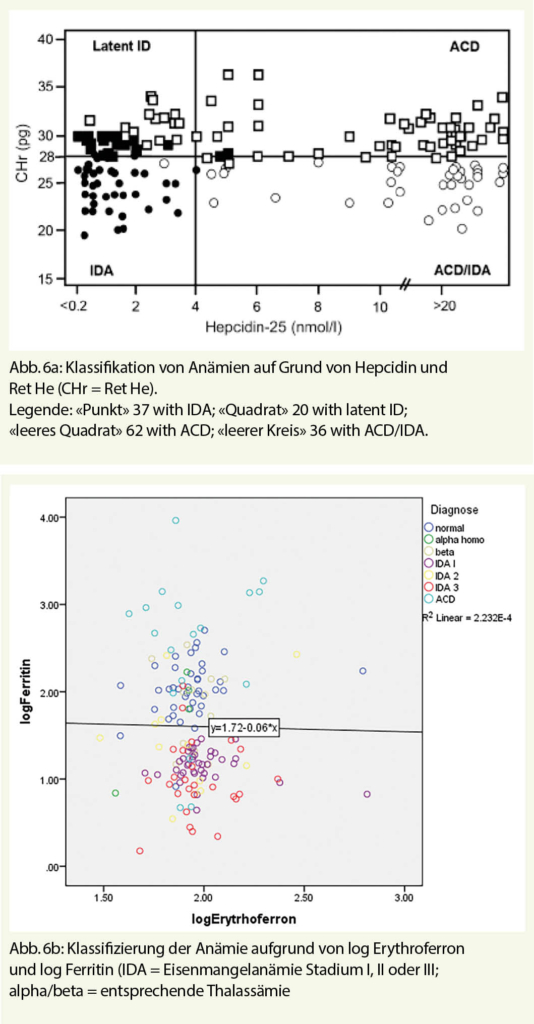
Wenn immer möglich soll die zu Grunde liegende Krankheit behandelt werden, ansonsten kann Erythropoetin eingesetzt werden, sofern genügend Eisen vorhanden ist. Es ist mehr und mehr klar, dass Hepcidin und Erythroferron pathophysiologisch eine wichtige Rolle spielen. Diese helfen auch in der Diagnostik, besonders bei der Differenzierung von ACD und Eisenmangelanämie wie in Abbildung 6 gezeigt.
Trotz aufwändiger Abklärung gibt es eine Prozentzahl von Fällen, bei denen keine Diagnose gefunden werden kann. In der Altersanämie kann das bis zu 25% der Fälle ausmachen selbst bei Berücksichtigung des korrekt angepassten Referenzwertes.
Copyright bei Aerzteverlag medinfo AG
Private Universität im Fürstentum Liechtenstein
Dorfstrasse 24
FL-9495 Triesen
andreas.huber@ufl.li
LaboSalamin
Ave. du Rothorn 10, 3960 Sierre
s.brunner@labosalamin.ch
Die Autoren haben keine Interessenkonflikte im Zusammenhang mit diesem Beitrag deklariert.
1 Bärlocher K. Vitaminmangel am Beispiel der Folate. der informierte @rzt. 2021; 11 Ausgabe 7Juli
2. Walter P, Infanger E, Mühlemann P. Food Pyramid of the Swiss Society for Nutrition. Ann Nutr Metab 2007;51(suppl 2):15–20
3. Rohrmann S, Pestoni G, Krieger JP, Faeh D, Sych J, Chatelan A, Bochud M. menuCH – wie ernährt sich die Schweiz? Schweizer Zeitschrift für Ernährungsmedizin 1, 2020 20-22
4. Huang Z, Yu Liu Y, Qi G, Brand D, and Zheng SG. Role of Vitamin A in the Immune System. J Clin Med. 2018; 7(9): 258. doi: 10.3390/jcm7090258.
5. Charoenngam N, Holick MF. Immunologic Effects of Vitamin D on Human Health and Disease. Nutrients. 2020 Jul 15;12(7):2097. doi: 10.3390/nu12072097.
6. Panagiotou G, Tee SA, Ihsan Y, Athar W, Marchitelli G, Kelly D, Boot CS, Stock N, Macfarlane J, Martineau AR, Burns G, Quinton R. Low serum 25- hydroxyvitamin D (25[OH]D) levels in patients hospitalized with COVID-19 are associated with greater disease severity. Clin Endocrinol (Oxf). 2020 Oct;93(4):508-511.
7. Annweiler C, Hanotte B, Grandin de l’Eprevier C, Sabatier JM, Lafaie L, Célarier T. Vitamin D and survival in COVID-19 patients: A quasi-experimental study. J Steroid Biochem Mol Biol. 2020 Nov;204:105771. doi: 10.1016/j.jsbmb.2020.105771. Epub 2020 Oct 13. PMID: 33065275; PMCID: PMC7553119.
8. Sooriyaarachchi P, Jeyakumar DT, King N, Jayawardena R. Impact of vitamin D deficiency on COVID-19. Clin Nutr ESPEN. 2021 Aug;44:372-378. doi: 10.1016/j.clnesp.2021.05.011. Epub 2021 May 29. PMID: 34330492; PMCID: PMC8164501.
9. Chiu SK, Tsai KW, Wu CC, Zheng CM, Yang CH, Hu WC, Hou YC, Lu KC, Chao YC. Putative Role of Vitamin D for COVID-19 Vaccination. Int J Mol Sci. 2021 Aug 20;22(16):8988. doi: 10.3390/ijms22168988. PMID: 34445700; PMCID: PMC8396570.
10. Lee GY, Han SN. The Role of Vitamin E in Immunity. Nutrients. 2018 Nov 1;10(11):1614. doi: 10.3390/nu10111614. PMID: 30388871; PMCID: PMC6266234.
11. Beck MA, Kolbeck PC, Rohr LH, Shi Q, Morris VC, Levander OA. Vitamin E deficiency intensifies the myocardial injury of coxsackievirus B3 infection of mice. J Nutr. 1994 Mar;124(3):345-58. doi: 10.1093/jn/124.3.345. PMID: 8120653.
12. Tutusaus A, Marí M, Ortiz-Pérez JT, Nicolaes GAF, Morales A, García de Frutos P. Role of Vitamin K-Dependent Factors Protein S and GAS6 and TAM Receptors in SARS-CoV-2 Infection and COVID-19-Associated Immunothrombosis. Cells. 2020;9(10):2186. Published 2020 Sep 28. doi:10.3390/cells9102186
13. Liugan M, Carr AC. Vitamin C and Neutrophil Function: Findings from Randomized Controlled Trials. Nutrients. 2019 Sep 4;11(9):2102. doi: 10.3390/nu11092102. PMID: 31487891; PMCID: PMC6770220.
14. Peterson CT, Rodionov DA, Osterman AL, Peterson SN. B Vitamins and Their Role in Immune Regulation and Cancer. Nutrients. 2020 Nov 4;12(11):3380. doi: 10.3390/nu12113380. PMID: 33158037; PMCID: PMC7693142.
15. Moser U. Vitamins – wrong approaches. Int J Vitam Nutr Res. 2012 Oct;82(5):327-32. doi: 10.1024/0300-9831/a000127. PMID: 23798051.