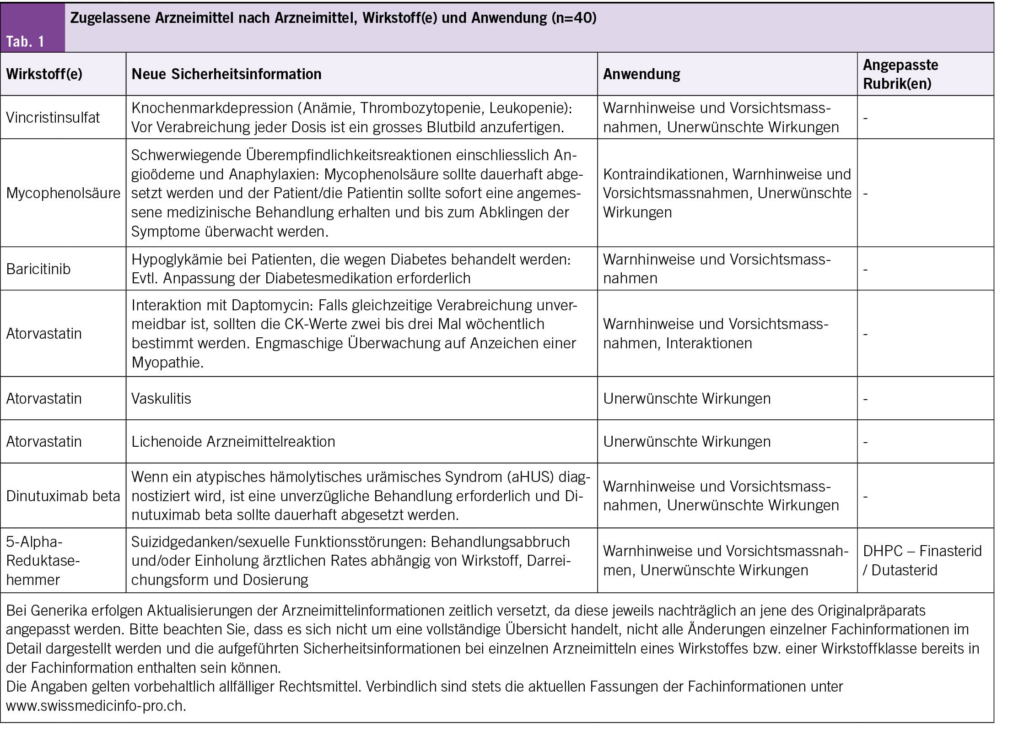
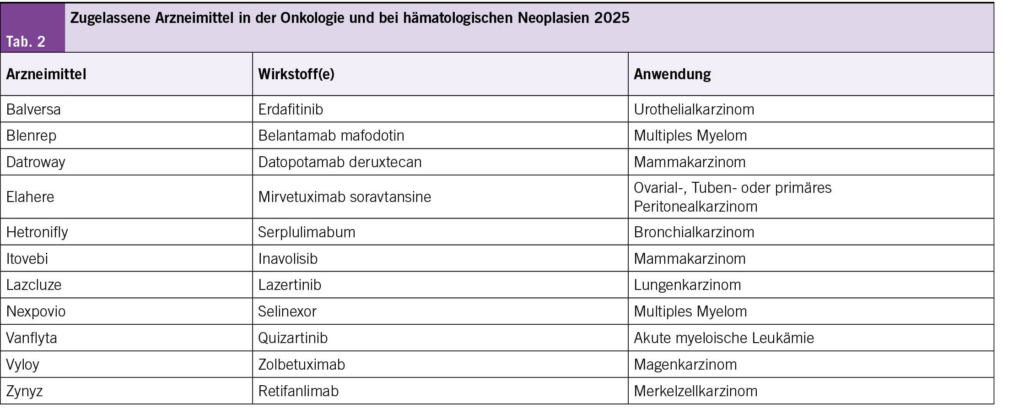
Sicherheit, Durchführbarkeit und Patientenerfahrung bei zehnminütigen Pembrolizumab-Infusionen
Die steigende Krebsinzidenz und der Personalmangel erfordern effizientere Arbeitsabläufe in der ambulanten Onkologie. Pembrolizumab wird üblicherweise über einen Zeitraum von 30 Minuten verabreicht. Diese prospektive Studie untersuchte die Sicherheit und die Patientenerfahrung bei einer Verkürzung der Pembrolizumab-Infusionsdauer auf 10 Minuten, um die Effizienz der Arbeitsabläufe in der ambulanten Onkologie zu verbessern.
Methoden
In dieser prospektiven Single-Centre-Studie an einem grossen niederländischen Lehrkrankenhaus waren Erwachsene, die Pembrolizumab für eine zugelassene Indikation erhielten, teilnahmeberechtigt, wenn sie keine Vorgeschichte von infusionsbedingten Reaktionen (IRRs) des Grades ≥ 2 hatten. Nach zwei standardmässigen 30-minütigen Infusionen ohne IRRs wurde die Dauer auf 15 und anschliessend auf 10 Minuten reduziert. Die Vitalparameter wurden vor und nach der Infusion überwacht. Unerwünschte Ereignisse wurden gemäss den Common Terminology Criteria for Adverse Events v5.0 bewertet. Die Pembrolizumab-Talspiegel und die von den Patienten berichteten Erfahrungswerte wurden erfasst. Der primäre Endpunkt war die Inzidenz von IRRs des Grades ≥ 2 während verkürzter Infusionen, wobei die Sicherheit vorab auf < 10% festgelegt wurde.
Ergebnisse
Von 97 eingeschriebenen Patienten schlossen 78 das Protokoll ab; die Abbrüche waren hauptsächlich auf das Fortschreiten der Erkrankung oder nicht damit zusammenhängende unerwünschte Ereignisse zurückzuführen. Ein Patient (1.1% [95%-KI, 0.0 bis 6.1]) erlitt während verkürzter Infusionen eine IRR des Grades 2; es traten keine IRRs des Grades ≥ 3 auf. Die meisten Patienten gaben eine hohe Zufriedenheit an, und es wurden über 150 Stunden ambulante Infusionskapazität eingespart.
Schlussfolgerungen
Zehnminütige Pembrolizumab-Infusionen sind sicher und gut verträglich und verbessern sowohl die Patientenzufriedenheit als auch die ambulante Effizienz.
Quelle: Safety, Feasibility, and Patient Experience of Ten-Minute Pembrolizumab Infusions: A Prospective Cohort Study, Authors: Elianne C.S. de Boer
Aktivüberwachungsstudie mit Metformin bei risikoarmem Prostatakrebs
Die aktive Überwachung (AS) ist eine Standardbehandlungsstrategie für Prostatakrebs (PCa) mit geringem Risiko, jedoch kommt es bei einem erheblichen Anteil der Patienten letztendlich zu einem Fortschreiten der Erkrankung. Metformin, ein häufig verschriebenes Antidiabetikum, hat in präklinischen Studien und Beobachtungsdaten eine Antitumoraktivität gezeigt, was zu Untersuchungen hinsichtlich seines Potenzials zur Verzögerung des Fortschreitens von PCa geführt hat.
Patienten und Methoden
Die Metformin Active Surveillance Trial (MAST) war eine multizentrische, randomisierte, doppelblinde, placebokontrollierte Phase-III-Studie zur Bewertung der Wirksamkeit von Metformin bei Männern mit lokal begrenztem PCa mit geringem Risiko, die mit AS behandelt wurden. Die teilnahmeberechtigten Teilnehmer wurden im Verhältnis 1:1 randomisiert entweder der Metformin-Gruppe (850 mg zweimal täglich) oder der Placebo-Gruppe zugewiesen und bis zu 36 Monate lang beobachtet. Der primäre Endpunkt war die Zeit bis zum Fortschreiten der Erkrankung, definiert als therapeutisches und/oder pathologisches Fortschreiten. Das progressionsfreie Überleben (PFS) wurde anhand der Kaplan-Meier-Analyse und Cox-Proportional-Hazards-Modellen bewertet.
Ergebnisse
Insgesamt wurden 408 Patienten randomisiert (205 Metformin, 203 Placebo). Nach einer medianen Nachbeobachtungszeit von 36 Monaten kam es bei 144 Teilnehmern zu einer Progression (70 Metformin, 74 Placebo), ohne dass ein signifikanter Unterschied im PFS festgestellt wurde (Hazard Ratio [HR], 1.09 [95%-KI, 0.79 bis 1.52]; P = 0.59). Die Negativrate der Biopsien nach 36 Monaten betrug 41.0% (Metformin) gegenüber 31.1% (Placebo; P = 0.181). In einer vorab festgelegten Subgruppenanalyse war Metformin mit einer erhöhten pathologischen Progression bei adipösen Patienten (BMI ≥ 30; HR, 2,3) assoziiert.
Schlussfolgerung
Metformin reduzierte das Fortschreiten bei Männern mit risikoarmem PCa unter AS nicht. Die bei adipösen Patienten beobachteten Beobachtungen müssen weiter untersucht werden.
Quelle: Fleshner NE et al. Metformin Active Surveillance Trial in Low-Risk Prostate Cancer. J Clin Oncol 2025; 43: 3662-3671(2025).DOI: 10.1200/JCO-25-01070
ctDNA-Variabilität vor Behandlung bei fortgeschrittenem NSCLC
Die Quantifizierung von Veränderungen der zirkulierenden Tumor-DNA (ctDNA) während der Behandlung ermöglicht eine schnelle Identifizierung von Patienten, die auf die Therapie ansprechen. Eine genaue Interpretation erfordert jedoch auch das Verständnis der Variabilität der ctDNA-Spiegel ohne Behandlung. In der vorliegenden Analyse von 360 Patienten mit fortgeschrittenem, epidermalem Wachstumsfaktor-Rezeptor-(EGFR)-mutiertem, nicht-kleinzelligem Lungenkrebs (NSCLC) wurden die Veränderungen der ctDNA-Spiegel in gepaarten Proben vor der Behandlung charakterisiert und Faktoren bewertet, die mit der Variabilität in Zusammenhang stehen.
Methoden
Bei Screening- und Zyklus-1-Proben (C1D1) von 132 zuvor unbehandelten und 228 zuvor behandelten Patienten aus den Studien FLAURA und AURA3 wurde die ctDNA mittels Next-Generation-Sequencing (Guardant360/GuardantOMNI NGS-Panel) quantifiziert und mittels digitaler Polymerase-Kettenreaktion (ddPCR, Biodesix) quantifiziert.
Ergebnisse
In den Studien FLAURA und AURA3 kam es bei 31/132 (23.5%) bzw. 43/228 (18.9%) Patienten mit paarweisen Vorbehandlungs-Plasmaproben zu einer Verringerung der ctDNA-Spiegel (Panel-Mittelwert VAF) um ≥ 20% vom Screening bis C1D1, darunter eine Verringerung um ≥ 50% bei 12 (9.1%) bzw. 23 (10.1%) Patienten. Eine Verringerung um 100% (ctDNA-Clearance) wurde bei 0 bzw. 5 (2.2%) Patienten beobachtet. Die Hintergrundvariabilität konnte nicht vollständig durch die technische Variabilität innerhalb von NGS oder durch NGS-ddPCR oder andere potenzielle Variabilitätsquellen erklärt werden. Grössere Veränderungen standen im Zusammenhang mit einer niedrigen VAF und einer geringen Menge an zellfreier DNA (cfDNA).
Quelle: Markovets a ET AL. Variability of Circulating Tumor DNA Levels in Plasma Samples From Patients With Advanced Non–Small-Cell Lung Cancer in the Absence of Treatment. JCO Precis Oncol 2025; 9: e2500287. DOI: 10.1200/PO-25-00287
SwissBreastCare
Bethanienspital
Toblerstrasse 51
8044 Zürich