Für kaum ein anderes Thema der Geburtshilfe existieren so viele Metaanalysen und Reviews wie für die Prävention der Frühgeburten (FG) und trotzdem bleibt bis dato vieles kontrovers diskutiert (1). In der Folge wird der aktuelle Wissensstand von wichtigen Pfeilern in der Prävention der Frühgeburtlichkeit beleuchtet.
Die Rate an Frühgeburten (FG), d.h. Lebendgeburten vor 37 Schwangerschaftswochen (SSW), liegt in Europa bei ca. 8.7% (6,3-13,3%) (2) und lag 2019 in der Schweiz bei 6.7% (3).
Eine FG geht je nach Gestationsalter mit einer erheblichen Morbidität, aber auch möglichen Mortalität einher. Folglich bleibt die Bestrebung, die FG-Rate zu reduzieren, ein zentrales Ziel der modernen Geburtshilfe (4, 5). Die wichtigsten Risikofaktoren der FG sind der Status nach (St. n.) spontaner FG (OR 3.6; CI 95%
3.2-4.0), ein Schwangerschaftsintervall <12 Monate (OR 4.2; CI 95% 3.0-6.0) sowie eine vaginale Blutung in der Spätschwangerschaft (OR 5.9; CI 95% 5.1-6.9) (4-7). Das grösste Risiko für eine FG stellt aber eine Mehrlingsschwangerschaft dar (OR ≥ 6) (5). Somit hat die Prävention von Mehrlingsschwangerschaften im Rahmen der reproduktionsmedizinischen Therapien eine grosse Bedeutung. Das Wiederholungsrisiko bei St. n. FG liegt bei 30% (CI 95%; 27% bis 34%) (8).
Primäre Prävention
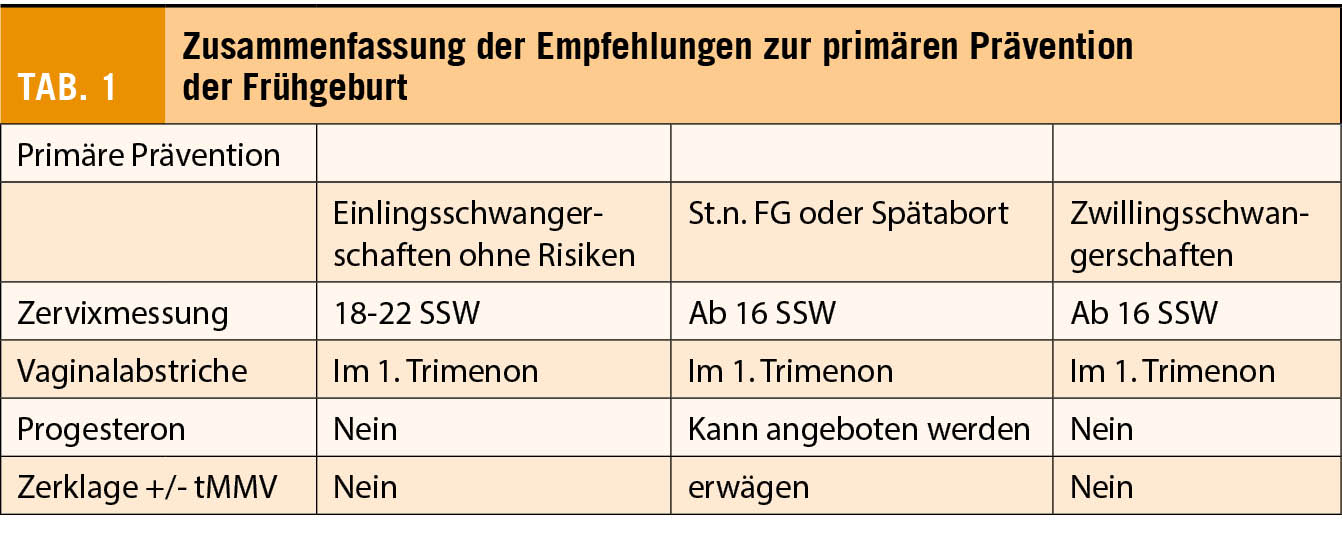
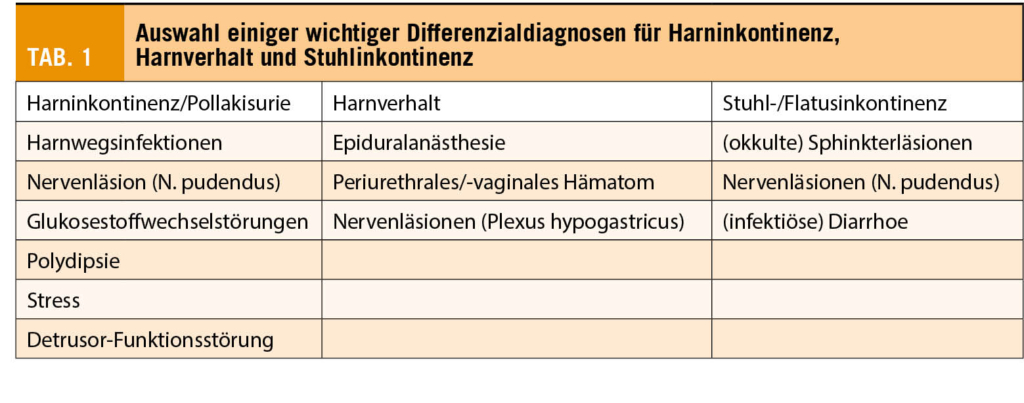
Die primäre Prävention bezieht sich auf eine Vorsorgemassnahme bei asymptomatischen Patientinnen mit erhaltener Zervix (Zx). Je nach Intervention wird spezifiziert, ob alle Schwangeren davon profitieren sollen, oder ob es sich um eine Massnahme handelt, die speziell Frauen mit St. n. FG oder Spätabort bzw. mit Zwillingsschwangerschaften angeboten werden soll. Tabelle 1 fasst die Empfehlungen der primären Prävention zusammen.
Messung der Zervixlänge
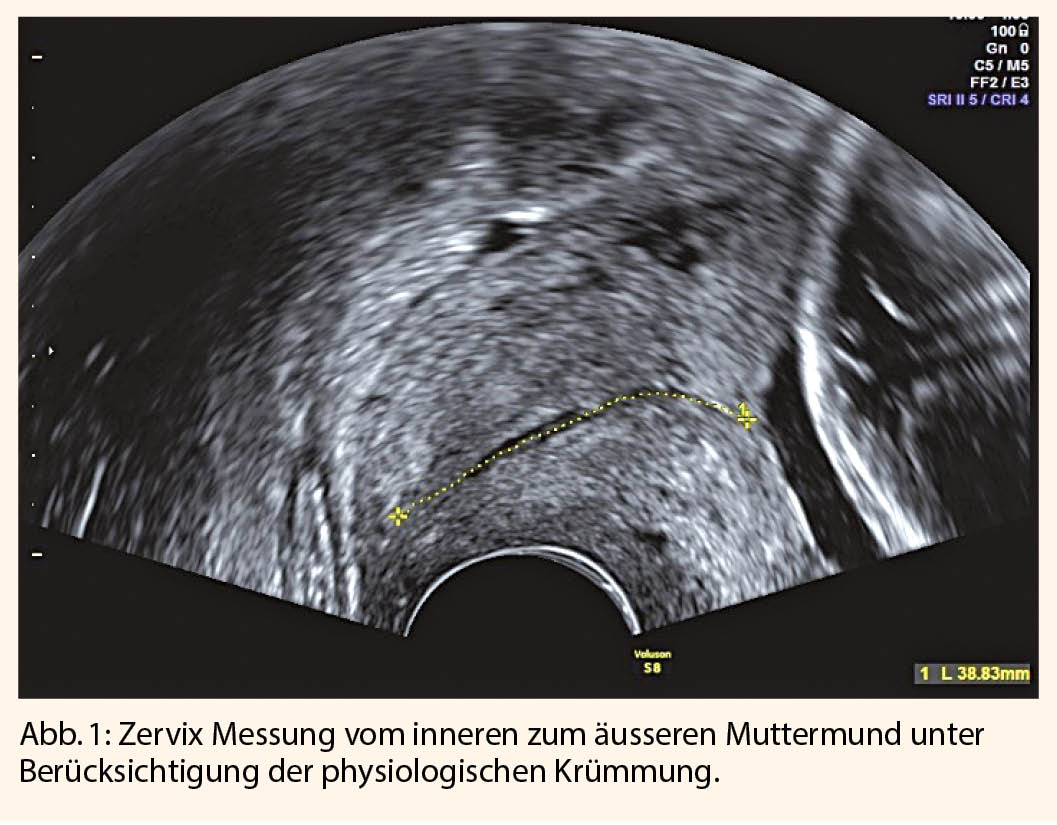
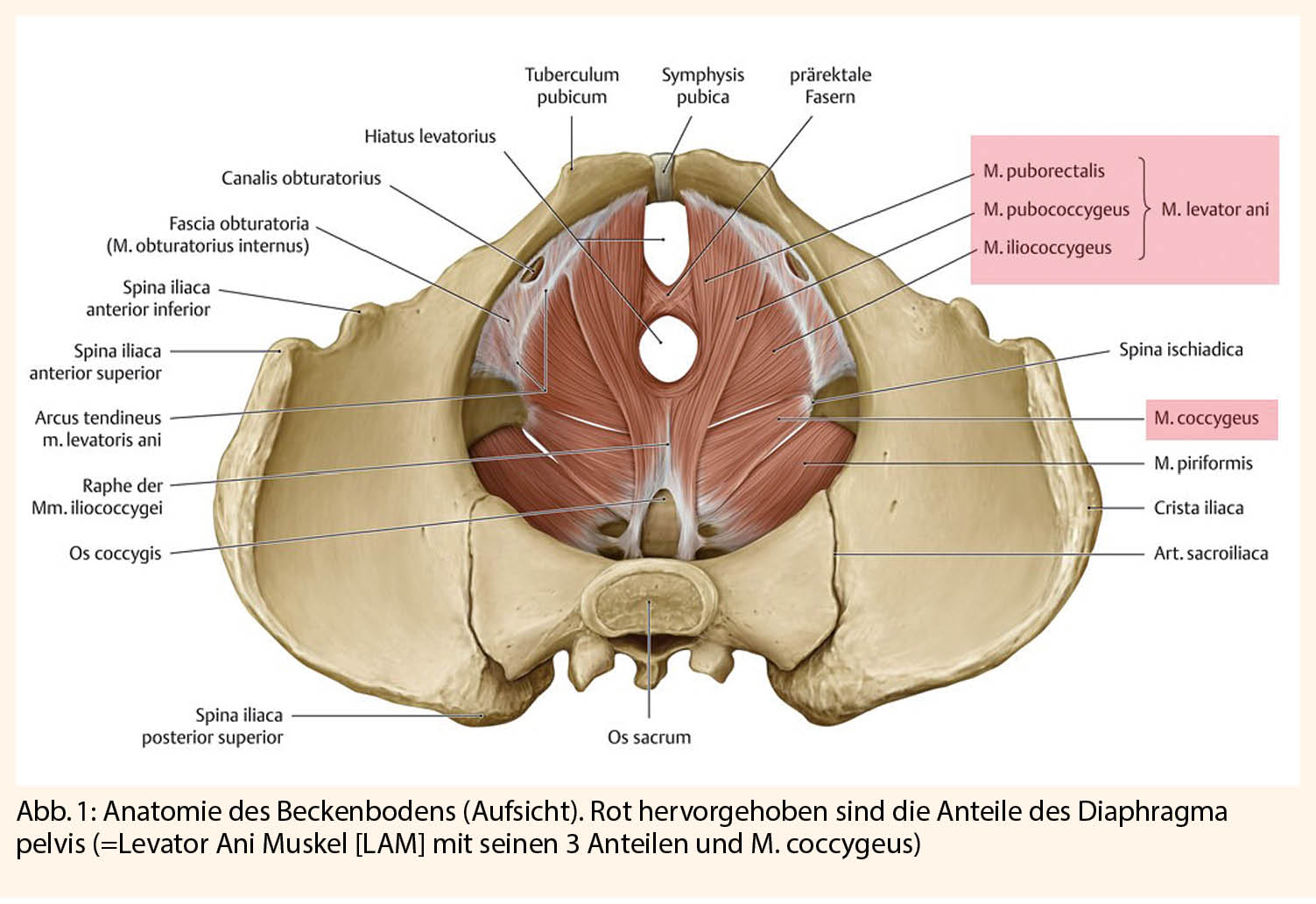
Das Risiko einer FG ist indirekt proportional zur Zervixlänge. In den Empfehlungen der schweizerischen Gesellschaft für Ultraschall in der Medizin (SGUM) wurde die Messung der Zervixlänge beim 2. Trimester Screening (20-23 SSW) vor über 10 Jahren implementiert (9). Mittlerweile findet sich die Empfehlung für eine routinemässige Zervixmessung bei 18-22 SSW auch in den Leitlinien des American College of Obstericians and Gynecologists (ACOG) (4). Die Messung soll in einem Längsschnitt vom innern zum ässeren Muttermund erfolgen, gegebenenfalls auch unter Berücksichtigung der physiologischen Krümmung (Abb. 1). Bei einer transabdominalen Messung von ≤ 25mm soll eine transvaginale Nachmessung erfolgen (10). Die Messung des Trichters hat keine Relevanz. Per Definition gilt vor der 25 SSW ist eine Zervixlänge von ≤ 25mm als verkürzt und ist mit einem signifikant erhöhten FG-risiko assoziiert (11). Bei St.n. FG oder Spätabort soll die Messung der Zervixlänge, dies wegen der hohen Detektionsrate an Zervixverkürzungen und der Möglichkeit einer Behandlung, bereits ab 16 SSW durchgeführt werden. Ebenso
wird bei Zwillingen eine routinemässige Zervixlängenmessung ab 16 SSW empfohlen (4, 5).
Vaginalabstriche
Das generelle Screening auf eine bakterielle Vaginose ist international weiterhin umstritten. Gemäss den Leitlinien der ACOG wird ein routinemässiger Vaginalabstrich, und auch bei St.n. FG oder Spätabort bzw. Zwilligsschwangerschaft nicht empfohlen, die Briten wiederum bieten grosszügig einen an (1, 4). Basierend darauf, dass mit einer Behandlung der bakteriellen Vaginose mit Clindamycin im frühen 2. Trimenon, eine signifikante Senkung der Frühgeburtlichkeit erreicht werden konnte (12), wird bei uns im klinischen Alltag, anlässlich der ersten Schwangerschaftskontrolle ein Gram-Präparat durchgeführt (13). Eine vor kurzem publizierte kontrolliert randomisierte Studie (PREMEVA-Trial) zeigte nun aber, dass ein Screening auf bakterielle Vaginose und eine allfällige Therapie mit Clindamycin bei Patientinnen mit niedrigem Risiko für FG weder die Rate an Spätaborten noch die frühen FG reduzieren konnte (14).
Zerklage/totaler Muttermundsve
In der Beratung von Frauen mit St.n. FG oder Spätabort kann eine prophylaktische Zerklage in Erwägung gezogen werden (5). Die Datenlage bzw. der Benefit gegenüber regelmässigen Ultraschallkontrollen und einem Eingreifen bei einer tatsächlichen Zervixverkürzung wird zurzeit noch kontrovers diskutiert. Bisher konnte kein Nachteil eines abwartenden Procederes vs. einer prophylaktischen Zerklage in Bezug auf die Prävalenz der FG oder der perinatalen Mortalität gezeigt werden (15). Diese Aspekte sind in der Beratung und Aufklärung für den Eingriff selbstverständlich zu berücksichtigen und die Entscheidung für oder gegen die prophylaktische Zerklage muss weiterhin individuell abgewogen werden. Der Eingriff sollte dann im frühen 2. Trimenon und falls erwünscht, nach abgeschlossener Pränataldiagnostik durchgeführt werden. Es gibt Hinweise, dass die zusätzliche Anlage eines TMMVs, mit dem Ziel das Uteruskavum vor dem Eindringen von Bakterien zu schützen, die Rate an FG reduzieren kann (16).
Eine prophylaktische Zerklage bei Zwillingsschwangerschaften ist nicht indiziert (4, 5).
Progesteron
Auch bezüglich einer prophylaktischen Progesterongabe findet sich eine heterogene Datenlage. In den meisten Guidelines wird jedoch empfohlen, bei St. n. FG oder Spätabort Progesteron (200-400mg/Tag vaginal oder oral) grosszügig anzubieten (4,5).
Für Zwillingsschwangerschaften gibt es keine Empfehlung für eine prophylaktische Gabe von Progesteron (4,5). Eine kürzlich veröffentlichte randomisierte Studie (EVENT-Study) untermauert diese Empfehlung für Zwillingschwangerschaften. Es konnte gezeigt werden, dass es zwischen den Gruppen mit Progesteron vs. Placebo keinen signifikanten Unterschied in der FG-rate gab (17). Entsprechend scheint die Gabe von Progesteron, wenn überhaupt, dann nur einen kleinen Stellenwert in der primären Prävention von Frühgeburtlichkeit zu haben.
Sekundäre Prävention
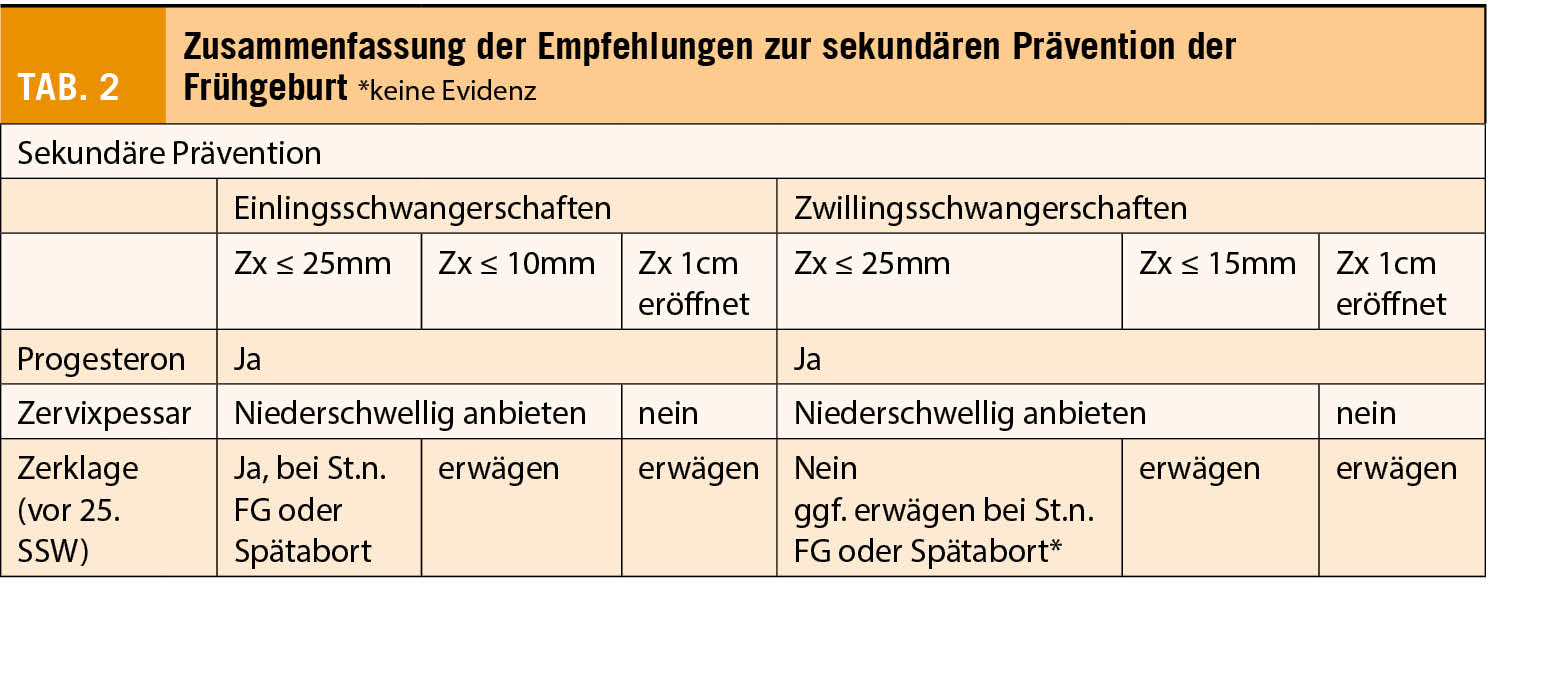
Die sekundäre Prävention bezieht sich auf Massnahmen bzw. Therapien, die bei Frauen mit asymptomatischer Zervixverkürzung, d.h. ohne Kontraktionen oder vorzeitigem Blasensprung, angewandt werden können. Auch hier wird, wenn nötig, zwischen Einlings- und Zwillingsschwangerschaften unterschieden. Tabelle 2 fasst die Empfehlungen der sekundären Prävention zusammen.Sekundäre Prävention.
Progesteron
Diverse Studien konnten für Einlingsschwangerschaften mit einer asymptomatischen Zervixverkürzung ≤ 25mm vor der 25. SSW zeigen, dass mit der Gabe von Progesteron vaginal im Vergleich zu Placebo eine signifikante Reduktion der FG-rate ≤ 34 SSW und der neonatalen Morbidität erreicht werden kann (18, 19).
Obwohl die Datenlage für die Progesterongabe bei Zwillingsschwangerschaften mit Zervixverkürzung etwas schwächer ist, wird die Gabe von Progesteron (200-400mg/Tag vaginal oder oral) in den Leitlinien der schweizerisch/deutschen und österreichischen Fachgesellschaft (SGGG/DGGG/ÖGGG) empfohlen (5).
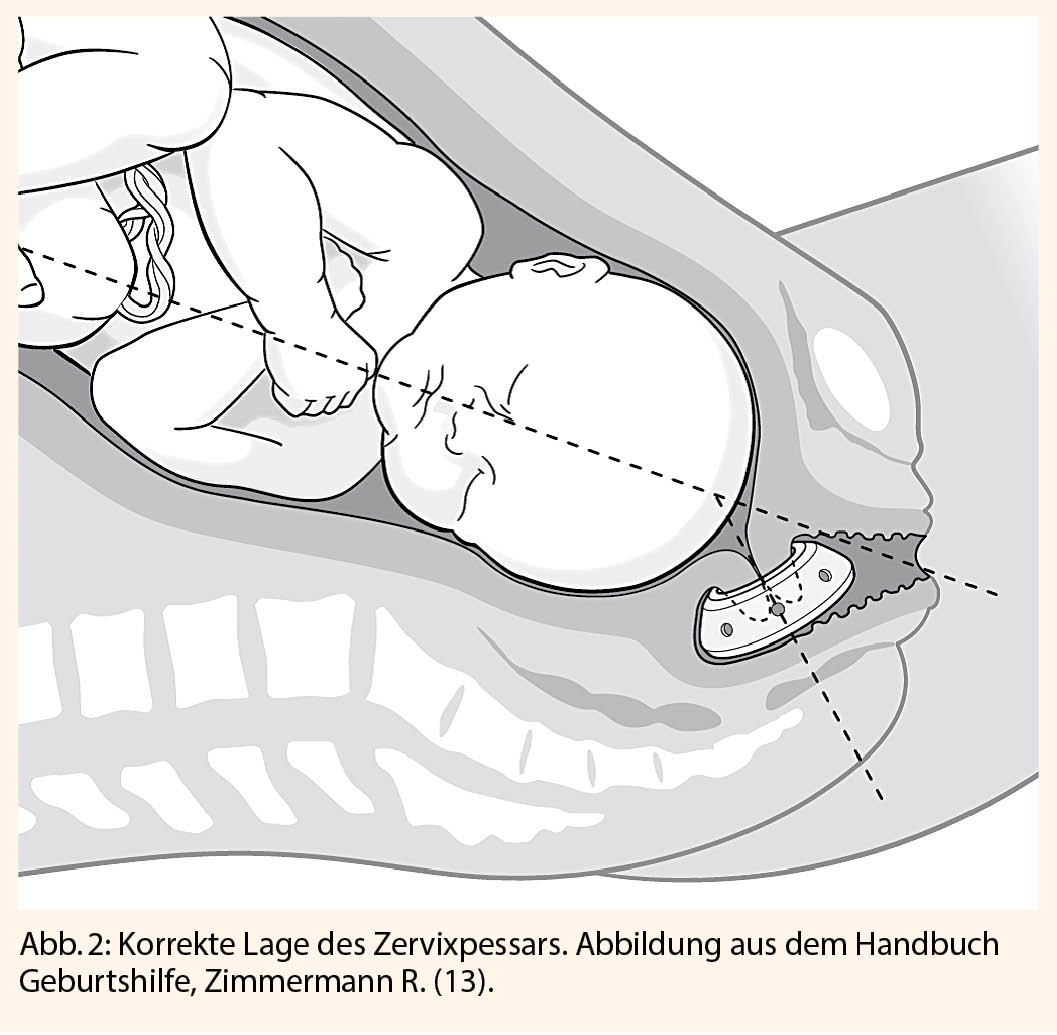
Zervixpessar
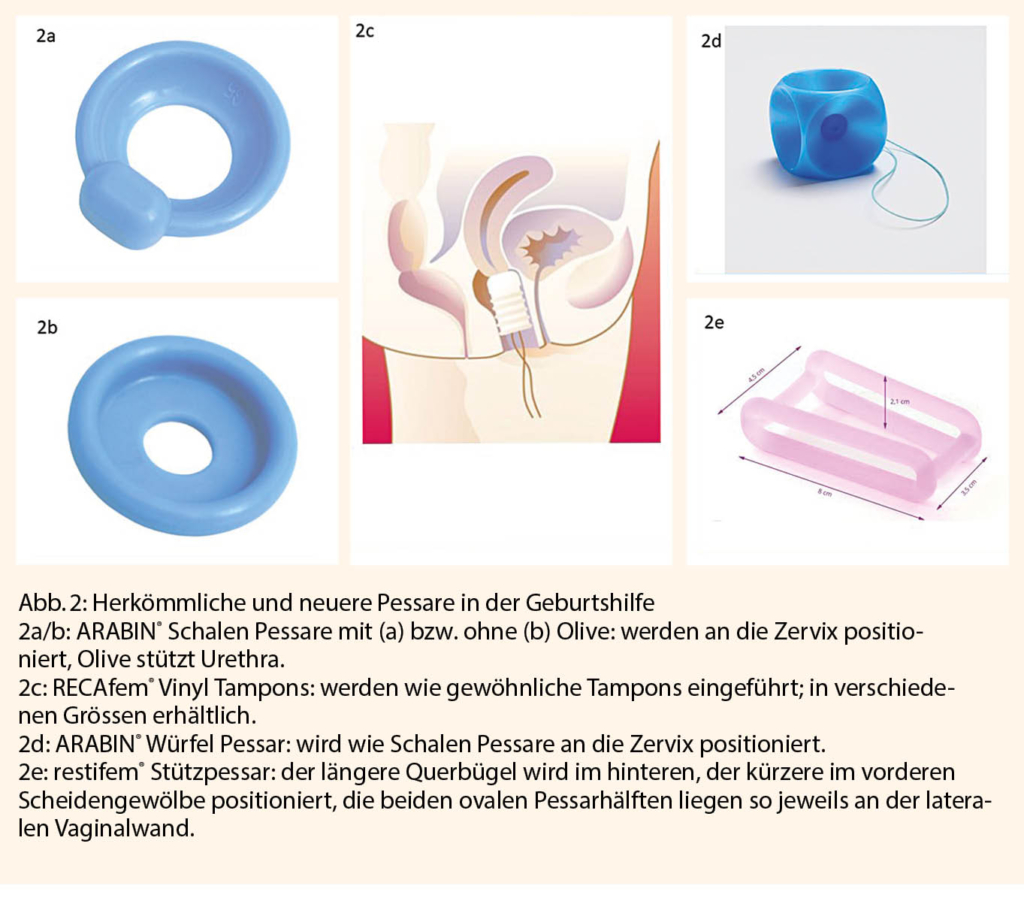
Ziel des Zervixpessars ist es, einerseits der Zervix zu stabilisieren und andererseits, durch die konkave Passform, den Druck auf diese zu verringern (Abb 2). In der Literatur finden sich unterschiedliche Resultate bezüglich des Nutzens des Zervixpessars bei einem CK ≤ 25mm (20, 21). In den Empfehlungen der ACOG wird generell eher von der Einlage eines Zervixpessars abgeraten (4). Wichtig ist, dass ein Zervixpessar nur am wehenfreien Uterus eingesetzt wird. Da die Einlage des Pessars, abgesehen von vermehrtem Ausfluss, ein sehr komplikationsarmer Eingriff ist, wird dieser bei uns mit gegebener Indikation vor der 32. SSW niederschwellig angeboten (5, 13).
Vaginalsonographische Kontrollen der Zervixlänge bei liegendem Pessar sind nicht indiziert (4). Beklagt die Patientin ein Fremdkörpergefühl wird, die Lage des Pessars manuell kontrolliert und bei Bedarf reponiert.
Die obigen Überlegungen und Empfehlungen gelten auch für Zwillingsschwangerschaften (5, 13).
Zerklage
Bei der therapeutischen Zerklage zur sekundären Prävention der FG wird zwischen der Ultraschall-indizierten (auch therapeutische Zerklage), bei sonographisch verkürzter Zervix, und der klinisch-indizierten Zerklage (auch Notfallzerklage), bei bereits sichtbarer und ggf. prolabierender Fruchtblase unterschieden.
In den Leitlinien der ACOG und der SGGG/DGGG/ÖGGG sind die Empfehlungen zur therapeutischen Zerklage mit grosser Vorsicht formuliert und betonen stets die fallbezogene Abwägung der Indikation (4, 5). Die Empfehlungen basieren auf den Resultaten folgender Studien:
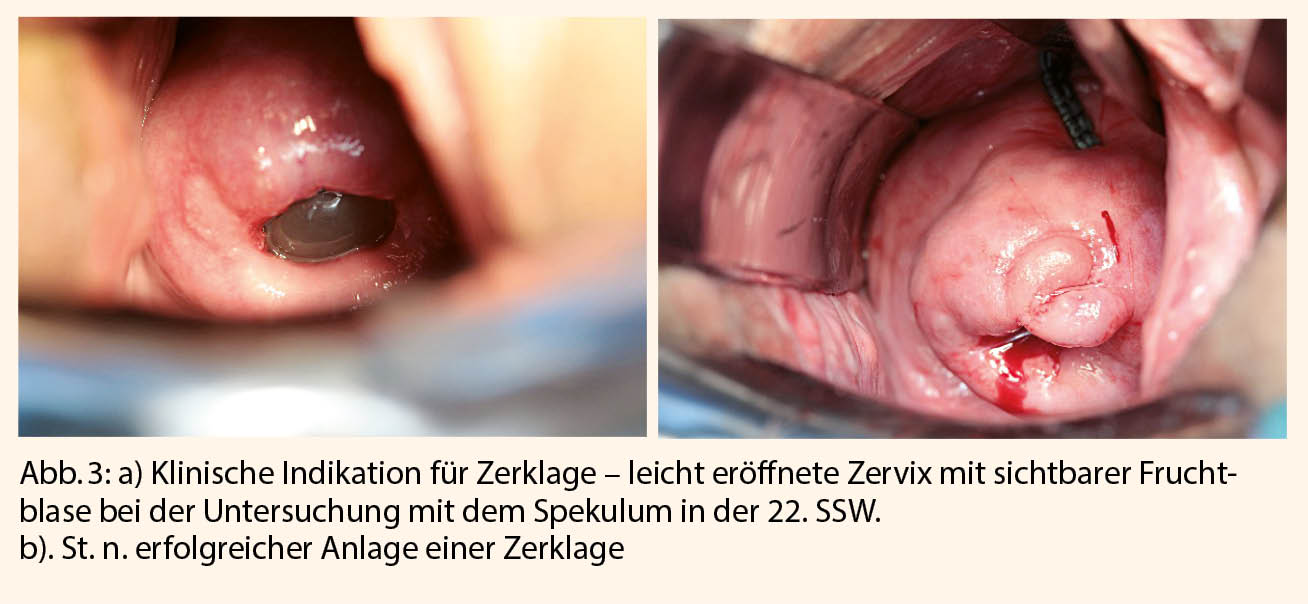
Beghella et al. konnte für Einlingsschwangerschaften ohne Vorgeschichte zeigen, dass ein möglicher Nutzen einer Ultraschall-indizierten Zerklage vor der 25. SSW erst ab einer Zervixverkürzung ≤ 10mm vorliegt (22). Der Benefit einer Zerklage bei klinischer Indikation wurde in einer 2015 publizierten Metaanalyse untersucht und fand eine signifikante Verlängerung der Schwangerschaft (+ 5.4 SSW) sowie eine ca. 50% Reduktion der perinatalen Mortalität von ca. 60 auf 30% (23). Abbildungen 3a und b illustrieren einen Fall vor und nach klilnisch-indizierter Zerklage in der 22. SSW.
Die beste Evidenz für den Nutzen der therapeutischen Zerklage liegt für Fälle mit St.n. FG und Zervix ≤ 25mm vor. Mehrere Metaanalysen zeigen einen signifikanten Vorteil der Zerklage gegenüber Bettruhe zur Reduktion der FG vor 34 SSW (p < 0.02) sowie eine Reduktion der perinatalen Mortalität und Morbidität (24, 25).
Eine aus 2019 stammende Metaanalyse postuliert, dass die Zerklage bei Zwillingschwangerschaften mit einer Zervixverkürzung < 15mm zu einer 6-8 wöchigen Verlängerung der Schwangerschaft führt (26). Eine im Jahre 2020 publizierte randomisiert kontrollierte Studie konnte den Nutzen der klinisch indizierten Zerklage bei Zwillingen zeigen, wonach diese mit einem signifikant höheren GA bei Geburt und einer geringeren neonatalen Morbidität und Mortalität einhergeht (27).
In den Leitlinien wird zudem die prophylaktische peri-operative Gabe von Antibiotika sowie die Gabe von Indometacin empfohlen (4, 5). Unklar bleibt die Rolle einer therapeutischen Antibiotikatherapie in Hinblick auf den Benefit der neonatalen Morbidität und Mortalität sowie die Indikation einer präinterventionellen Amniocentese zum Ausschluss einer bereits manifesten intrauterinen Infektion. Bezüglich des Nutzens eines TMMV bei Verkürzung der Zervix auf unter 15 mm stehen bis heute keine randomisiert, kontrollierten Studien zur Verfügung.
Copyright bei Aerzteverlag medinfo AG
Klinik für Geburtshilfe
UniversitätsSpital Zürich
Frauenklinikstrasse 10
8091 Zürich
ladina.vonzun@usz.ch
Klinik für Geburtshilfe
UniversitätsSpital Zürich
Frauenklinikstrasse 10
8091 Zürich
Die Autorinnen haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Medley N, Poljak B, Mammarella S, Alfirevic Z. Clinical guidelines for prevention and management of preterm birth: a systematic review. BJOG. 2018;125(11):136.
2. Chawanpaiboon S, Vogel JP, Moller AB, Lumbiganon P, Petzold M, Hogan D, et al. Global, regional, and national estimates of levels of preterm birth in 2014: a systematic review and modelling analysis. Lancet Glob Health. 2019;7(1):e37-e46.
3. Neugeborenen. Bundesamt für Statistik Schweiz. Online: https://www.bfs.admin.ch/bfs/de/home/statistiken/gesundheit/gesundheitszustand/gesundheit-neugeborenen.html; Stand 30.08.2021.
4. American College of O, Gynecologists‘ Committee on Practice B-O. Prediction and Prevention of Spontaneous Preterm Birth: ACOG Practice Bulletin, Number 234. Obstet Gynecol. 2021;138(2):e65-e90.
5. Leitline der SGGG/DGGG/ÖGGG. Prävention und Therapie der Frühbegurt(S2k-Niveau, AWMF-Resisternummer 015/025, Februar 2019,Überprüft am 18.08.2021) – Teil 1 mit Empfehlung zur Epidemiologie, Äthiologie, Prädiktion, primären und sekundären Prävention der Frühgeburt.
6. Schummers L, Hutcheon JA, Hernandez-Diaz S, Williams PL, Hacker MR, VanderWeele TJ, et al. Association of Short Interpregnancy Interval With Pregnancy Outcomes According to Maternal Age. JAMA Intern Med. 2018;178(12):1661-70.
7. Goodfellow L, Care A, Alfirevic Z. Controversies in the prevention of spontaneous preterm birth in asymptomatic women: an evidence summary and expert opinion. BJOG. 2021;128(2):177-94.
8. Phillips C, Velji Z, Hanly C, Metcalfe A. Risk of recurrent spontaneous preterm birth: a systematic review and meta-analysis. BMJ Open. 2017;7(6):e015402.
9. Schweizerische Gesellschaft für Ultrsaschall in der Medizin SGuG. Emfpehlungen zur Ultraschalluntersuchung in der Schwangerschaft. 2019.
10. Friedman AM, Schwartz N, Ludmir J, Parry S, Bastek JA, Sehdev HM. Can transabdominal ultrasound identify women at high risk for short cervical length? Acta Obstet Gynecol Scand. 2013;92(6):637-41.
11. Iams JD, Goldenberg RL, Meis PJ, Mercer BM, Moawad A, Das A, et al. The length of the cervix and the risk of spontaneous premature delivery. National Institute of Child Health and Human Development Maternal Fetal Medicine Unit Network. N Engl J Med. 1996;334(9):567-72.
12. Ugwumadu A, Manyonda I, Reid F, Hay P. Effect of early oral clindamycin on late miscarriage and preterm delivery in asymptomatic women with abnormal vaginal flora and bacterial vaginosis: a randomised controlled trial. Lancet. 2003;361(9362):983-8.
13. Zimmerman R. Hanbuch Geburtshilfe. Eigenverlag. Verein zur Förderung der Spitzenmedizin in der Geburtshilfe Zürich. 2018.
14. Subtil D, Brabant G, Tilloy E, Devos P, Canis F, Fruchart A, et al. Early clindamycin for bacterial vaginosis in pregnancy (PREMEVA): a multicentre, double-blind, randomised controlled trial. Lancet. 2018;392(10160):2171-9.
15. Berghella V, Mackeen AD. Cervical length screening with ultrasound-indicated cerclage compared with history-indicated cerclage for prevention of preterm birth: a meta-analysis. Obstet Gynecol. 2011;118(1):148-55.
16. Saling E, Schumacher E. (Total surgical cervical occlusion. Conclusions from data of several clinica, which use total surgical cervical occlusion). Z Geburtshilfe Neonatol. 1996;200(3):82-7.
17. Rehal A, Benko Z, De Paco Matallana C, Syngelaki A, Janga D, Cicero S, et al. Early vaginal progesterone versus placebo in twin pregnancies for the prevention of spontaneous preterm birth: a randomized, double-blind trial. Am J Obstet Gynecol. 2021;224(1):86 e1- e19.
18. Norman JE, Marlow N, Messow CM, Shennan A, Bennett PR, Thornton S, et al. Vaginal progesterone prophylaxis for preterm birth (the OPPTIMUM study): a multicentre, randomised, double-blind trial. Lancet. 2016;387(10033):2106-16.
19. Romero R, Conde-Agudelo A, Da Fonseca E, O’Brien JM, Cetingoz E, Creasy GW, et al. Vaginal progesterone for preventing preterm birth and adverse perinatal outcomes in singleton gestations with a short cervix: a meta-analysis of individual patient data. Am J Obstet Gynecol. 2018;218(2):161-80.
20. Saccone G, Maruotti GM, Giudicepietro A, Martinelli P, Italian Preterm Birth Prevention Working G. Effect of Cervical Pessary on Spontaneous Preterm Birth in Women With Singleton Pregnancies and Short Cervical Length: A Randomized Clinical Trial. JAMA. 2017;318(23):2317-24.
21. Conde-Agudelo A, Romero R, Nicolaides KH. Cervical pessary to prevent preterm birth in asymptomatic high-risk women: a systematic review and meta-analysis. Am J Obstet Gynecol. 2020;223(1):42-65 e2.
22. Berghella V, Ciardulli A, Rust OA, To M, Otsuki K, Althuisius S, et al. Cerclage for sonographic short cervix in singleton gestations without prior spontaneous preterm birth: systematic review and meta-analysis of randomized controlled trials using individual patient-level data. Ultrasound Obstet Gynecol. 2017;50(5):569-77.
23. Ehsanipoor RM, Seligman NS, Saccone G, Szymanski LM, Wissinger C, Werner EF, et al. Physical Examination-Indicated Cerclage: A Systematic Review and Meta-analysis. Obstet Gynecol. 2015;126(1):125-35.
24. Althuisius SM, Dekker GA, Hummel P, van Geijn HP, Cervical incompetence prevention randomized cerclage t. Cervical incompetence prevention randomized cerclage trial: emergency cerclage with bed rest versus bed rest alone. Am J Obstet Gynecol. 2003;189(4):907-10.
25. Berghella V, Odibo AO, To MS, Rust OA, Althuisius SM. Cerclage for short cervix on ultrasonography: meta-analysis of trials using individual patient-level data. Obstet Gynecol. 2005;106(1):181-9.
26. Li C, Shen J, Hua K. Cerclage for women with twin pregnancies: a systematic review and metaanalysis. Am J Obstet Gynecol. 2019;220(6):543-57 e1.
27. Roman A, Zork N, Haeri S, Schoen CN, Saccone G, Colihan S, et al. Physical examination-indicated cerclage in twin pregnancy: a randomized controlled trial. Am J Obstet Gynecol. 2020;223(6):902 e1- e11