Der phobische Schwindel, heute zunehmend im Sinne des «persistierenden postural-perzeptiven Schwindels» (engl. PPPD) indiziert, stellt eine funktionelle Schwindelform ohne primär organisch fassbare Ursache dar. Für Patient/-innen ist er häufig mit erheblichem Leidensdruck verbunden. Die Symptomatik liegt an der Schnittstelle von somatischer und psychischer Medizin, gekennzeichnet durch eine Störung der visuell-vestibulär-emotionalen Netzwerke, und weist eine hohe Komorbidität mit Angsterkrankungen und depressiven Störungen auf (1). Der Beitrag beleuchtet die historische Entwicklung, das klinische Erscheinungsbild sowie diagnostische und therapeutische Strategien mit besonderem Augenmerk auf evidenzbasierte kognitiv-verhaltenstherapeutische Ansätze und edukative Interventionen.
Phobic dizziness, also known as functional or somatoform dizziness, is a common and distressing condition that often lacks an identifiable organic cause. It poses a diagnostic and therapeutic challenge because of overlapping somatic, vestibular, and psychiatric factors. This article provides a historical context, describes the clinical picture, and outlines the current diagnostic approaches. Special focus is given to interdisciplinary collaboration and evidence-based treatment options, particularly cognitive behavioral therapy. The article concludes with a set of practice-relevant take-home messages for general practitioners.
Keywords: Phobischer Schwindel, persistierender postural-perzeptiver Schwindel, kognitive Verhaltenstherapie, interdisziplinäre Therapieansätze
Einleitung und historischer Überblick
Der Begriff «phobischer Schwindel» wird erstmals als Syndrom von Brandt und Dieterich 1986 beschrieben (2) und äussert sich durch attackenartig auftretenden Schwindel mit subjektiven Gleichgewichtsstörungen im Stand und beim Gehen. Seit den 1990er-Jahren ist der Begriff «phobischer posturaler Schwindel» (engl. phobic postural vertigo, PPV) systematisch verwendet worden, um eine häufige, nicht organische Form anhaltender Schwindelsymptomatik zu beschreiben, die sich von Schwindelsymptomen im Rahmen von psychischen Erkrankungen, wie beispielsweise der Agoraphobie und der Panikstörung, unterscheidet. Zudem konnte in Follow-up-Studien bei PPV ein Therapieansprechen unter anderem auf Psychotherapie, Pharmakotherapie und Physiotherapie beobachtet werden (3). Mit zunehmendem Verständnis für psychosomatische Erkrankungen wurde der phobische Schwindel bzw. PPV als funktionelle Störung mit hoher Krankheitslast eingeordnet, die in vielen Fällen zu einer Einschränkung im Alltags- und Berufsleben führen kann und einer multimodalen Therapie bedarf.
Aktuelle Klassifikationen, insbesondere das ICD-11 und die Konsensusdefinition der Bárány Society, fassen den PPV und verwandte Krankheitsbilder zunehmend unter dem Begriff «Persistent Postural-Perceptual Dizziness (PPPD)» zusammen (4). Dieses Syndrom betont die funktionellen, häufig chronifizierten und durch psychische Belastung verstärkten Symptome (5).
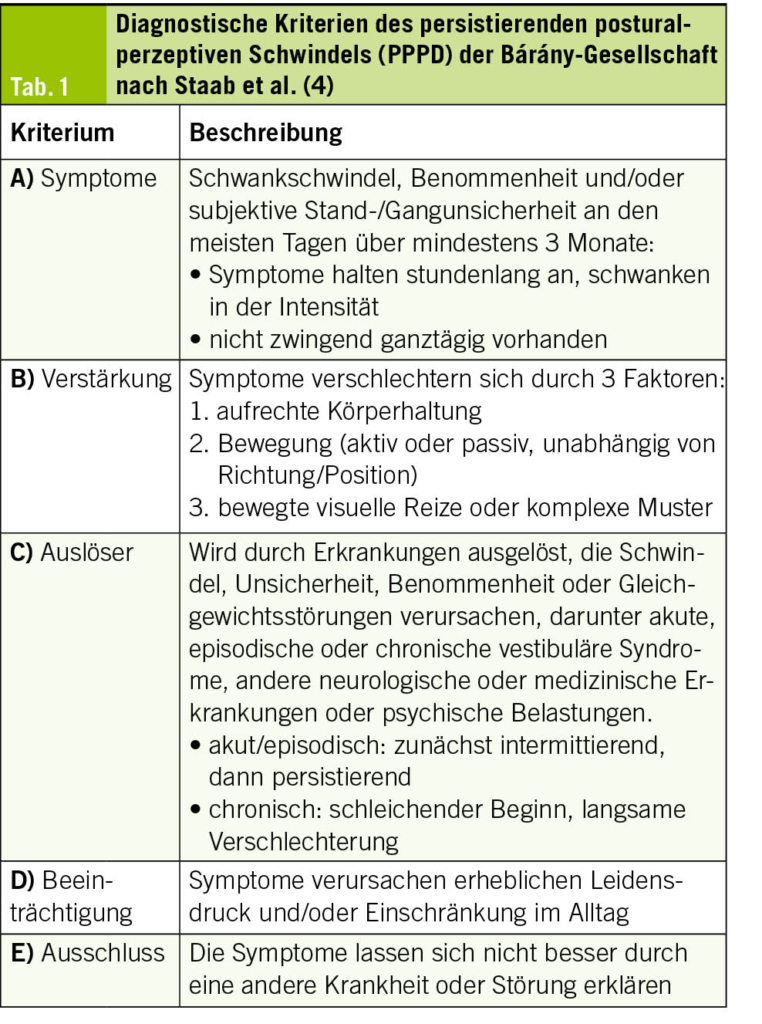
Für eine gesicherte Diagnose müssen alle fünf Kriterien (A–E) erfüllt sein (Tab. 1).
Der phobische Schwindel äussert sich typischerweise durch diffuse, anhaltende oder episodische Schwindelgefühle, meist als «Schwanken» oder «Benommenheit» beschrieben. Es kann zu einer dauerhaften Stand- und Gangunsicherheit führen, die häufig von Angst und Gefühlen der Hilflosigkeit begleitet wird. Die Symptomatik kann durch Erkrankungen ausgelöst werden, die das Gleichgewicht stören oder Schwindel, Unsicherheit oder Benommenheit verursachen (vestibuläre, neurologische oder andere medizinische Erkrankungen, psychische Belastungen), und kann durch aufrechte Körperhaltung, visuelle Reize (Menschenmengen, Supermarktgänge) sowie aktive oder passive Bewegung verstärkt werden (4, 6). Anders als bei anderen vestibulären Erkrankungen, wie z. B. dem gutartigen Lagerungsschwindel oder dem M. Menière, besteht beim funktionellen Schwindel bzw. PPPD keine eigentliche Drehbewegung oder ein Drehschwindel, sondern ein Gefühl von Instabilität. Begleitet wird der Zustand häufig von vegetativen Symptomen wie Palpitationen, Schwitzen oder Engegefühl. Die organmedizinische Abklärung bleibt in der Regel unauffällig, doch in ca. 50 % der Fälle lassen sich psychiatrische Komorbiditäten wie Angst- oder depressive Störungen feststellen (1).
Differenzialdiagnostisch abzugrenzen sind:
• vestibuläre Migräne
• benigner paroxysmaler Lagerungsschwindel
• Vestibularisparoxysmie
• Angsterkrankungen (Panikstörung, Agoraphobie)
• Somatisierungsstörungen und depressive Episoden
Schwindel als interdisziplinäre Aufgabe
Die Versorgung von Patient/-innen mit phobischem Schwindel bzw. PPPD erfordert ein abgestimmtes Zusammenspiel mehrerer medizinischer Disziplinen. In der Regel erfolgt die Erstabklärung im hausärztlichen Bereich, wobei bei unklarer Symptomatik neurologische und/oder ORL-fachärztliche Untersuchungen folgen sollten. Liegt eine funktionelle Störung nahe, kann die gezielte Einbindung psychotherapeutischer Expertise entscheidend zur Verbesserung der Lebensqualität beitragen. Wie der Psychiater Michael Rufer betonte, ist die klassische Unterscheidung in «somatisch» vs. «psychogen» beim Schwindel heute obsolet (7). Vielmehr sollte von einem «Schwindelspektrum» gesprochen werden, bei dem zentrale (Neurologie), periphere (ORL) und psychogene (Psychiatrie) Anteile gleichzeitig oder nacheinander wirksam sein können. Weiter schlug er hierzu ein biopsychosoziales Modell vor, das individuelle somatische und psychische Krankheitsfaktoren integriert und den Betroffenen ein nachvollziehbares Krankheitskonzept anbietet (7).
Pathophysiologie und psychodynamische Aspekte
Beim phobischen Schwindel handelt es sich um ein multifaktorielles Geschehen. Zentrale Merkmale sind:
• Übererregung des vegetativen Nervensystems
• Hypervigilanz gegenüber Körpersymptomen
• Einschränkung der propriozeptiven Selbstregulation, übermässige posturale Kontrolle bei vermeintlich hohem Risiko, um Stürze zu vermeiden («walking on ice»)
• visuelle Dominanz
• Besserung der Symptome unter «dual task»-Bedingungen (8)
• Alexithymie (eingeschränkte Gefühlswahrnehmung)
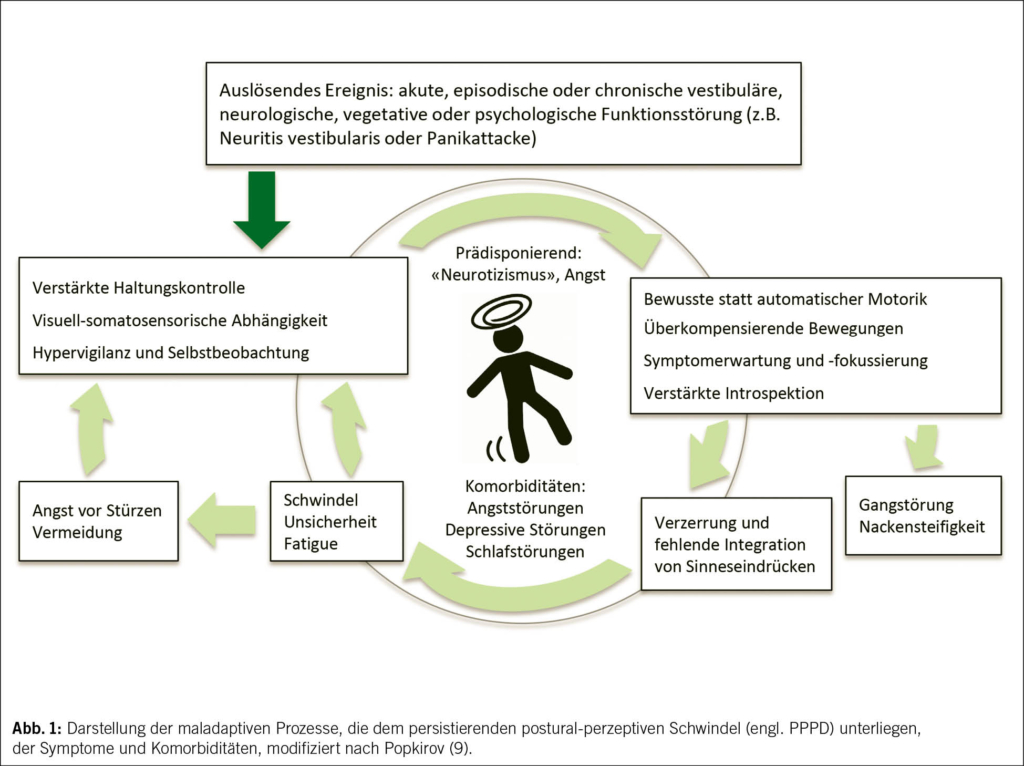
Der Schwindel fungiert dabei häufig als Angstäquivalent, insbesondere bei Patient/-innen mit inadäquater Gefühlsverarbeitung und einem erhöhten Kontrollbedürfnis. Exogene Trigger wie Stress, neue Lebenssituationen (z. B. Elternschaft, berufliche Verantwortung) oder unbewältigte Lebensereignisse (z. B. Todesfälle) spielen eine zentrale Rolle. Die fehlerhafte Verarbeitung von externen und internen Stimuli wird als sogenannte Maladaptation bezeichnet, die sich in Wechselwirkung mit körperlichen und psychischen Reaktionen in einem Teufelskreis von Verunsicherung und Schonverhalten manifestieren kann. Die Folgen können eine erhöhte Introspektionsfähigkeit, eine Fokussierung auf körperliche Signale bzw. Reaktionen und die Entwicklung einer ausgeprägten Vermeidung von körperlichen und sportlichen Aktivitäten sein (Abb. 1).
Diagnostik in der hausärztlichen Praxis
Die Diagnostik basiert auf einer klinischen Einschätzung mit strukturierter Anamnese (Verlauf, Trigger, Situationsbindung), ergänzt um eine neurologische Grunduntersuchung (inkl. z. B. Romberg-Test, Unterberger-Tretversuch, Halmagyi-Curthoys-Kopfimpulstest). Die Diagnostik beginnt mit der sorgfältigen Anamnese (körperlich, psychisch, sozial).
Relevante Fragen können sein:
• Wann, wie oft und wie tritt der Schwindel auf?
• Wie lange dauern die Schwindelepisoden?
• Bestehen typische Auslöser, Verstärker oder Begleitsymptome?
• Gab es organische Vorabklärungen?
• Liegen psychiatrische Komorbiditäten vor?
Im hausärztlichen Setting sind folgende Schritte zentral:
• Ausschluss einer gefährlichen somatischen Ursache (Red Flags!)
• Funktionsdiagnostische Hinweise:
– Keine persistierenden objektivierbaren vestibulären Ausfälle, PPPD kann jedoch auch zusätzlich bei einem funktionsdiagnostischen Defizit auftreten
– Stabiler Gang in gewohnter, Unsicherheit/Schwanken in ungewohnter Umgebung
• Orientierung an der ICD-10-Klassifikation für somatoforme oder Angststörungen bzw. an der ICD-11-Klassifikation für PPPD
• Falls unklar: Überweisung an einen neurootologischen Spezialisten (Neurologie oder ORL)
• Bei Hinweisen auf psychische Beschwerden und psychosoziale Belastungen: Indikation zur Psychotherapie prüfen
Zur Abgrenzung struktureller Ursachen werden phasengerechte apparative Untersuchungen empfohlen. Eine strukturierte Psychoedukation dient der Symptomvalidierung und ist bereits ein erster therapeutischer Schritt, welcher auch von den behandelnden somatischen Ärzt/-innen durchgeführt werden kann (5, 6).
Behandlung: multimodale und psychotherapeutische Strategien
1. Psychoedukation und Krankheitsmodell
Ein zentraler erster Schritt in der Behandlung besteht darin, den Patient/-innen ein verstehbares und zu akzeptierendes Krankheitsmodell zu vermitteln. Sie müssen nicht zwischen «körperlich» oder «psychisch» entscheiden, sondern lernen, beide Ebenen zu berücksichtigen. Dieses sollte verdeutlichen, dass die Beschwerden real und behandelbar sind, unabhängig davon, ob eine organische Ursache vorliegt. Schwindel kann auch ein körperlicher Ausdruck von Stress sein, weshalb der aktuelle persönliche Lebenskontext berücksichtigt werden sollte.
2. Kognitive Verhaltenstherapie (KVT)
KVT gilt als evidenzbasierte und effektive Therapiemethode, die folgende Elemente beinhalten sollte:
• Expositionen mit symptomprovozierenden Reizen
(z. B. Drehstuhl)
• Aufbau von emotionaler Wahrnehmung (Affektdifferenzierung)
• Rückfallprophylaxe durch Selbstbeobachtung und Stressbewältigung unter Berücksichtigung der individuellen Lebenssituation
Ziel ist es, angstverstärkende Bewertungsketten zu hinterfragen und adaptive Bewegungsmuster durch Expositionsübungen wiederherzustellen (1, 5).
4. Ergänzende Verfahren
• Vestibuläre Physiotherapie (Gleichgewichtstraining), ggf. mit visueller Desensibilisierung, Achtsamkeit und Entspannungsverfahren, Biofeedback, Gruppentherapie zur Förderung emotionaler Kompetenzen
Copyright
Aerzteverlag medinfo AG
Zweitabdruck aus «PRAXIS» 01/26
MBA, Oberärztin
Fachärztin für Psychiatrie und Psychotherapie
Universitätsspital Zürich
Klinik für Konsiliarpsychiatrie und Psychosomatik
Rämistrasse 100
8091 Zürich
Psychologin FSP
Universitätsspital Zürich
Klinik für Konsiliarpsychiatrie und Psychosomatik
Interdisziplinäres Zentrum für Schwindel und neurologische Sehstörungen
Rämistrasse 100
8091 Zürich
Die Autorinnen haben keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Dieterich, M., & Staab, J. P. (2017). Functional dizziness: from phobic postural vertigo and chronic subjective dizziness to persistent postural-perceptual dizziness. Current Opinion in Neurology, 30(1), 107-113.
2. Brandt, T, Dieterich, M. (1986). Phobischer Attacken-Schwankschwindel, ein neues Syndrom. Münchner Medizinische Wochenschrift, 128:247-250.
3. Brandt, T., Huppert, D. & Dieterich, M. (1994). Phobic postural vertigo: a first follow-up. Journal of Neurology, 241, 191-195.
4. Staab, J. P., Eckhardt-Henn, A., Horii, A., Jacob, R., Strupp, M., Brandt, T., & Bronstein, A. (2017). Diagnostic criteria for persistent postural-perceptual dizziness (PPPD): Consensus document of the committee for the classification of vestibular disorders of the Bárány Society. Journal of Vestibular Research: Equilibrium and Orientation, 27(4), 191-208.
5. Madrigal, J., Herrón-Arango, A.F., Bedoya, M.J., Cordero Chen, J., Castillo-Bustamante, M. (2024). Persistent Challenges: A Comprehensive Review of Persistent Postural-Perceptual Dizziness, Controversies, and Clinical Complexities. Cureus, 16(5):e60911.
6. Popkirov, S., Staab, J.P., & Stone, J. (2017). Persistent postural-perceptual dizziness (PPPD): a common, characteristic and treatable cause of chronic dizziness. Practical Neurology, 18, 13 – 5.
7. Rufer, M. (2011). Psychotherapie bei Schwindel: Erklärungsmodell und Fallbeispiel. Schweizer Archiv für Neurologie und Psychiatrie, 162(8):318-321.
8. Staab, J.P. (2023). Persistent Postural-Perceptual Dizziness: Review and Update on Key Mechanisms of the Most Common Functional Neuro-otologic Disorder. Neurologic Clinics 41(4):647-664.
9. Popkirov, S. (2024). Funktionelle neurologische Störungen: Erkennen, verstehen, behandeln (2. Aufl.). Springer Berlin.