Die ISCHEMIA Studie (1, 2) ist eine der relevantesten Studien der letzten Dekade was die Behandlung der chronischen Koronarsyndrome betrifft, und es ist wenig wahrscheinlich, dass vergleichbare Untersuchungen folgen werden. Insofern gilt es, die Ergebnisse kritisch zu beleuchten und im klinischen Alltag bestmöglich zu integrieren. Wir fassen die wichtigsten Studienelemente zusammen und diskutieren deren Einfluss auf die Abklärung und Therapie unserer Patienten mit koronarer Herzerkrankung (KHK).
Zusammenfassung der Studie
Die ISCHEMIA Studie (1, 2) hat Patienten mit stabiler KHK und mindestens moderater Ischämie gemäss einem nicht-invasiven Stresstest randomisiert zu initial Leitlinien-konformer medikamentöser Therapie (n=2591) oder einer Revaskulariation (n=2588) mit entweder perkutaner Koronarintervention (PCI) (74%) oder aortokoronarer Bypass (ACB) Operation (26%) zusätzlich zur medikamentösen Therapie. Während einer Beobachtungsdauer von im Median 3.2 Jahren, zeigte sich kein signifikanter Unterschied zwischen den Therapiestrategien in Bezug auf den primären Endpunkt kardiovaskuläre Mortalität, Myokardinfarkt, Hospitalisation für instabile Angina pectoris oder Herzinsuffizienz, überlebter plötzlicher Herztod (invasiv 16.4% versus konservativ 18.2%, HR=0.93, CI 0.80-1.08, p=0.34) oder den sekundären Endpunkt kardiale Mortalität oder Myokardinfarkt (invasiv 14.2% versus konservativ 16.5%, HR=0.90, CI 0.77-1.06, p=0.21). Die invasive Strategie zeigte jedoch eine deutliche Überlegenheit in Bezug auf die Lebensqualität, Häufigkeit von Angina pectoris und der körperlichen Belastbarkeit bei symptomatischen Patienten, welche unmittelbar nach dem Eingriff verzeichnet wurde und im Verlauf aufrechterhalten wurde.
Studiendesign
- Randomisiert, unverblindet, parallel
- Anzahl Patienten: 5179
- Beobachtungsdauer: bis 5 Jahre (median 3.2 Jahre)
- Patienten mit Verdacht auf KHK wurden mit einem nicht-invasiven Stresstest untersucht. Bei Bestätigung einer moderaten bis schweren Ischämie erfolgte eine koronare Computertomographie-Angiographie (CCTA) zum Ausschluss einer relevanten Hauptstammstenose und Bestätigung mindestens einer signifikanten Koronarstenose.
- Primärer Endpunkt aufgrund langsamer Rekrutierung von initial kardiovaskulärer Mortalität und Myokardinfarkt erweitert auf zusätzlich Hospitalisation für instabile Angina pectoris oder Herzinsuffizienz, und überlebter plötzlicher Herztod
- Konservativer Therapiearm (n=2591): initial Leitlinien-basierte medikamentöse Therapie, falls nicht erfolgreich Cross-Over zu Revaskularisation mit PCI oder ACB-Operation
- Invasiver Therapiearm (n=2588): Revaskularisation mit PCI (74%) oder ACB-Operation (26%)
Einschlusskriterien
- >20 Jahre alt
- Moderate bis schwere Ischämie gemäss einem nicht-invasiven Stresstest (nuklear (49.6%): ≥10% Ischämie, Stressechokardiographie (20.9%): ≥3 Segmente mit Ischämie, Magnetresonanz-tomographie (MRT) (5%): ≥12% Ischämie und/oder ≥3 Segmente mit Ischämie, Ergometrie (24.5%): ≥1.5mm ST Senkung in ≥2 Ableitungen oder ≥2mm ST Senkung in 1 Ableitung bei <7 METs mit Angina)
Ausschlusskriterien
- ≥50% Hauptstammstenose gemäss CCTA
- Fortgeschrittene chronische Niereninsuffizienz (glomeruläre Filtrationsrate (GFR) <30 ml/min)
- Myokardinfarkt innerhalb der letzten 2 Monate
- Linksventrikuläre Ejektionsfraktion <35%
- Inakzeptable Angina Symptome bei Studienbeginn
- New York Heart Association (NYHA) Klasse III-IV Herzinsuffizienz
- PCI oder ACB-Operation im Jahr vor Randomisierung
Studienpopulation
- Mittleres Patientenalter: 64 Jahre
- Frauen: 23%
- Diabetes: 41%
- Mediane linksventrikuläre Ejektionsfraktion: 60%
- Angina Häufigkeit bei Studienbeginn: keine Angina 35%, mehrmals pro Monat 44%, täglich/wöchentlich 20%
Crossover
- Koronarangiographie: 96% in der invasiven Gruppe und 28% in der medikamentösen Gruppe
- Revaskularisation: 79% in der invasiven Gruppe, 23% in der medikamentösen Gruppe
Hauptresultate
- Stresstest zur Detektion der Ischämie: nuklear 49.6%, Stressechokardiographie 20.9%, MRT 5%, Ergometrie 24.5%
- Primärer Endpunkt (kardiovaskuläre Mortalität, Myokardinfarkt, Hospitalisation für instabile Angina pectoris oder Herzinsuffizienz, überlebter plötzlicher Herztod): invasiv 16.4% versus konservativ 18.2%, HR=0.93, CI 0.80-1.08, p=0.34
- Sekundärer Endpunkt (kardiale Mortalität oder Myokardinfarkt): invasiv 14.2% versus konservativ 16.5%, HR=0.90, CI 0.77-1.06, p=0.21
- Gesamtmortalität: invasiv 9% versus konservativ 8.3%, HR=1.05, 95% CI 0.83-1.32, p=0.67
- Peri-prozedurale Myokardinfarkte: invasiv versus konservativ HR=2.98, 95% CI 1.87-4.74, p<0.01
- Spontane Myokardinfarkte: invasiv versus konservativ HR=0.67, 95% CI 0.53-0.83, p<0.01
- Lebensqualität (höherer Score = höhere Lebensqualität): Seattle Angina Questionnaire (SAQ) summary Score (=Lebensqualität, Häufigkeit von Angina, körperliche Einschränkungen) Differenz invasiv minus konservativ 4.1 Punkte (95% Kredibilitätsinterval (KI) 3.2-5.0) nach 3 Monaten, 4.2 Punkte (95% KI 3.3-5.1) nach 12 Monaten, 2.9 Punkte (95% KI 2.2-3.7) nach 36 Monaten
- Keine signifikante Interaktion zwischen anatomischen Schweregrad, Schweregrad der Ischämie, oder Ramus interventricularis anterior (RIVA) und den 2 Therapiestrategien, aber ein Trend für besseres Outcome mit der invasiven Strategie
Integration in den klinischen Alltag
Für wen gilt ISCHEMIA ?
Für die Anwendung der Studienergebnisse in der Praxis sollte bestmöglich verstanden werden, welche KHK Patienten in ISCHEMIA eingeschlossen wurden. Dies ist leicht nachzuvollziehen anhand der Ausschlusskriterien (siehe oben), welche auf einen beachtlichen Anteil der Patienten in der klinischen Routine zutreffen. Von den «offiziell» geprüften Patienten in ISCHEMIA wurden 78% aufgrund diverser Ausschlusskriterien nicht berücksichtigt (1, Appendix). Im Berner PCI Register erfüllen von 20’ 000 registrierten Patienten 67% der Patienten die drei einfach zu prüfenden Ausschlusskriterien ACS, Hauptstammstenose und LVEF <35% und kämen somit nicht für den Studieneinschluss in Frage (Daten beim Autor). Eine italienische Studie hat erhoben, dass von 5070 Patienten, die in einem Register für chronisches Koronarsyndrom (START) eingeschlossen wurden, 84,7% die Einschlusskriterien nicht erfüllten. Allerdings konnte der Schweregrad der Ischämie gemäss Stresstest in diesem Register nicht erhoben werden (in ISCHEMIA moderate bis schwere Ischämie) (3). Wichtig ist weiter ein detaillierter Blick auf die Angina pectoris Kriterien, um potentiell schwerwiegende Ereignisse durch ein initial konservatives Vorgehen zu vermeiden. Nicht in ISCHEMIA berücksichtigt wurden Patienten mit Angina (Canadian Cardiovascular Society) CCS III und IV oder Angina pectoris jeglicher Klasse, die sich rasch verschlechtert oder zunimmt. Während Angina CCS IV (Ruheangina) beim stabilen chronischen Koronarsyndrom selten ist, ist die Angina CCS Klasse III häufiger. Diese ist definiert durch das Auftreten von Beschwerden bereits nach cirka 200 Metern Gehstrecke in der Ebene («2 Blocks») oder dem Hochsteigen eines Stockwerkes. Solche Patienten sollen unverändert nach Echokardiographie direkt zur Koronarangiographie zugewiesen werden. Viel schwieriger einzuordnen ist die erhebliche und nicht dokumentierte Patientenselektion in ISCHEMIA. Es ist offensichtlich, dass eine Vielzahl von KHK Patienten nicht einer detaillierten Prüfung unterzogen wurden, wohl auch, weil die behandelnden Ärzte eine Studienteilnahme als zu gefährlich beurteilten und ihren Patienten eine Randomisierung nicht zumuten wollten. Nur etwa 3 Patienten pro Jahr und Studienzentrum (!) wurden eingeschlossen (5179 Patienten über 6 Jahre an 320 Studienzentren). Daraus ergibt sich, dass die Studienresultate keinesfalls in dogmatischer Weise wegweisend sein dürfen für alle «ISCHEMIA-like» Patienten im Bewusstsein, dass ein massgeblicher, nicht dokumentierter Selektionsprozess ablief und die externe Validität eingeschränkt ist. Die Beurteilung des erfahrene Kardiologen/innen unter Berücksichtigung aller Aspekte bleibt somit ein unverzichtbares Element in der KHK Abklärung.
KHK Abklärung gemäss ISCHEMIA
Obwohl die ISCHEMIA Studie nicht darauf angelegt war, den optimalen Abklärungsalgorithmus für die KHK zu untersuchen, und das klinische Outcome sowohl nach funktioneller als auch anatomischer KHK Abklärung gleichwertig ist (4), wird das Design der ISCHEMIA Studie unweigerlich einen Einfluss auf die zukünftigen Abklärungspfade haben.
Echokardiographie Der Ausschluss einer relevanten Valvulopathie oder einer eingeschränkten linksventrikulären Ejektionsfraktion (LVEF) mittels fachärztlich durchgeführter Echokardiographie steht am Anfang jeder KHK Abklärung. Entsprechend ist dies in den Richtlinien für das chronische Koronarsyndrom vorgesehen (Klasse IB) (5).
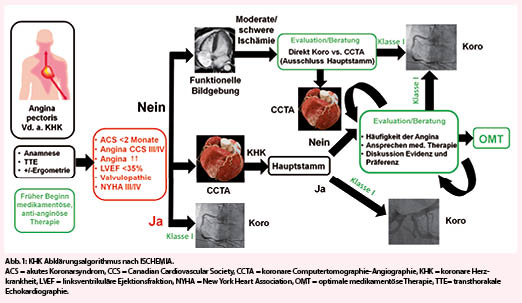
Anatomische KHK Tests Zweifelsohne stärkt die ISCHEMIA Studie die Rolle der CCTA wie vermutlich keine Studie zuvor und wird deren Rolle im Abklärungspfad der KHK festigen (Abbildung 1). Dies aus zwei Gründen: erstens muss zwingend eine Hauptstammstenose ≥50% ausgeschlossen werden, um ein initial konservatives Vorgehen gemäss ISCHEMIA rechtfertigen zu können, was mit funktionellen Stresstests nicht verlässlich möglich ist. Zweitens hatten etwa 20% der Patienten mit nachgewiesener moderater bis schwerer Ischämie keine nachweisbare obstruktive KHK (diese Patienten wurden nicht randomisiert), was die Bedeutung des anatomischen Ausschlusses einer obstruktiven KHK unterstreicht. Im Zusammenhang mit dem zukünftig vermehrten Einsatz der CCTA sollte daran gedacht werden, dass gemäss Leitlinien vor allem bei geringer bis mittlerer Vortest-Wahrscheinlichkeit eine hohe Aussagekraft hat und die Technik bei folgenden Patienten aus Qualitäts- oder Sicherheitsgründen nicht empfohlen ist: Kontraindikation für Nitroglycerin, Vorhofflimmern, Herzfrequenz nicht <70/min senkbar, Adipositas BMI >35kg/m2, bereits implantierte Stents, und GFR<30ml/min. In solchen Fällen ist einem nicht-invasiven Stresstest oder direkt der Koronarangiographie der Vorzug zu geben.
Funktionelle Stresstests Überraschend gab es in ISCHEMIA keinen signifikanten Zusammenhang zwischen dem Schweregrad der myokardialen Ischämie und Mortalität (p trend=0.33) und nur eine schwache Assoziation zwischen dem Grad der Ischämie und zukünftigen Myokardinfarkten (p for trend=0.04). Demgegenüber steht eine eindeutige Assoziation zwischen der anatomischen Komplexität (arteriosklerotische «Krankheitslast») und Mortalität wie auch Myokardinfarkt (p for trend für beide Endpunkte <0.001). Dies unterstreicht die Relevanz der anatomischen Bildgebung, ist aber auch ein Steilpass für die CCTA, vermehrt quantitative Aspekte über den Stenosegrad hinaus zu erheben. Es ist aber zu früh, das seit Dekaden manifeste Konzept der Ischämie zu verwerfen. Grössere Beobachtungsstudien (6, 7) weisen auf eine deutliche Assoziation zwischen Ischämie und Prognose hin und dienten als Basis für die bisherigen Leitlinien. Auch in diesem Kontext ist zu betonen, dass die im Median 3.2-jährige Beobachtungszeit für eine lebenslange, teils progrediente Erkrankung und einer Lebenserwartung von >20 Jahren nach der initialen KHK Abklärung (ISCHEMIA medianes Alter 64 Jahre) zu kurz ist. In diesem Zusammenhang wird es wichtig sein, die bereits signifikanten Unterschiede zugunsten der Revaskularisation im Hinblick auf spontane Myokardinfarkte im Langzeitverlauf zu verfolgen. Dass eine bestehende Koronarischämie bei betablockierten mehrheitlich sportlich nicht aktiven Patienten keine Arrhythmien zur Folge hat, mag sein. Wie sicher ein initial konservatives Vorgehen bei sportlich noch sehr aktiven Patienten ist, bleibt aber ungeklärt.
Unabhängig vom Ischämieausmass und vom anatomischen Schweregrad der KHK gab es keinen klaren Vorteil des invasiven im Vergleich zum initial konservativen Vorgehen. Allerdings zeigt der Forrest Plot (1), dass sich die Punktschätzwerte sehr konsistent in Richtung Nutzen für ein invasives Vorgehen bewegen, je schwerer die KHK ist, auch wenn die statistische Signifikanz nicht erreicht wird.
Früher Einsatz der Leitlinien-konformen medikamentösen Therapie
Bei Patienten mit Angina pectoris sollte möglichst beim ersten Kontakt bereits probatorisch eine anti-anginöse Therapie etabliert werden, um im Verlauf deren Wirksamkeit und allfällige Nebenwirkungen zu erfassen (5). Wenn die Resultate der erweiterten KHK Abklärung dann vorliegen, ermöglicht dies, das weitere Prozedere (initial konservativ versus invasiv) vor dem Hintergrund erster Erfahrungen mit der anti-anginösen Therapie zu besprechen. Bereits die ESC Leitlinien über die myokardiale Revaskularisation 2018 (8) haben empfohlen, vorerst zu überprüfen, ob die Angina pectoris mit Medikamenten gut eingestellt werden kann (Klasse IA).
Wertung der Ischemia Studie in der Diskussion mit Patienten
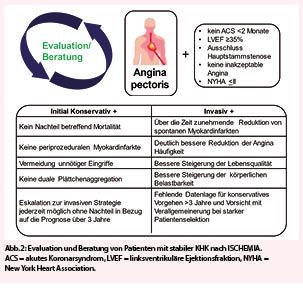
Die Ergebnisse der ISCHEMIA Studien sollten den Patienten erklärt und im Kontext Ihrer Erwartungen und Befürchtungen in der Gesamtschau der verfügbaren Evidenz diskutiert werden. Bei Vorliegen bestimmter Kriterien ist unverändert direkt die Koronarangiographie zu empfehlen (Abbildung 1). Sind diese nicht evident, eine Hauptstammstenose ausgeschlossen und die Angina mit Medikamenten zufriedenstellend kontrolliert ohne störende Nebenwirkungen, sollten mit dem Patienten die weiteren Optionen erläutert werden. Die Vor- und Nachteile betreffend Symptomatik und Prognose sind elementare Bestandteile dieser Diskussion (Abbildung 2). Eine Reduktion der Angina pectoris erfolgt durch Stent oder Bypass äusserst effizient (in einem von drei Patienten komplett eliminiert) ohne Notwendigkeit, längerfristig anti-anginöse Medikamente einzunehmen. Der Erfolg auf Symptomebene hängt von der Häufigkeit der Angina ab, d.h. je häufiger die Angina auftritt, desto wahrscheinlicher wird die Revaskularisation diesbezüglich erfolgreich sein.
Betreffend Prognose ist es für die Patienten von Belang, dass eine initial konservative Therapie über die Dauer von 3.2 Jahren betreffend Vermeidung prognostisch relevanter Ereignisse (Tod oder Myokardinfarkt) ähnliche Ergebnisse erbringt wie die Revaskularisation mit Stent oder Bypass. Dies unter ausgebauter medikamentöser Therapie mit guter Kontrolle der Risikofaktoren (Aspirin, Statin, Betablocker, u.a.). So war der mediane Blutdruckwert in der initial konservativen Gruppe 130/77 mmHg und das mediane LDL-C betrug 1.7 mmol/L am Ende der Studie. Die Patienten sollten wissen, dass mit einem initial invasiven Vorgehen das Risiko für spontane Herzinfarkte signifikant tiefer ist (HR 0.67, 95% CI: 0.53 bis 0.83) und die Kaplan-Meier Kurvenverläufe auf einen über die Zeit zunehmenden Vorteil (Scherenform) mit der invasiven Strategie zeigen, konsistent mit anderen grossen Studien (9). Zudem reihen sich diese Ergebnisse in die Resultate von mehreren Autopsiestudien ein, in welchen in der Mehrzahl der Patienten als Ursache für tödliche Myokardinfarkte signifikante (>75%) Stenosen vorlagen (10, 11). Dies ist auch konsistent mit angiographischen und intravasuklären Ultraschall (IVUS) Studien in ACS Patienten, die zeigen, dass mehrheitlich Stenosen >50% (12) und kleine Lumenflächen (2mm2) (13) vorlagen. Die relevante Koronarstenose, insbesondere wenn durch eine lipidhaltige Plaque bedingt, ist also kein benigner Befund und das Ansprechen derselben auf Statine variabel.
Es liegt in der Natur der Sache, dass das Risiko für einen peri-prozeduralen Myokardinfarkt nur bei einem invasiven Vorgehen besteht. Solche Infarkte stellen häufig eine Laborauffälligkeit dar, verlaufen für den Patienten nicht selten unbemerkt und haben häufig keine prognostische Relevanz (14). Man sollte nicht vergessen, dass bereits eine 90 Sekunden andauernde Balloninflation je nach Troponin-Assay zu einem formalen Myokardinfarkt (gemäss 4th Universal Definition) in 11-63% der untersuchten Studienpatienten führt (15).
Den Patienten sollte weiter bewusst sein, dass bei mindestens einem Drittel der Fälle mit der initial konservativen Strategie im Verlauf trotzdem eine invasive Abklärung stattfinden wird, und dass jederzeit eine Neubeurteilung stattfinden muss, wenn sich der Schmerzcharakter- und/oder die Häufigkeit ändert.
Ein initial konservatives Vorgehen kann für Patienten von Vorteil sein, die gegenüber einem invasiven Vorgehen kritisch eingestellt sind oder wenn die Gefahren einer Intervention als höher eingestuft werden (z.B. sehr hohes Blutungsrisiko, schwere Niereninsuffzienz, hohe Komplexität der KHK etc.) als der potentielle Gewinn.
Copyright bei Aerzteverlag medinfo AG
Schweizer Herz- und Gefässzentrum
Universitätsklinik für Kardiologie
Inselspital
3010 Bern
Leiter Herzkatheterlabor
Universitätsklinik für Kardiologie
Inselspital
Freiburgstrasse 18
3010 Bern
lorenz.raeber@insel.ch
Sarah Bär erhält Forschungsbeiträge an die Institution von Bangerter Rhyner Stiftung und Medis.
Lorenz Räber erhält Forschungsbeiträge and die Institution von Abbott
Vascular, Bangerter Rhyner Stiftung, Biotronik, BostonScientific, Heartflow, Medis, Sanofi, Schweizerische Herzstiftung, Regeneron und Beratungs- oder Sprecherhonorare von Abbott Vascular, AstraZeneca, Amgen, Canon, Occlutech, Sanofi, Vifor.
am Online-Beitrag unter: www.medinfo-verlag.ch