Während der COVID-19 Pandemie werden Check-ups immer beliebter. Aber sind sie wirklich sinnvoll? Einige Studien lassen daran zweifeln, denn sie können keine Evidenz für die Wirksamkeit aufzeigen. Die Praxis zeigt jedoch, dass diese Vorsorgeuntersuchungen oft sinnvoll sind, da viele Menschen nicht nur im Sinne einer Primärprävention einen Check-up machen wollen. Viel mehr gehen die Leute zum Arzt, weil sie im Frühstadium einer Krankheit die Progredienz der Erkrankung und daraus entstehende Komplikationen vermeiden möchten. Zudem gehen immer mehr Leute zum Check-up, weil sie damit eine Resilienz aufbauen wollen, und weil sie ihren Gesundheitszustand insgesamt verbessern möchten.
In der Bevölkerung wird aktuell viel darüber gesprochen, wie eine Infektion mit dem SARS-CoV-2 verhindert werden kann. Vorsorge, Check-ups und Präventionsmedizin sind inzwischen fast Modewörter geworden. Die Menschen wollen ihr Immunsystem aufbauen und Risikofaktoren für eine ungünstige Prognose bei einer Infektion mit SARS-CoV-2 reduzieren. So sind auch Check-ups während der COVID-19 Pandemie immer beliebter geworden.
Oft versteht man unter Check-up eine periodische Allgemeinuntersuchung bei Menschen, die sich gesund fühlen. Somit ist ein Check-up für subjektiv Gesunde eine Vorsorgeuntersuchung im Rahmen der Primärprävention, bei der es vor allem um die Früherkennung bislang symptomloser Krankheiten geht (1).
Argumente gegen Check-ups basieren stark auf der bekannten Cochrane Metaanalyse aus dem Jahr 2019. Anhand von 17 Studien behaupten die Autoren, dass diese Vorsorgeuntersuchungen die Morbidität und Mortalität insgesamt nicht reduzieren würden (2).
Um diese Punkte zu adressieren, müssen die folgenden Fragen zwingend gestellt werden:
1) WARUM gehen Leute zum Check-up? Was sind die motivierenden Faktoren und Gründe? Gehen Menschen zum Arzt nur um Krankheiten zu vermeiden bzw. früh zu erkennen, oder wollen sie durch den Arztbesuch das Wohlbefinden und den Gesundheitszustand sowie ihre Leistung verbessern?
2) WIE wird ein Check-up durchgeführt und welche Diagnostik wird eingesetzt? Sind alle Check-up Angebote in der Schweiz gleichwertig?
3) WANN und zu welchem Zeitpunkt werden Check-ups durchgeführt?
Nach Beantwortung dieser Fragen, wird es klar, dass viele Menschen nicht nur im Sinne einer Primärprävention einen Check-up machen wollen. Viel mehr gehen die Leute zum Arzt, weil sie im Frühstadium einer Krankheit die Progredienz der Erkrankung sowie Komplikationen vermeiden möchten. Zudem gehen immer mehr Leute zum Check-up, weil sie sportlich ambitioniert sind, weil der Leistungsdruck bei der Arbeit hoch ist und sie Resilienz aufbauen wollen, und weil sie ihren Gesundheitszustand insgesamt verbessern wollen. Damit müssen die Studien zur Präventionsmedizin kritisch interpretiert werden, da sie oft nur die primärpräventiven Interventionen analysieren.
Ausgangslage
Warum wollen Leute zum Check-up?
Immer mehr Personen gehen zum Arzt, um Ihre Gesundheit zu optimieren. Auch Unternehmen interessieren sich vermehrt für die Gesundheit der Mitarbeiter, denn sie wissen, dass deren Gesundheit und Wohlbefinden die Produktivität steigert und Krankheitsausfälle reduziert (3). Damit die Firmen produktiv und erfolgreich bleiben, bieten sie daher Check-ups für Mitarbeiter an.
Aber auch Menschen mit chronischen Krankheiten wie z.B. arterielle Hypertonie, KHK, Diabetes und weitere metabolische Krankheiten wollen einen Check-up, um Komplikationen zu vermeiden und um ihr Wohlbefinden zu optimieren. Gerade multimorbide Patienten können von einem holistischen Ansatz eines Check-ups profitieren und sie bevorzugen oft Vorsorgeuntersuchungen beim Hausarzt, statt nur organspezifische Untersuchungen bei Spezialisten durchzuführen. Schliesslich muss der Mensch und die Organsysteme bei Multimorbidität und Polypharmazie als Ganzes betrachtet werden. Studien zeigen zudem, dass langjährige, regelmässige und vertrauliche Arzt-Patientenbeziehungen die besten Ergebnisse ermöglichen (4).
Schliesslich gibt es auch Leute bei denen die eigentlichen Motive, wie zum Beispiel Angststörungen und Geschlechtserkrankungen («Hidden Agenda») unausgesprochen bleiben, solange nicht danach gefragt wird. Im Rahmen der Anamneseerhebung ist es somit wichtig, eine «Hidden Agenda» aktiv herauszufinden oder auszuschliessen.
Wie wird ein Check-up gestaltet und durchgeführt
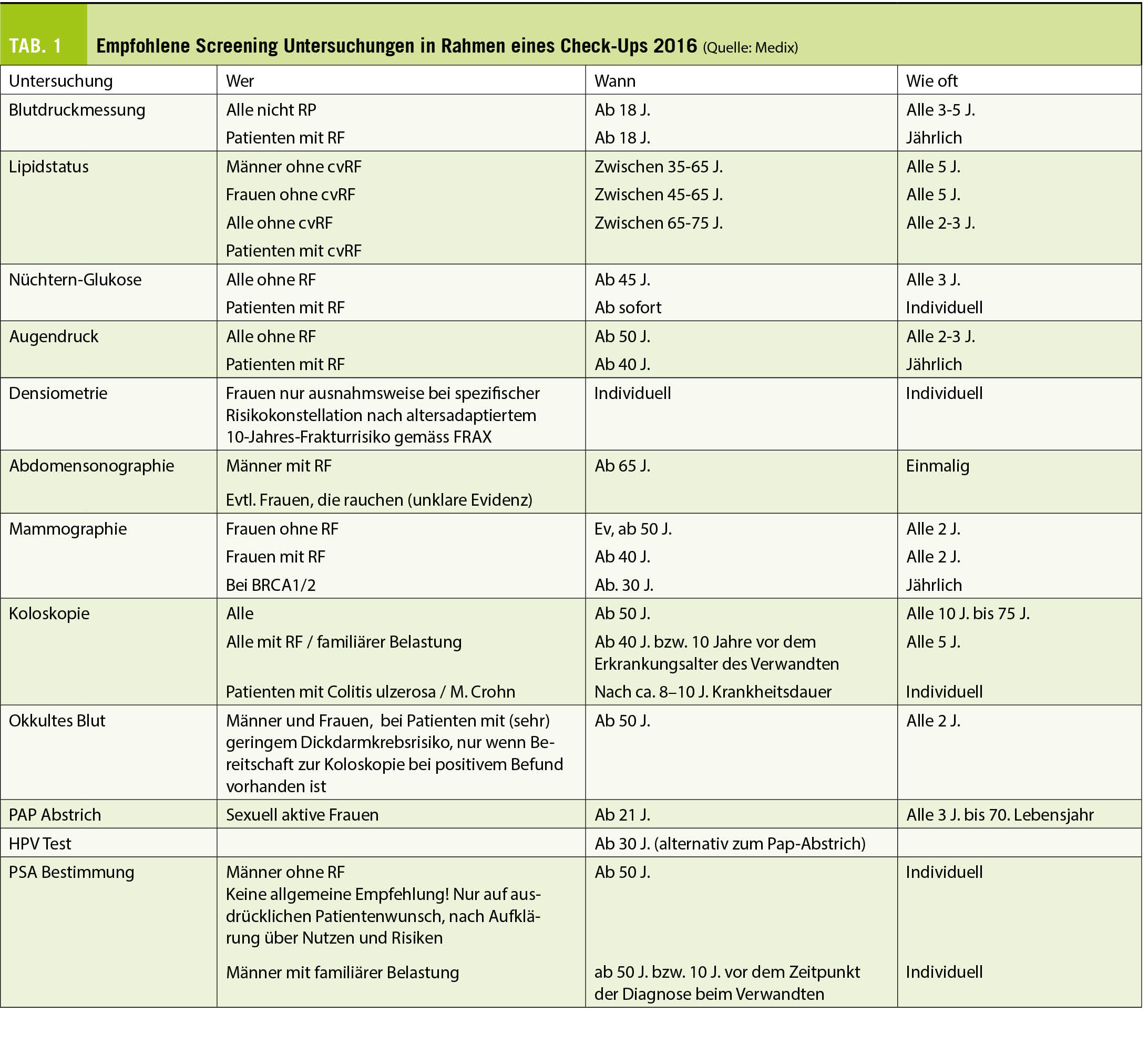
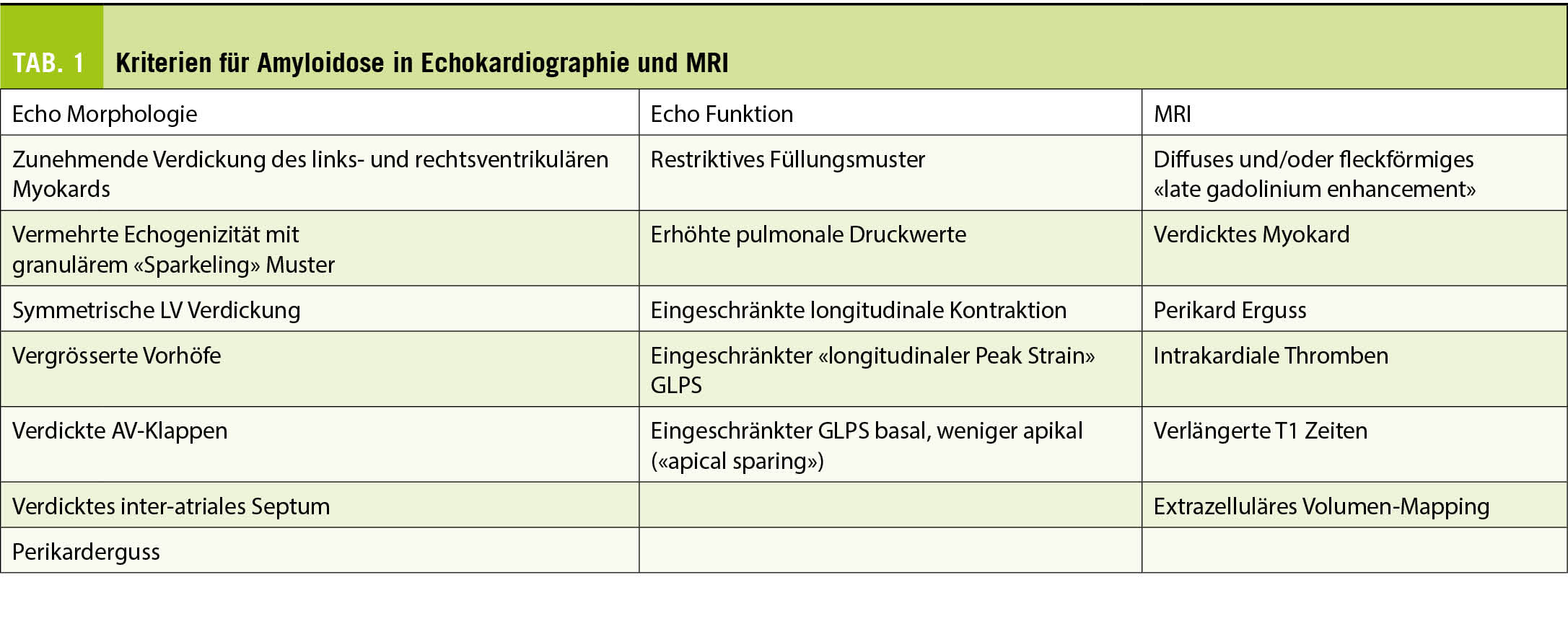
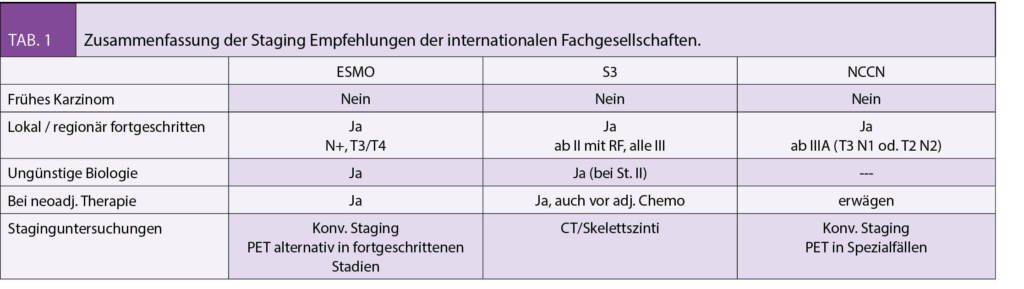
Grundsätzlich gehören zum Check-up die Anamnese, klinische Untersuchungen, Laboruntersuchungen und apparative Untersuchungen. Welche Untersuchungen vorgenommen und wie das Grundprogramm ergänzt wird, sind von Anamnese, Symptomen, Lebensstil und dem Untersucher abhängig (Tab. 1). Check-ups werden daher sehr unterschiedlich durchgeführt. Ähnlich wie z.B. in der Orthopädie, wo der Outcome einer Hüft-TP vom Operateur und dem chirurgischen Zentrum abhängig ist, wird die Qualität und das Nutzen eines Check-ups stark vom Arzt beeinflusst.
Entscheidet sich ein Arzt zum Beispiel ein Thorax-Röntgen als Screening für Lungenkrebs bei Rauchern einzusetzen, ist die Wahrscheinlichkeit, dass er einen Tumor verpasst erheblich grösser als bei einem Low-Dose-CT. Studien zeigen eine relative Reduktion von sogar 20% in der Lungenkrebsmortalität für die Niedrigdosis-CT-Gruppe im Vergleich zum konventionellen Thorax-Röntgen (5).
Zudem ist es an der Zeit, die Gestaltung der Prävention umzudenken. Auf Populationsebene sind auch Coaching Programme sowie Digital- und Tele-Medizin nötig, gerade auch während eines Lock-Downs. Das traditionelle Modell, in welchem alles in der Arztpraxis gemacht werden soll, ist Vergangenheit (4).
Wann findet ein Check-up statt – «Timing is all»
Zum einen spielt die Frequenz von Check-ups eine Rolle. Die kritischen Meta-Analysen, messen die Kosten-Wirksamkeit von jährlichen Check-ups und schliessen Personen über 65 Jahren von den Studien aus. Aus rein ökonomischer Sicht kann die Frequenz von Check-ups eine signifikante Rolle in der Kosten-Wirksamkeit der Analyse spielen. Zum anderen sind Nutzen und Wirksamkeit vom Timing abhängig. Eine Koloskopie, Augendruckmessung oder PSA Bestimmung bei einem 35-Jährigen ohne Risikofaktoren ist sinnlos oder sogar schädlich. PAP ist jedoch bei sexuell aktiven Frauen bereits mit 21 Jahren indiziert (Tab 1).
Sollen Menschen, die sich kerngesund fühlen, eine Vorsorge Untersuchung angeboten bekommen?
Basierend vor allem auf der Cochrane Studie argumentieren einige Ärzte, dass keine sicheren Hinweise auf eine Senkung von Morbidität oder Mortalität durch Check-ups bei asymptomatischen Menschen gegeben seien (6). Bei vielen gesunden Personen geht es jedoch nicht primär um Mortalität und Morbidität, sondern vielmehr um Verbesserung der Leistung und Gesundheit, sowie von Förderung eines gesunden Lebensstils und somit auch um die Reduktion von Risikofaktoren.
Zum Beispiel bei Spitzensportlern und einigen Hobby Sportlern (je nach Disziplin) sind beispielsweise jährliche sportärztliche Screenings indiziert. Auch wenn z.B. EKG-Screening-Untersuchungen im Rahmen von Check-ups nicht bei allen Personen nötig sind, wird ein EKG bei Sportlern empfohlen (7).
Gemäss einer Studie vom National Research Council and Institute of Medicine in den Vereinigten Staaten sind bis zur Hälfte aller frühzeitigen Todesfälle durch Risikoverhalten und ungesunden Lebensstil verursacht. Durch motivierende Gespräche im Rahmen eines Check-ups, Beratung und Aufklärung, kann ein gesunder Lebensstil durch Sport, Ernährung, Schlaf, Health Litteracy, Rauchstopp und Gewichtsreduktion verbessert werden. Zudem können die Ärzte wichtige Themen zu psychosozialen Aspekten der Gesundheit und Depression gerade während der Zeit von Home-Office und Lock-down angehen. Schliesslich können auch Impfungen während eines Check-ups aufgefrischt werden.
Selbstverständlich ist die Früherkennung von Krankheiten für die Prognose sehr wichtig. Leider gehen Personen jedoch oft zum Check-Up erst wenn sie Symptome haben und sind bei dem Arzttermin gar nicht asymptomatisch (8). Zum Beispiel bei Herz-Kreislauf-Erkrankungen – die nach den Krebserkrankungen in der Schweiz die zweithäufigste Todesursache sind – ist die Früherkennung von familiären Hypercholesterinämien wichtig aber die Diagnosestellung findet oft mit Verzögerung statt. Das Motto «je früher die Diagnose, desto besser» ist hier von grosser Bedeutung, da einer ihrer wichtigsten Risikofaktoren das Cholesterin ist, besonders das LDL-Cholesterin (LDL-C) (AGLA 1). In einer Studie in Circulation konnte 2015 gezeigt werden, dass 4,4% der Patienten, bei denen die Hypercholesterinämie gerade erst entdeckt worden war, eine KHK entwickelten. Lag die Hypercholesterinämie schon ein bis zehn Jahre vor, waren es 8,1%. Bei 11 bis 20 Jahren waren es 16,5% (9). Daher messen die aktuellen Guidelines der European Society of Cardiology (ESC) dem Screening von kardiovaskulären Risikofaktoren und der konsequenten Senkung des LDL-C eine grosse Bedeutung bei.
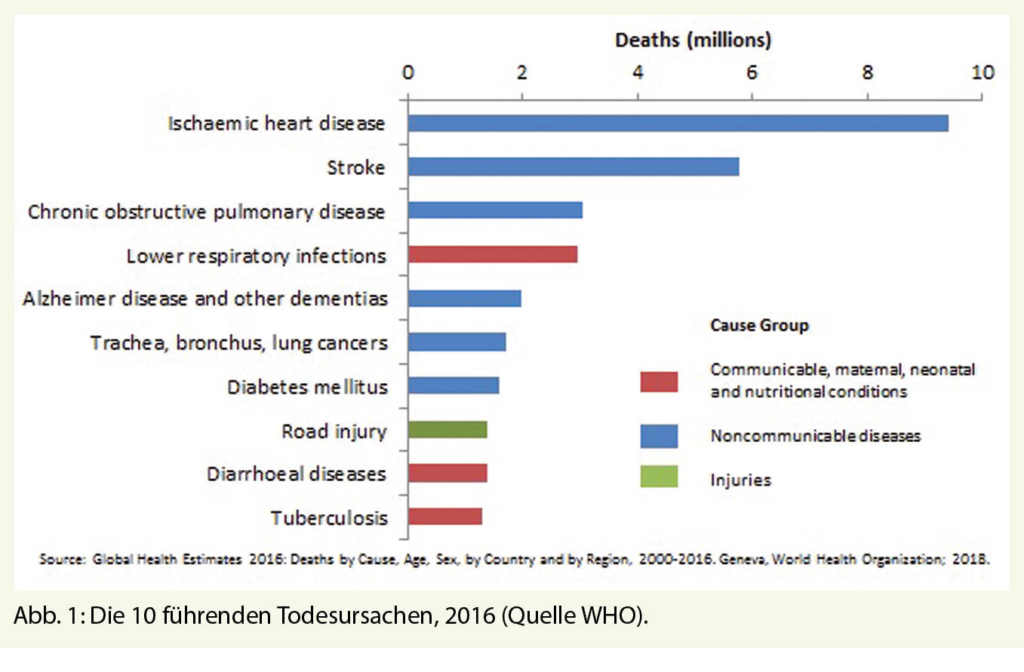
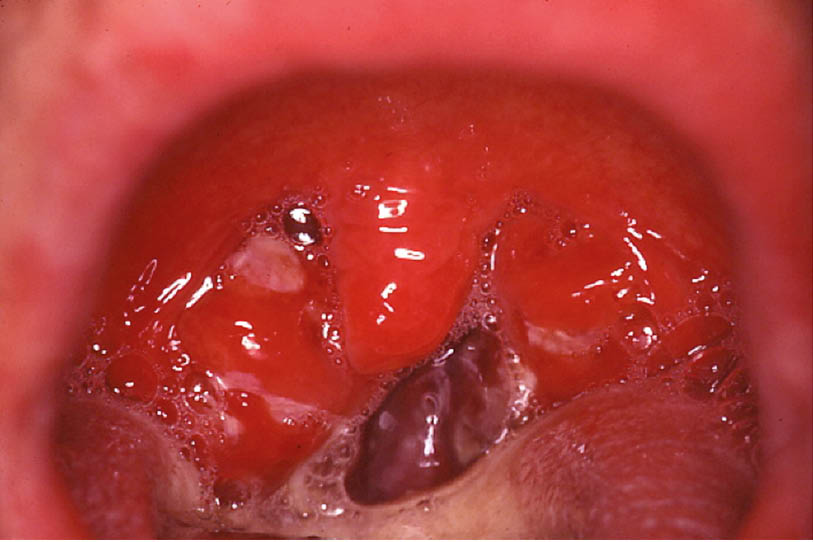
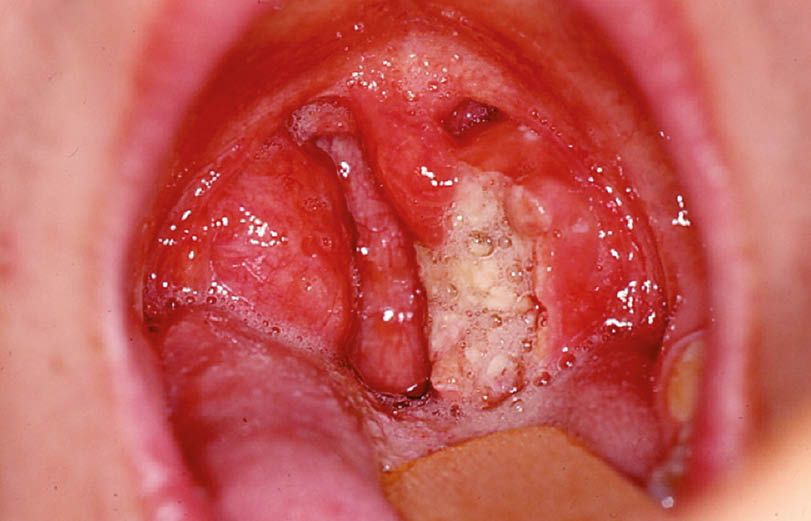
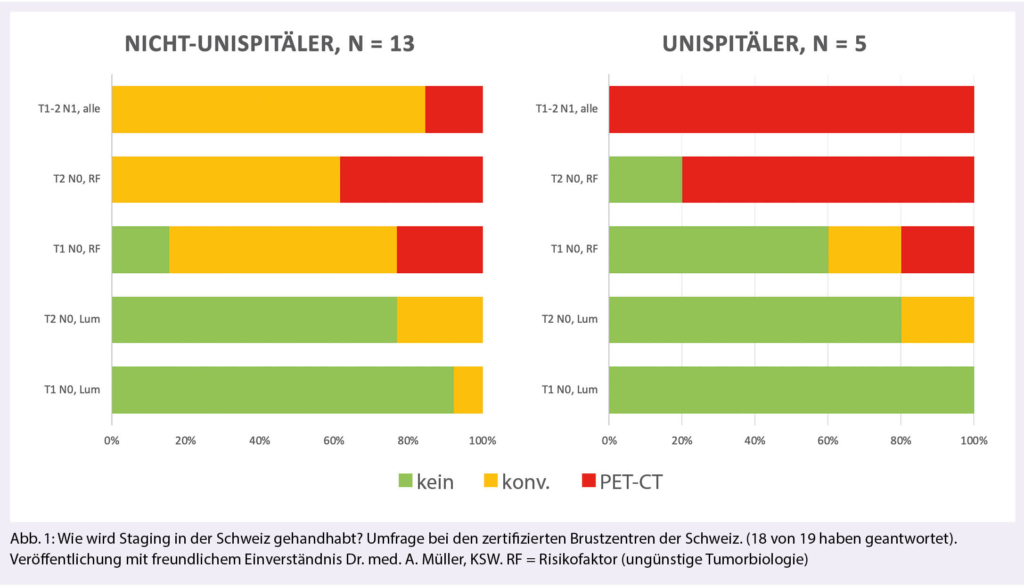
Bluthochdruck ist bekannterweise einer der wichtigsten kardiovaskulären Risikofaktoren mit einer hohen Prävalenz in der Schweiz und weltweit (Abb. 1). 60% der über 60-Jährigen und 80% der über 75-Jährigen sind hyperton. Die frühzeitige Diagnose und Behandlung der Hypertonie und deren Risikofaktoren wie Adipositas und Dyslipidämie kann das Auftreten von Folgekrankheiten wie Koronare Herzerkrankungen, Schlaganfall oder Nephropathien deutlich verringern. Leider sind jedoch bis 80% der Patienten mit einer arteriellen Hypertonie suboptimal eingestellt und profitierten so indirekt vom Check-up (10). Weitere Risikofaktoren, die während eines Check-ups anamnestisch erhoben werden, sind familiäre Belastungen, erhöhter Alkoholkonsum, Nikotinkonsum und Bewegungsmangel.
Ähnlich auch bei Lungenkrebs. Lungenkrebs ist die häufigste krebsbezogene Todesursache in der Schweiz – 85% der Fälle verlaufen tödlich. In der Schweiz stirbt jede 20. Person an Lungenkrebs. Machen sich Symptome wie Husten, Hämoptoe, Dyspnoe oder Schmerzen bemerkbar, ist es häufig schon zu spät. Auch bei Blutdruck und Diabetes ist die Früherkennung wichtig, um sekundäre Folgen zu vermeiden.
Die Prävention zahlt sich aus wenn die Qualität der Check-ups stimmt
Nach der Cochrane Studie von 2012 belasten Check-ups nach Ansicht der Autoren die Patienten durch unnötige Diagnosen. Die Diagnosen werden jedoch aufgrund objektiver Daten und Richtlinien oder nach systematischem Ausschlussverfahren erstellt und sind nicht «unnötig.» Die Diagnostik, die Interpretationen und die Therapien können jedoch sehr unnötig, unsinnig und auch schädigend sein.
Genauso wie eine verpasste Diagnose zu einer erheblichen Morbidität und Mortalität führen kann, kann auch eine Übertherapie höchst negative Auswirkungen haben. Daher geht es hier viel mehr darum, dass die Check-ups durch kompetente Fachleute durchgeführt werden mit individuellem Screening und richtigem Timing.
Zudem dienen die Check-ups nicht nur der Reduktion von Morbidität oder Mortalität. Viel mehr können Risikoverhalten und Risikofaktoren durch Beratung und Aufklärung angegangen werden und Check-ups können zu einem gesünderen und produktiveren Lebensstil führen.
Damit müssen die Studien zur Präventionsmedizin kritisch interpretiert werden, da sie oft nur die primärpräventiven Interventionen analysieren. Die Qualität der Check-ups müssen überprüft werden und neue Modelle der Präventionsmedizin sind gefragt.
Copyright bei Aerzteverlag medinfo AG
Check-up Zentrum Hirslanden
Forchstrasse 420
8702 Zollikon
anna.erat@hirslanden.ch
Die Autorin ist Chefärztin am Hirslanden Check-up Zentrum. Ansonsten hat sie in Zusammenhang mit diesem Artikel keine Interessenskonflikte deklariert.
1. Huber F, Beise U. Guideline Check up. Medix 2016, 4.
2. Krogsbøll LT, Jørgensen KJ, Gøtzsche PC. General health checks in adults for reducing morbidity and mortality from disease. Cochrane Database of Systematic Reviews 2019, Issue 1. Art. No.: CD009009. DOI: 10.1002/14651858.CD009009.pub3
3. Dahik A, Lovich D, Kreafle C, Bailey A, Kilmann J, Kennedy D, Roongta P, Schuler F, Tomlin L, Wenstrup J. What 12,000 Employees Have to Say About the Future of Remote Work. BCG Report 2020.
4.. Horn DM, Haas JS. Covid-19 and the Mandate to Redefine Preventive Care. N Engl J Med. 2020, Aug 12. doi: 10.1056/NEJMp2018749. Epub ahead of print. PMID: 32786183.
5. National Lung Screening Trial Research T, Aberle DR, Adams AM, et al. Reduced lung-cancer mortality with low-dose computed tomographic screening. The New England journal of medicine 2011, Aug 4;365(5):395-409.
6. Mehrotra A, Prochazka A. Improving value in health care — against the annual physical. N Engl J Med 2015;373:1485-1487.
7. Erat A. Pre-participation Evaluation for Screening of Health Risks in Leisure and Young Competitive Athletes Swiss Sports & Exercise Medicine 2019, 67 (3), 6–11.
8. Hunziker S, Schläpfer M, Langewitz W. et al. Open and hidden agendas of „asymptomatic“ patients who request check-up exams. BMC Fam Pract 2011; 12, 22 https://doi.org/10.1186/1471-2296-12-22
9. Navar-Boggan AM, Peterson ED, D’Agostino RB Sr, Neely B, Sniderman AD, Pencina MJ. Hyperlipidemia in early adulthood increases long-term risk of coronary heart disease. Circulation 2015, Feb 3;131(5):451-8.
10. Grätzel von Grätz P. Check-up mit 35 – Sinn oder Unsinn? Aerztezeitung 2015, May 05.