Wir haben für Vitamin D neue Erkenntnisse gewonnen. Aus hochqualitativen Studien bei über 36 000 Menschen geht hervor, dass eine tägliche Vitamin-D-Gabe von 800 IE bei älteren Erwachsenen mit Vitamin-D-Mangel und vorhandenem Sturzrisiko das Hüftbruchrisiko und das Sturzrisiko senkt. Wir haben auch gelernt, dass eine Vitamin-D-Supplementation bei gesunden mittelalterlichen und älteren Menschen ohne Vitamin-D-Mangel und ohne Osteoporose keinen zusätzlichen Schutz bietet. Auch zeigen grosse intermittierende Bolus-Gaben von Vitamin D entweder keinen Schutz vor Knochenbrüchen oder führen sogar zu einer Zunahme des Knochenbruchrisikos und Sturzrisikos bei vulnerablen älteren Menschen und sind damit obsolet. In den letzten Jahren zeigten jedoch grosse randomisierte Studien zur täglichen Vitamin-D-Gabe mit 2000 IE bei gesunden Menschen ohne Vitamin-D-Mangel im Alter von 50 Jahren (VITAL) und im Alter von 70 Jahren (DO-HEALTH) einen Vorteil auf das Immunsystem bezüglich Reduktion fortgeschrittener Krebserkrankungen, Krebsmortalität und Autoimmunerkrankungen.
We have gained new insights into vitamin D. High quality studies of over 36 000 people have shown that daily vitamin D supplementation of 800 IU reduces the risk of hip fracture and falling in older adults with vitamin D deficiency and existing falling risk. We have also learnt that vitamin D supplementation in healthy middle-aged and elderly people without vitamin D deficiency and without osteoporosis offers no additional protection. Also, large intermittent bolus doses of vitamin D either show no protection against fractures or even lead to an increase in fracture risk and fall risk in vulnerable elderly people and are therefore obsolete. In recent years, however, large randomised studies on daily vitamin D supplementation with 2000 IU in healthy people without vitamin D deficiency at the age of 50 (VITAL) and at the age of 70 (DOHEALTH) have shown a benefit on the immune system in terms of reducing advanced cancers, cancer mortality and autoimmune diseases.
Keywords: Vitamin D, fracture risk, osteoporosis, immune system, cancer
Grundlagen der Vitamin-D-Versorgung
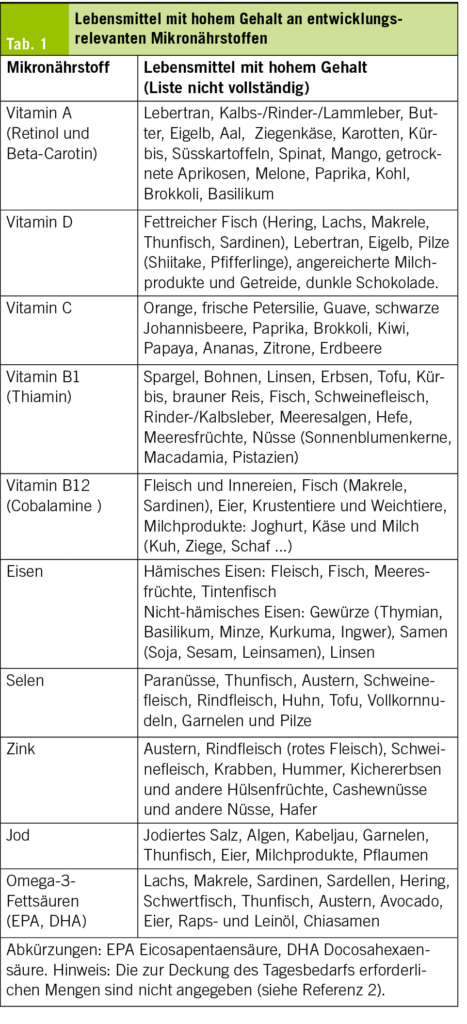
Vitamin D spielt in jedem Alter eine wichtige Rolle im Erhalt unserer Knochengesundheit und bei der Regulation des Kalziumspiegels im Blut. Während der Kalziumbedarf mit einer gesunden Ernährung gedeckt werden kann, ist es wichtig festzuhalten, dass dies für Vitamin D nicht gilt. Es ist nahezu unmöglich, genügend Vitamin D aus der Nahrung zu sich zu nehmen, da nur wenige Nahrungsmittel namhafte Mengen an Vitamin D enthalten (Lachs, fetter Fisch). Der grösste Teil von Vitamin D wird mithilfe von Sonnenlicht über die Haut gebildet (1). Diese hauteigene Vitamin-D-Produktion nimmt jedoch mit dem Alter ab, und ältere Menschen vermeiden oft wegen der Hitze eine direkte Sonnenexposition. Weitere Faktoren, die unabhängig vom Alter die Wirkung der Sonnenexposition als Hauptquelle von Vitamin D einschränken, sind die Saisonalität und die Anwendung von Sonnenschutzprodukten. Auch ein ausreichender Vitamin-D-Spiegel nach einem sonnenreichen Sommer kann nicht über den Winter hinweg aufrechterhalten werden. Die Halbwertszeit von Vitamin D (25-Hydroxy-Vitamin-D) beträgt nur 2–3 Wochen (2).
Da durch gesunde Ernährung und direkte Sonneneinstrahlung im Winter nicht genügend Vitamin D produziert werden kann, zeigen Studien, dass etwa 50 % der Kinder und Erwachsenen an einem Vitamin-D-Mangel, mit Blutwerten von unter 20 ng/ml für das 25-Hydroxy-Vitamin- D (25[OH]D), aufweisen (3–5). Vitamin-D-Supplemente sind daher altersunabhängig im Winter eine zu erwägende Massnahme zum Ausgleich eines saisonalen Vitamin-D-Mangels. Bei älteren Erwachsenen ist eine Prävention des Vitamin-D-Mangels mit Vitamin-D-Supplementen nach den Erkenntnissen unabhängig von der Jahreszeit (3–5).
Vitamin-D-Supplementation bezüglich Knochenbruchprävention
Ein Vitamin-D-Mangel erhöht das Risiko für Stürze und Knochenbrüche. Für ältere Erwachsene (Alter 65+) mit erhöhtem Risiko für einen Vitamin-D-Mangel und Osteoporose führt eine tägliche Supplementierung mit 800 IE, insbesondere in Kombination mit einer ausreichenden Kalziumzufuhr, belegtermassen zu einer Verminderung des Sturz- und Hüftbruchrisikos (6–9). Hingegen ist die Evidenz zur Wirkung von Vitamin-D-Supplementen, um das Knochenbruchrisiko und Sturzrisiko bei gesunden alten Menschen zu senken, unklar (10, 11).
In den Jahren 2016 bis 2018 wurden vier Metaanalysen durchgeführt, um den Nutzen von Vitamin D für die Frakturprävention zu untersuchen. Zwei dieser Metaanalysen konzentrieren sich auf die Primärprävention von Frakturen bei Erwachsenen ab 50 Jahren, bei denen kein Risiko für Frakturen und kein Vitamin-D-Mangel besteht (12, 13). Eine weitere Metaanalyse konzentrierte sich auf die Kombination von Vitamin D plus Kalzium (9) und die zuletzt publizierte Metaanalyse auf die individuelle Wirkung von Vitamin D ohne Kalzium (14). Die neueren Metaanalysen unterstützen keinen primärpräventiven Schutz einer Vitamin-D-Supplementation vor Frakturen bei Erwachsenen im Alter 50+ ohne Vitamin-D-Mangel und ohne Osteoporose (12, 13). Allerdings ist die Anzahl von grossen Interventionsstudien in dieser Niedrigrisiko-Zielgruppe limitiert (12, 13). Erwachsenen im Alter von 65 und darüber mit einem hohen Risiko für Vitamin-D-Mangel und Osteoporose sollte eine Vitamin-D-Supplementation mit 800 IE Vitamin D pro Tag (mit [9] und ohne [15] zusätzliche Kalzium-Supplementation) anhand der bestehenden Evidenz nicht vorenthalten werden. Allerdings sollten bei der Hochrisikopopulation älterer Erwachsener mit erhöhtem Sturzrisiko die grossen Vitamin-D-Bolusgaben wegen gegenteiliger Wirkung mit Frakturzunahme vermieden werden (16, 17).
Bezüglich neuer Resultate der VITAL- und DO-HEALTH-Studie mit zusätzlich 2000 IE Vitamin D am Tag zeigte sich bei generell gesunden Menschen im Alter von 50+ (VITAL) und 70+ (DO-HEALTH) eine neutrale Wirkung auf das Knochenbruchrisiko. In der Einordnung der Resultate dieser Studien ist wichtig festzuhalten, dass in VITAL nur 12 % und in DO-HEALTH nur 36 % der Teilnehmer zum Studienbeginn einen Vitamin-D-Mangel hatten und alle Teilnehmer in beiden Studien zusätzlich zur Studienmedikation 800 IE Vitamin D einnehmen durften (10, 11, 18).
Insbesondere für ältere Erwachsene mit einem erhöhten Risiko für Frakturen und/oder Vitamin-D-Mangel ist es weiterhin sinnvoll, 800 IE Vitamin D pro Tag einzunehmen, analog den Empfehlungen der International Osteoporosis Foundation (19), der US Endocrine Society (20) und NOF (21). Wie bereits erwähnt, sollten grosse monatliche oder jährliche Bolusapplikationen von Vitamin D bei älteren Erwachsenen mit einem Risiko für Frakturen wegen Zunahme des Frakturrisikos in der klinischen Versorgung nicht fortgesetzt werden (6).
Heutige Empfehlungen
In den heutigen Empfehlungen zu Vitamin D (Institute of Medicine [22], DGE [23], BAG Schweiz [24], US Endocrine Society [25], IOF [19]) wird die tägliche Vitamin-D-Zufuhr altersabhängig definiert: 400 IE (Internationale Einheiten) pro Tag im ersten Lebensjahr, 600 IE pro Tag zwischen dem 2. und 64. Lebensjahr und 800 IE/Tag ab dem 65. Lebensjahr (in der Schweiz 800 IE/Tag ab dem 60. Lebensjahr). Es ist gut belegt, dass im Erwachsenenalter 600 bis 800 IE/Tag in über 97 % der Fälle den Vitamin-D-Mangel korrigieren können (26, 27). Diese Dosis ist zudem auf die Population bezogen sicher und ohne vorherige Messung der 25-Hydroxy-Vitamin-D-Blutkonzentration anwendbar (Institute of Medicine [22], DGE [23], BAG Schweiz [24], US Endocrine Society [25], IOF [19]).
Angesichts der hohen Winterprävalenz des Vitamin-D-Mangels bei Kindern und älteren Erwachsenen und der beschränkten Möglichkeiten, eine ausreichende Vitamin-D-Zufuhr über eine gesunde Ernährung sicherzustellen, ist in ganz Europa unabhängig vom Alter eine Indikation zur Supplementierung in den Wintermonaten November bis Ende April zu erwägen. Älteren Menschen wird aufgrund der verminderten hauteigenen Vitamin-D-Produktion bei Sonnenexposition sowie der belegten Prävention von Stürzen und Hüftbrüchen eine Supplementierung mit Vitamin D auch im Sommer empfohlen. Die empfohlenen Tagesdosen zur Supplementierung entsprechen den oben genannten Angaben zur Vitamin-D-Zufuhr.
Der Dachverband Osteologie (DVO) hat im September 2023 eine überarbeitete Version der Osteoporose-Leitlinie herausgegeben (https://dv-osteologie.org/osteoporose-leitlinien). Sie fasst die aktuelle Evidenz zur Prophylaxe, Diagnostik und Therapie der Krankheit bei postmenopausalen Frauen und bei Männern ab dem 50. Lebensjahr zusammen.
Wie wirkt Vitamin D bezüglich Knochenbruchprävention?
Neben der antiresorptiven Wirkung von Vitamin D am Knochen hat Vitamin D mechanistisch gesehen einen zweiten relevanten muskelzentrierten Wirkungspfad in der Knochenbruchprävention. Der Hauptrisikofaktor für eine Hüftfraktur ist ein Sturz, und über 90 % aller Frakturen treten nach einem Sturz auf (28). Daher ist es für das Verständnis und die Prävention von Frakturen im höheren Alter wichtig, den engen Zusammenhang von Muskelschwäche (29) und Stürzen (30, 31) zu berücksichtigen. Tatsächlich kann eine antiresorptive Behandlung allein bei Personen über 80 Jahren mit nicht skelettalen Risikofaktoren für Frakturen trotz einer Verbesserung des Knochenstoffwechsels die Anzahl der Frakturen nicht verringern (32).
Die Muskelschwäche ist ein wichtiger Risikofaktor für Stürze und ein Merkmal des klinischen Syndroms eines schweren Vitamin-D-Mangels. Muskelschwäche aufgrund eines Vitamin-D-Mangels kann das Frakturrisiko durch eine erhöhte Sturzanfälligkeit erhöhen. Der Vitamin-D-Rezeptor (VDR) wird im menschlichen Muskelgewebe exprimiert, wie in den meisten Studien gezeigt wurde (79). An seinen Rezeptor im Muskelgewebe gebundenes Vitamin D kann zu einer De-novo-Proteinsynthese führen (80), gefolgt von einer relativen Zunahme des Durchmessers und der Anzahl der schnellen Typ-II-Muskelfasern (80). Bemerkenswert ist, dass die schnellen Typ-II-Muskelfasern im Vergleich zu den langsamen Typ-I-Muskelfasern mit zunehmendem Alter abnehmen, was zu einer erhöhten Sturzneigung führt. Darüber hinaus erhöht eine Supplementierung mit Vitamin D im Vergleich zu einem Placebo die Anzahl der Vitamin-D-Rezeptoren im Muskelgewebe sowie die Anzahl und den Durchmesser der Typ-II-Muskelfasern bei postmenopausalen Frauen (80).
Schliesslich ist es wichtig zu beachten, dass Vitamin D mehrere Komponenten des Sturz-Fraktur-Konstrukts beeinflussen kann, darunter Kraft (8), Gleichgewicht (81), Funktion der unteren Extremitäten (82), Stürze (77), Knochendichte (83, 84), das Risiko von Hüft- und nicht vertebralen Frakturen (85, 86) und das Risiko der Einweisung in ein Pflegeheim (87).
Sicherheit der Vitamin-D-Supplementation
Um die schützende Wirkung von Vitamin D auszuschöpfen, sollte anhand der heutigen Datenlage eine tägliche Supplementierung gewählt werden (6). Alternativ zeigt eine umfassende Literatur, dass Vitamin-D-Bolusgaben (ab 60 000 IE monatlich oder ab 300 000 IE jährlich), insbesondere bei älteren Erwachsenen, sowohl das Sturz- als auch das Knochenbruchrisiko erhöhen können. Eine Erklärung ist, dass der Körper bei zu hohen Vitamin-D-Gaben gegenregulierende Mechanismen in Gang setzt, die Vitamin D akut abbauen und dann eher zu einem Vitamin-D-Mangel führen (6).
Ist es sinnvoll, den Blutspiegel des 25-Hydroxy-Vitamin-D zu messen?
Ob eine ausreichende Vitamin-D-Versorgung vorliegt, lässt sich über die Bestimmung des 25(OH)D-Wertes im Blut ermitteln. Ein 25(OH)D-Blutwert von weniger als 20 ng/ml (< 50 nmol/l) wird als Vitamin-D-Mangel bezeichnet. Werte unter 10 ng/ml (< 25 nmol/l) gelten als schwerer Mangel und können negative Folgen wie Rachitis bei Kleinkindern und Osteomalazie bei Erwachsenen hervorrufen (2). Ein 25(OH)D-Zielwert zwischen 20 und 30 ng/ml wird bezüglich Fraktur- und Sturzprävention als optimal angesehen, wobei Werte über 45 ng/ml mit einem erhöhten Sturzrisiko in Verbindung gebracht wurden (26).
Die 25(OH)D-Bestimmung wird nicht als Routineuntersuchung empfohlen, wenn keine Risiken für einen schweren Vitamin-D-Mangel vorliegen. Hier kann eine direkte Supplementation mit der Standarddosis erfolgen (600–800 IE/d; bei jüngeren Menschen vor allem im Winter, ab dem 65. Lebensjahr unabhängig von der Jahreszeit).
Diese Empfehlung stützt sich darauf, dass ein Vitamin-D-Mangel weitverbreitet ist (siehe oben). Für ältere Erwachsene mit erhöhtem Risiko für einen Vitamin-D-Mangel und Osteoporose stützt sich diese Empfehlung auf hochqualitative klinische Interventionsstudien mit über 30 000 Menschen, in denen nachgewiesen wurde, dass Vitamin-D-Supplemente in einer Dosis von 800 IE/d das Sturzrisiko und das Hüftbruchrisiko um ca. 20–30 % vermindern (6–9). Die Sicherheit bzgl. Nebenwirkungen und Risiken dieser täglichen Empfehlung sind gut belegt bei Menschen mit und ohne Vitamin-D-Mangel (6).
Vitamin-D-Dosierung in den VITAL- und DO-HEALTH-Studien
Anhand der VITAL-Studie bei gesunden Menschen im Alter von 50 Jahren und darüber und der DO-HEALTH-Studie bei gesunden Menschen im Alter von 70 Jahren und darüber kann die Sicherheit auf eine tägliche Zufuhr von 2000 IE am Tag ausgeweitet werden (10, 33). Allerdings brachte die höhere Dosierung keine weiteren Vorteile für die Sturz- und Knochenbruchprävention in VITAL (33, 34) oder DO-HEALTH (10, 35). Ein Vorteil auf die Knochendichte an der Hüfte (36), Krebsprävention (37) und Prävention von frühzeitiger Gebrechlichkeit (38) konnte für die tägliche Dosierung von 2000 IU Vitamin D in DO-HEALTH jedoch nicht ausgeschlossen werden. Konsistent zeigt VITAL für die tägliche Dosierung von 2000 IU Vitamin D eine Reduktion schwerer Krebserkrankungen (39), Reduktion von Krebsmortalität (40) und Reduktion von Autoimmunerkrankungen (41).
Copyright
Aerzteverlag medinfo AG
Zweitabdruck aus Therapeutische Umschau 01/2025
Universität Basel, Dept. Universitäre Altersmedizin Felix Platter, Basel
Dept. Geriatrie und Altersforschung, Universität Zürich, Zürich
Tièchestrasse 99
8037 Zürich
heikea.bischoff-ferrari@uzh.ch
Die Autorin hat keine Interessenkonflikte im Zusammenhang mit
diesem Artikel deklariert.
1. Holick, M.F., Sunlight, UV-radiation, vitamin D and skin cancer: how much sunlight do we need? Adv Exp Med Biol, 2008. 624: p. 1-15.
2. Holick, M.F., Vitamin D status: measurement, interpretation, and clinical application. Ann Epidemiol, 2009. 19(2): p. 73-8.
3. Kunz, C., et al., No improvement in vitamin D status in German infants and adolescents between 2009 and 2014 despite public recommendations to increase vitamin D intake in 2012. Eur J Nutr, 2019. 58(4): p. 1711-1722.
4. Lips, P., et al., Current vitamin D status in European and Middle East countries and strategies to prevent vitamin D deficiency: a position statement of the European Calcified Tissue Society. Eur J Endocrinol, 2019. 180(4): p. P23-P54.
5. Lips, P., R.T. de Jongh, and N.M. van Schoor, Trends in Vitamin D Status Around the World. JBMR Plus, 2021. 5(12): p. e10585.
6. Mazess, R.B., H.A. Bischoff-Ferrari, and B. Dawson-Hughes, Vitamin D: Bolus Is Bogus-A Narrative Review. JBMR Plus, 2021. 5(12): p. e10567.
7. Bischoff-Ferrari, H.A., et al., Fall prevention with supplemental and active forms of vitamin D: a meta-analysis of randomised controlled trials. Bmj, 2009. 339: p. b3692.
8. Bischoff-Ferrari, H.A., et al., A pooled analysis of vitamin D dose requirements for fracture prevention. N Engl J Med, 2012. 367(1): p. 40-9.
9. Weaver, C.M., et al., Kalzium plus vitamin D supplementation and risk of fractures: an updated meta-analysis from the National Osteoporosis Foundation. Osteoporos Int, 2016. 27(1): p. 367-76.
10. Bischoff-Ferrari, H.A., et al., Effect of Vitamin D Supplementation, Omega-3 Fatty Acid Supplementation, or a Strength-Training Exercise Program on Clinical Outcomes in Older Adults: The DO-HEALTH Randomized Clinical Trial. JAMA, 2020. 324(18): p. 1855-1868.
11. Bischoff-Ferrari, H.A., S. Bhasin, and J.E. Manson, Preventing Fractures and Falls: A Limited Role for Kalzium and Vitamin D Supplements? JAMA, 2018. 319(15): p. 1552-1553.
12. Zhao, J.G., et al., Association Between Kalzium or Vitamin D Supplementation and Fracture Incidence in Community-Dwelling Older Adults: A Systematic Review and Meta-analysis. JAMA, 2017. 318(24): p. 2466-2482.
13. Force, U.S.P.S.T., et al., Vitamin D, Kalzium, or Combined Supplementation for the Primary Prevention of Fractures in Community-Dwelling Adults: US Preventive Services Task Force Recommendation Statement. JAMA, 2018. 319(15): p. 1592-1599.
14. Bolland, M.J., A. Grey, and A. Avenell, Effects of vitamin D supplementation on musculoskeletal health: a systematic review, meta-analysis, and trial sequential analysis. Lancet Diabetes Endocrinol, 2018. 6(11): p. 847-858.
15. Bischoff-Ferrari, H.A., et al., Vitamin D supplementation and musculoskeletal health. Lancet Diabetes Endocrinol, 2019. 7(2): p. 85.
16. Bischoff-Ferrari, H.A., et al., Effect of high-dosage cholecalciferol and extended physiotherapy on complications after hip fracture: a randomized controlled trial. Arch Intern Med, 2010. 170(9): p. 813-20.
17. Sanders, K.M., et al., Annual high-dose oral vitamin D and falls and fractures in older women: a randomized controlled trial. JAMA, 2010. 303(18): p. 1815-22.
18. Hsu, S., et al., Effects of Vitamin D 3 Supplementation on Incident Fractures by eGFR in VITAL. Clin J Am Soc Nephrol, 2024. 19(5): p. 638-640.
19. Dawson-Hughes, B., et al., IOF position statement: vitamin D recommendations for older adults. Osteoporos Int, 2010. 21(7): p. 1151-4.
20. Holick, M.F., et al., Evaluation, treatment, and prevention of vitamin D deficiency: an Endocrine Society clinical practice guideline. J Clin Endocrinol Metab, 2011. 96(7): p. 1911-30.