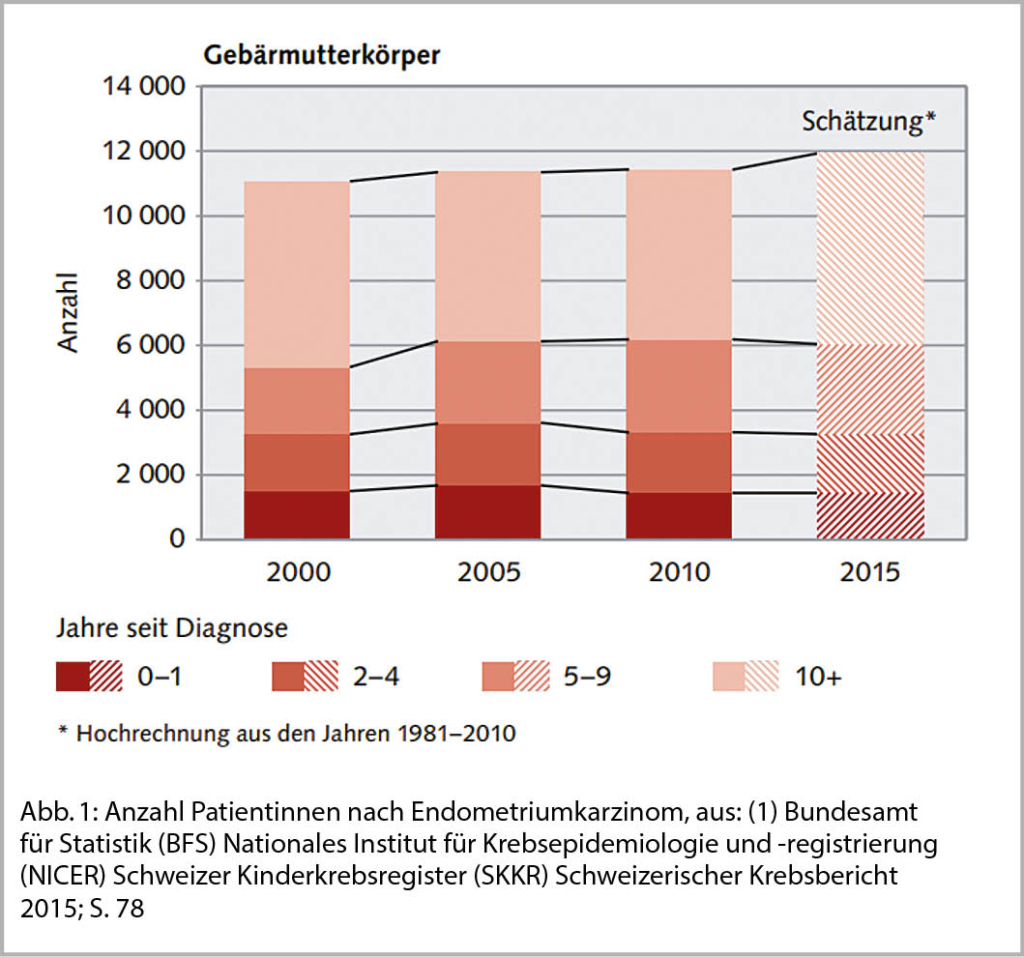
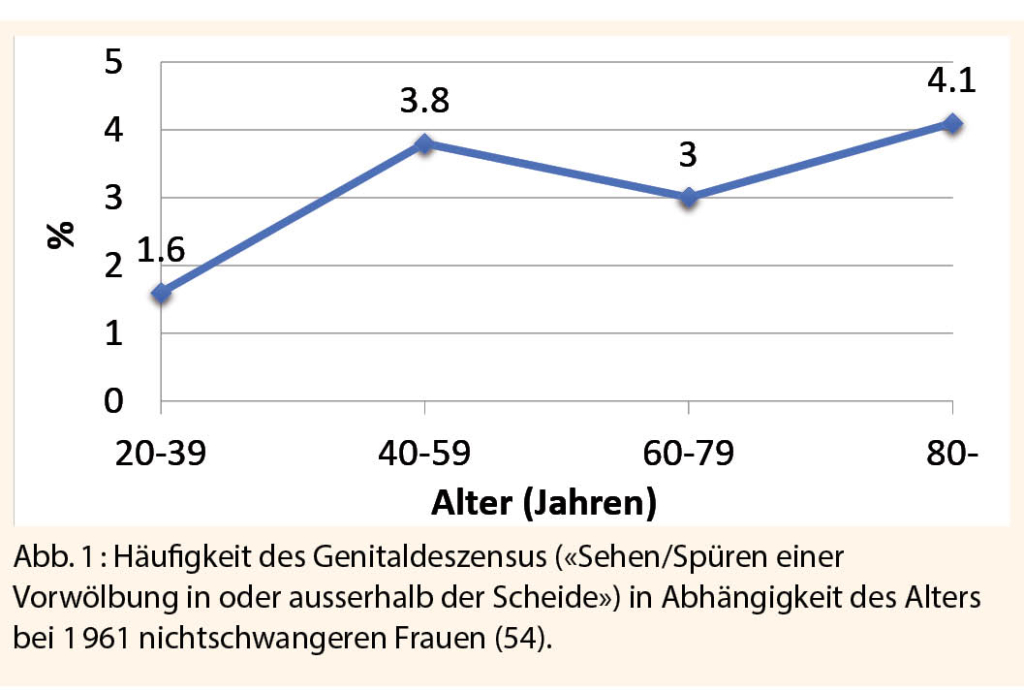
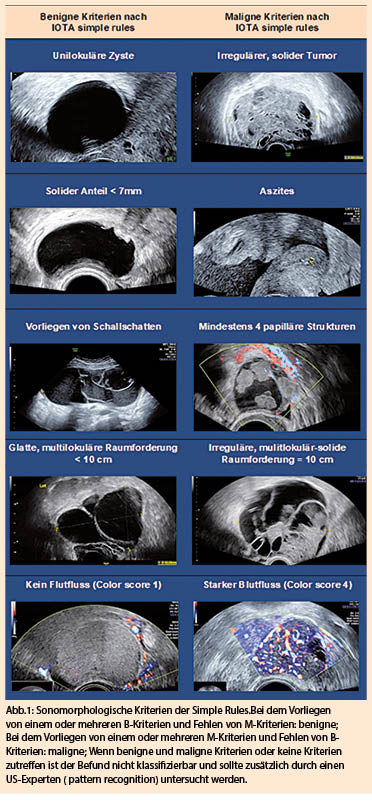
Auch wenn das Mammakarzinom die mittlerweile weltweit häufigste Tumorerkrankung der Frau ist, erkranken in der Schweiz gut 2000 Frauen pro Jahr an einem gynäkologischen Tumor, am häufigsten ist hierbei das Endometriumkarzinom zu nennen. Erfreulicherweise gehen bis auf das Ovarialkarzinom viele der gynäkologischen Tumorerkrankungen mit einer sehr guten Langzeitprognose einher. Auch wenn die Statistiken für die Nachsorgezahlen bislang lückenhaft sind, so leben aktuell in der Schweiz mehr als 15 000 Patientinnen nach einer gynäkologischen Tumorerkrankung, Tendenz steigend (s. Abb. 1). Der folgende Beitrag zeigt auf, was bei den verschiedenen gynäkologischen Tumorerkrankungen in der Nachsorge beachtet werden muss.
Aufgrund der geringen Fallzahlen liegen für das Vulva- oder Vaginalkarzinom keine eidgenössischen Zahlen vor. Die grosse Anzahl an Patientinnen in der Nachsorge ist multifaktoriell. Hohe 5-Jahres-Überlebensraten hat mit 70% das Zervixkarzinom und 77% das Endometriumkarzinom, die 10-Jahres-Überlebensraten vervollständigen diese Tendenz mit 70% für das Endometriumkarzinom und 60% für das Zervixkarzinom. Deutlich schlechter sehen die 5-Jahres-Überlebensraten nach wie vor für das Ovarialkarzinom mit nur 40% aus. Auch wenn die 10-Jahres-Überlebensrate zwischen 1998 und 2012 um 4% gestiegen ist, liegt sie nach wie vor nur bei 26% (1).
Nach Abschluss der Primärbehandlung, die sowohl rein lokoregionär als auch ergänzend systemisch sein kann, beginnt die Tumornachsorge. Während wir es bei Patientinnen mit Mammakarzinom bereits seit langem gewohnt sind, Erhaltungstherapien wie die antihormonelle Therapie zu begleiten, ist dies in den letzten Jahren auch bei den gynäkologischen Tumoren (z.B. PARP-Inhibitoren beim Ovarialkarzinom) Teil der Nachsorge geworden.
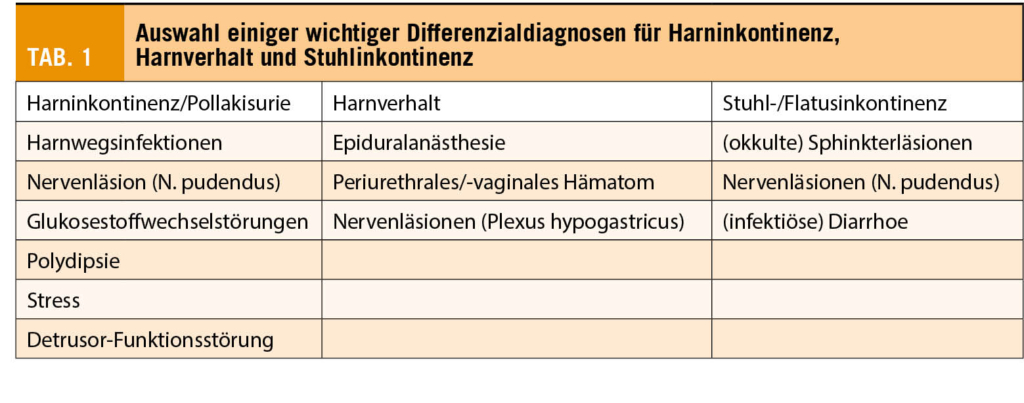
Auch wenn für jede Tumorentität Nachsorgeschemata vorliegen (2-5), basieren diese mehr auf Expertenmeinungen, als auf prospektiv randomisierten Studien. Bei allen Tumorentitäten ist in den ersten 3 Jahren das Kontrollintervall 3-monatlich empfohlen, gefolgt von 6-monatlichen Kontrollen in den Jahren 4 und 5. Danach sind in der Regel jährliche Kontrollen empfohlen. Es gilt diese Nachsorgeschemata eher als richtungsweisende Leitplanken zu sehen und inhaltlich mit den individuellen Bedürfnissen der Patientinnen zu füllen. Der Verlust in das Vertrauen des eigenen Körpers, die intensivere Auseinandersetzung mit sich selbst, der Prognose und die Angst vor dem Rezidiv führt bei vielen Patientinnen zu dem Wunsch nach einer intensiven Nachsorge mit regelmässiger Bildgebung und der Bestimmung von Tumormarkern (6). Eine Verschlechterung der Lebensqualität nach abgeschlossener Primärtherapie zeigt sich nicht nur bedingt durch anhaltende Einschränkungen durch die Primärtherapie, die Angst vor dem Rezidiv, sondern auch durch vermehrte Schlafstörungen, Depressionen und Fatigue. Da es auch mit noch so regelmässiger Nachsorge nicht möglich ist das Rezidiv zu verhindern, sollte der Focus vielmehr darauf liegen die Parameter zu beeinflussen, die die Lebensqualität verbessern und die Therapieadhärenz für Langzeittherapien oder Verbesserung des Lebensstils zu unterstützen. Validierte Tests und Screeningverfahren zur Erfassung der psychosozialen Belastung sollten genutzt werden. Unter Beachtung dieser Aspekte ist sicher die Zusammenstellung in Tabelle 1 hilfreich, die nicht auf apparative oder laborchemische Parameter focussiert, sondern die bio-psycho-sozialen Faktoren und die Compliancesteigerung sowie Aufarbeitung der bisherigen Therapien in das Zentrum der Nachsorge stellt (7).
Endometriumkarzinom
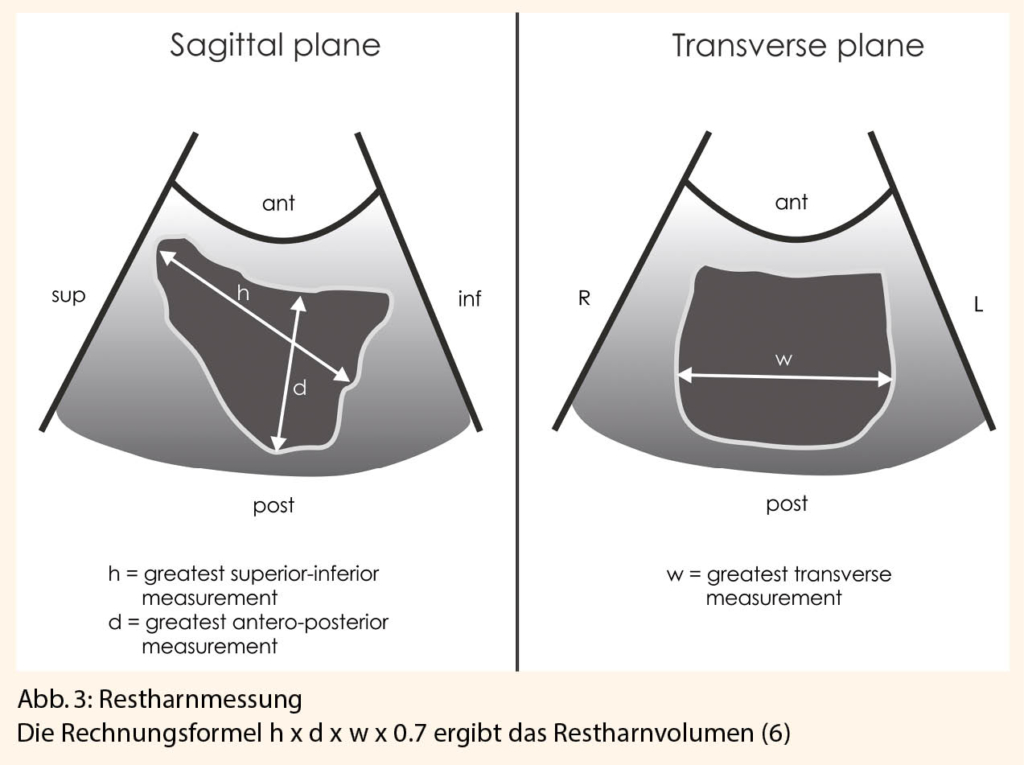
Ziel der Nachsorge beim Endometriumkarzinom ist das frühe Erkennen eines erneut kurativ behandelbaren Lokalrezidivs. Das Risiko dafür ist mit 13 % sehr gering, bei Patientinnen mit einem Niedrigrisikokarzinom in der Primärdiagnose sogar bei < 3 %. In der körperlichen Untersuchung inklusive Allgemeinstatus, gynäkologischer Spekulumeinstellung und rektovaginaler Palpation sowie Vaginalsonographie beziehungsweise Sonographie der ableitenden Harnwege ist die Erkennung eines Rezidivs oder Spätfolgen der Therapie möglich. Bedenkt man die problemlose Verfügbarkeit des Ultraschalls in der gynäkologischen Sprechstunde, die einfache Anwendung und die fehlende Strahlenbelastung zeigt diese Untersuchung zahlreiche Vorteile (8). In einigen Studien konnte eine Detektionsrate für Vaginalrezidive durch die gynäkologische Untersuchung inklusive rektovaginaler Palpation von 35–68 % ohne weitere apparative Diagnostik erzielt werden (9). Der zytologische Abstrich hingegen wird beim Endometriumkarzinom nicht empfohlen, da er nicht kosteneffizient ist und in nur ca. 10 % zur Diagnose beim asymptomatischen Rezidiv führt (10). Kritisch hinterfragen muss man, ob die frühzeitige Diagnose eines asymptomatischen Rezidivs sinnvoll ist. In Studien konnte bislang nicht gezeigt werden, dass die Behandlung von asymptomatischen Rezidiven zu einer Verlängerung des Überlebens führt. Vor allem die Diagnose von asymptomatischen Fernmetastasen führt hingegen zu einer Verschlechterung der Lebensqualität ohne das Gesamtüberleben zu verbessern (11). Da mehr als die Hälfte aller Patientinnen mit einem Rezidiv Beschwerden wie vaginale Blutungen, unspezifische Abdominalbeschwerden, Gewichtsverlust, Lymphödem oder persistierenden Husten äussern, ist das ärztliche Gespräch mit dem gezielten Nachfragen und Zuhören weiterhin wichtiger Bestandteil der Tumornachsorge.
Zervixkarzinom
Abhängig vom Tumorstadium steigt das Rezidivrisiko beim Zervixkarzinom und liegt ab dem FIGO Stadium ≥ IIB bereits bei 25%, ein Grossteil der Rezidive tritt dabei innerhalb der ersten 2 Jahre auf (12). Das lokale Rezidiv äussert sich in der Mehrzahl der Fälle mit Symptomen wie Ausfluss, Blutungen, Schmerzen und Lymphödem. Patientinnen mit Metastasen haben häufiger unspezifische Symptome. Auch wenn das Lokalrezidiv erneut kurativ behandelt werden kann und daher in der Nachsorge Ziel der klinischen Untersuchung ist, sind die Überlebensraten nach Therapie eines Rezidivs sehr ernüchternd.
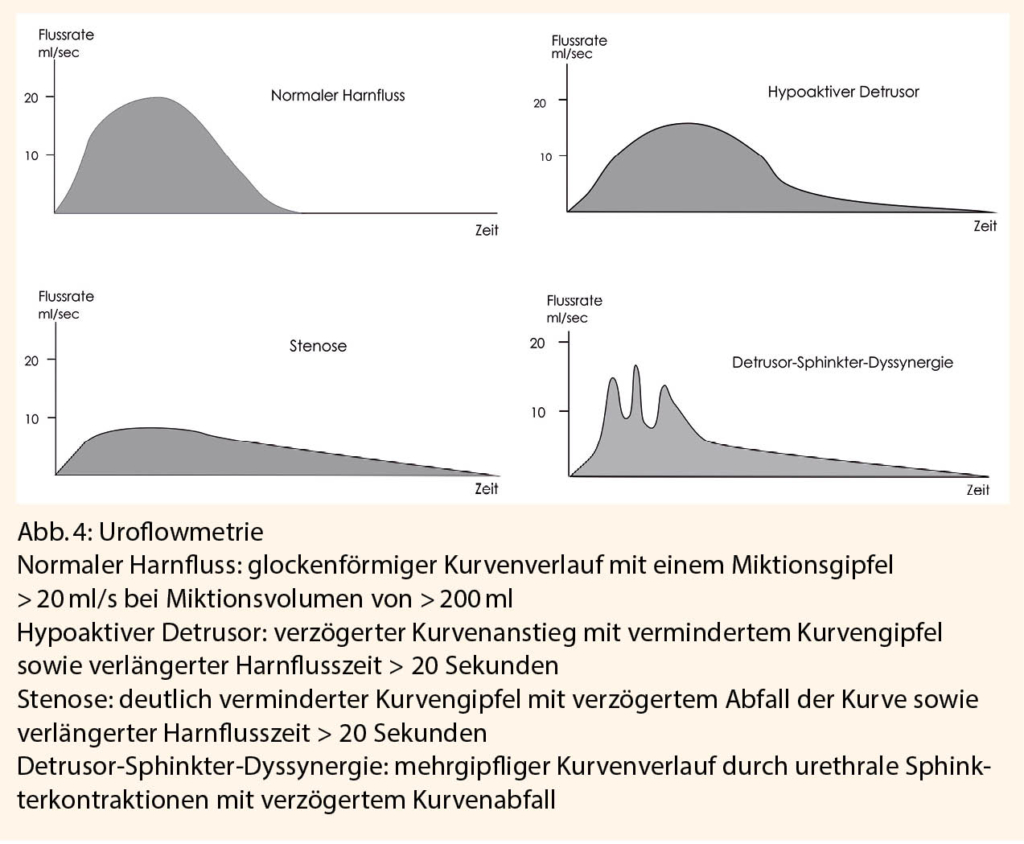
Der Nutzen der Zervixzytologie wird kontrovers diskutiert. Nach Radio-(Chemo-)Therapie ist der Abstrich in gut einem Drittel der Fälle pathologisch, aber nur etwa 8 % aller Lokalrezidive werden mit der Zytologie diagnostiziert. Rimel et al folgern daher in ihrer Studie, dass ein PAP-Resultat mit ASC-H oder LSIL ohne sichtbare Veränderungen ohne Kolposkopie im Rahmen des normalen Nachsorgerhythmus weiterkontrolliert werden kann, bis eine höhergradige Läsion auftritt (13). Ebenfalls ist die HPV-Bestimmung speziellen Fragestellungen vorbehalten (3). Der Ultraschall kann nicht nur Komplikationen der Primärtherapie wie Restharn oder Nierenstauung diagnostizieren, sondern kann auch Gewebezunahme im kleinen Becken oder Aszites zeigen. Dennoch gilt auch diese Untersuchung nur als fakultativ.
Ovarialkarzinom
In der Nachsorge des Ovarialkarzinoms ist man als nachbetreuender Arzt aufgrund der schlechten Überlebensraten und der Sorge vor dem Rezidiv sicher am häufigsten mit dem Wunsch nach Bildgebung und Tumormarkerkontrollen konfrontiert. Dies in der Regel mit der Vorstellung von Seiten der Patientin ein Rezidiv frühzeitig erkennen und behandeln zu können. Die routinemässige Kontrolle des CA 125 führt aber bislang nicht zu einer Verlängerung des Überlebens (14). Im Gegenteil bewirkt es nur, dass das frühzeitige Erkennen des asymptomatischen Rezidivs früher mit einer erneuten Chemotherapie behandelt wird, die zu einer schlechteren Lebensqualität führt. Diese verschlechterte Lebensqualität ist nicht nur allein bedingt durch die Nebenwirkungen der Therapie, sondern auch durch die Konfrontation mit dem Wissen um das Rezidiv und die damit verschlechterte Prognose. Unbestritten ist auch beim Ovarialkarzinom der Einsatz der Bildgebung bei einem Verdacht auf ein Rezidiv.
Vulva- und Vaginalkarzinom
Diese beiden Karzinome stellen die seltenen gynäkologischen Karzinome dar, die aber in den vergangenen 20 Jahren nicht nur in Deutschland, sondern auch in anderen europäischen Ländern eine deutliche Zunahme bei Patientinnen unter 50 Jahren gezeigt haben (15). Grundsätzlich haben beide Karzinome in den frühen Tumorstadien, in denen sie meistens entdeckt werden, gute Überlebensraten mit 93% (Stadium I) und 71% (Stadium II) Gesamtüberleben. Auch bei diesen Tumoren können Lokalrezidive erneut kurativ behandelt werden. Der Unterschied in der Prognose des Rezidivs ist bei diesen Tumoren eindrücklich von der Lokalisation abhängig. Während Lokalrezidive eine 5-Jahresüberlebensrate von 50 % haben, liegt dies bereits beim Leisten- oder Beckenrezidiv nur noch bei 27 % (16). Neben dem Gespräch steht somit die gynäkologische Speculumuntersuchung und bimanuelle Palpation im Zentrum der Nachsorge. Eine Kolposkopie ist grosszügig bei geringen Auffälligkeiten einzusetzen. Obwohl es keine Beweise aus Studien gibt, dass die regelmässige Zytologie der Vagina sinnvoll ist, erachten einige Autoren nach der Therapie von HPV-positiven Tumoren der Vagina die Zytologie und HPV-Analyse als indiziert (17). Weiterführende Bildgebung ist auch bei diesen Tumoren ohne den Verdacht auf ein Rezidiv oder Metastasen nicht angemessen.
Bedingt durch die Primärtherapie ist neben der allgemeinen Anamnese das Erfragen von psychosexuellen Beeinträchtigungen, Missempfindungen, Blutungen und vaginalem Fluor bei diesen Patientinnen besonders wichtig. Da Patientinnen dies oft tabuisieren, ist es Aufgabe der nachbehandelnden Ärztin, dies aktiv anzusprechen.
Copyright bei Aerzteverlag medinfo AG
Stadtspital Triemli
Frauenklinik
Birmensdorferstrasse 501
8063 Zürich
heike.passmann@triemli.zuerich.ch
Die Autorin hat in Zusammenhang mit diesem Artikel keine Interessenskonflikte deklariert.
1 Bundesamt für Statistik (BFS) Nationales Institut für Krebsepidemiologie und -registrierung (NICER) Schweizer Kinderkrebsregister (SKKR) Schweizerischer Krebsbericht 2015
2 Leitlinienprogramm Onkologie (Deutsche Krebs-gesellschaft, Deutsche Krebshilfe, AWMF) 2018.S3-Leitlinie Diagnostik, Therapie und Nachsorge der Patientinnen mit Endometriumkarzinom, Langversion 0.1, 2018, AWMF Registernummer: 032/034-OL.
3 Leitlinienprogramm Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF) 2021 S3-Leitlinie Diagnostik, Therapie und Nachsorge der Patientin mit Zervixkarzinom Langversion 2.1 – Mai 2021 AWMF-Registernummer: 032/033OL
4 Leitlinienprogramm Onkologie (Deutsche Krebs-gesellschaft, Deutsche Krebshilfe, AWMF) 2020. S3-Leitlinie Diagnostik, Therapie und Nachsorge maligner Ovarialtumoren Version 4.0- März 2020 AWMF-Registernummer: 032/035OL
5 Deutsche Gesellschaft für Gynäkologie und Geburtshilfe, S2k-Leitlinie Vulvakarzinom und seine Vorstufen, Diagnostik und Therapie. AWMF-Registernummer 015/059, August 2015
6 Brandenbarga D, Berendsen A.J., et al. Patients’ expectations and preferences regarding cancer follow-up care; Maturitas, Volume 105, November 2017, Pages 58-63
7 Sehouli J, Armbrust R, Alle Aspekte der Nachsorge in der gynäkologischen Onkologie am Beispiel des Ovarialkarzinoms; Gynäkologie 2021; 54:99-106
8 Testa AC et al (2005) The role of sonographic examination in the follow up of gynecological neoplasms. Gynecol Oncol 99 (3): 696-703
9 Salani, R. Recurrence patterns and surveillance for patients with early stage
endometrial cancer. Gynecol Oncol, 2011. 123(2): p. 205-7.
10 Bristow RE et al Cost effectiveness of routine vaginal cytology for endometrial cancer surveillance. Gynecol Oncol 2006.103(2): 709-713
11 Gadducci, A. An intensive follow-up does not change survival of patients with clinical stage I endometrial cancer. Anticancer Res, 2000. 20(3B): 1977-84.
12 Bodurka-Bevers, D. Posttherapy surveillance of women with cervical cancer: an outcomes analysis. Gynecol Oncol, 2000. 78(2): 187-93.
13 Rimel, B.J., et al., Cervicovaginal cytology in the detection of recurrence after cervical cancer treatment. Obstet Gynecol, 2011. 118(3): 548-53.
14 Rustin GJ et al. Early versus delayed treatment of relapsed ovarian cancer: a randomized trial. Lancet 2010; 376(9747): 1155-1163
15 Zentrum für Krebsregisterdaten im Robert-Koch-Institut (2016) Bericht zum Krebesgeschehen in Deutschland 2016
16 Maggione T et al. Patterns of recurrence in patients with squamous cell carcinoma of the vulva. A multicenter ctf study. Cancer 2000 89:116-122
17 Forner DR, Dannecker C. Nachsorge bei Vulva und Vaginalkarzinom. Gynäkologe 2021; 54:94-98