Jugendliche und junge Erwachsene mit Krebs zeigen besondere Bedürfnisse auf, werden aber in der Medizin nicht als eigene Interessensgruppe wahrgenommen, sondern zusammen mit Kindern oder mit Erwachsenen behandelt. In diesem Beitrag wurde daher durch eine Interviewstudie näher untersucht, wo Jugendliche und junge Erwachsene (insbesondere im Alter von 16 bis 18 Jahren) in der Schweiz behandelt werden sowie die Vor- und Nachteile der verschiedenen Vorgehensweisen näher betrachtet.
Adolescents and young adults with cancer have special needs but are not recognized as a separate interest group in medicine but are treated together with children or adults. This article therefore used an interview study to analyze in more detail where adolescents and young adults (particularly those aged 16 to 18) are treated in Switzerland and to take a closer look at the advantages and disadvantages of the various approaches.
Key Words: AYA, Krebs, pädiatrische Onkologie, hochspezialisierte Medizin
Einleitung
Jugendliche und junge Erwachsene mit Krebs im Alter von 15-39 Jahren werden als AYA (engl. adolescents and young adults) bezeichnet (1). Der vorliegende Beitrag fokussiert sich auf die untersuchte Altersgruppe von 16- bis 18-jährigen Patient/-innen und bezeichnet diese als AYA. Krebs bei AYA ist selten (2). Die pädiatrische Onkologie gehört aufgrund der geringen Fallzahlen und der komplexen Behandlungsverfahren, verbunden mit einem hohen personellen und technischen Aufwand, zur hochspezialisierten Medizin (HSM) (3).
AYA haben besondere Bedürfnisse, die sich von denjenigen der Kinder und auch von Erwachsenen unterscheiden. Im Ausland, z.B. in den USA, gibt es deshalb eigene AYA-Zentren, die an die Erwachsenenonkologie (4) oder an die Pädiatrie (5) angegliedert sind. In der Schweiz werden AYA hingegen nicht als eigene Interessensgruppe in der Medizin wahrgenommen, sondern entweder zusammen mit Kindern oder mit Erwachsenen behandelt (6). Es bestehen keine klaren gesetzlichen Regelungen, ob AYA in der Schweiz in einem Kinderonkologiezentrum oder auf der Erwachsenenstation behandelt werden. Der vorliegende Beitrag stellt die durchgeführte Interviewstudie vor, mit der Forschungsfrage: «Wo werden AYA – insbesondere 16- bis 18-jährige – mit Krebserkrankungen in der Schweiz behandelt?». Zudem wurden die Vor- und Nachteile der verschiedenen Vorgehensweisen näher betrachtet.
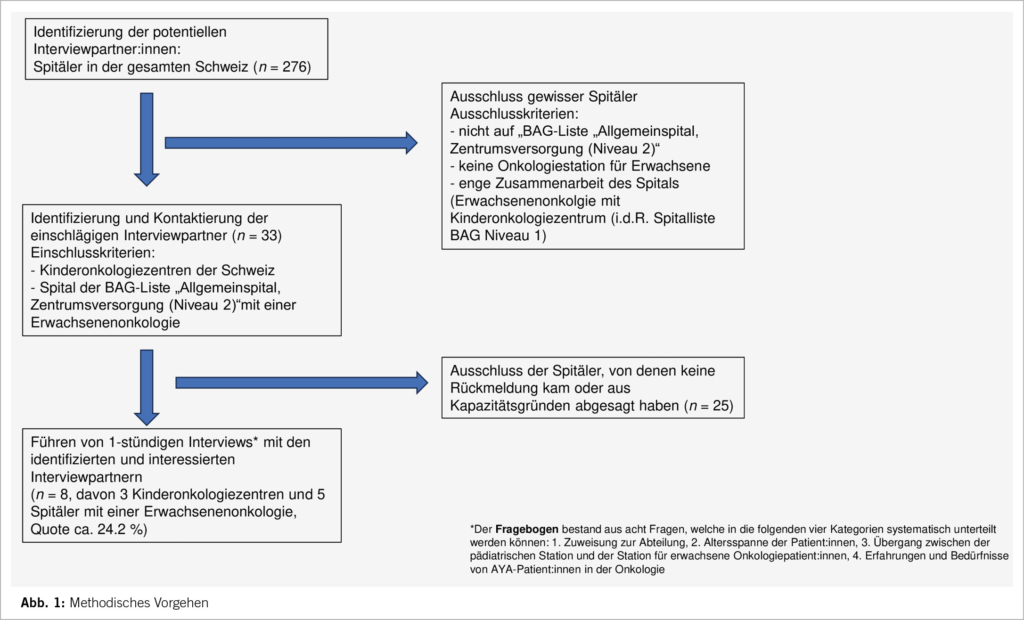
Methodisches Vorgehen
Zur Beantwortung der Forschungsfrage, auf welchen Abteilungen AYA behandelt werden, wurden Interviews mit Spitälern in der Schweiz durchgeführt. Es wurden insgesamt 33 Spitäler kontaktiert. Mit acht Spitälern kam ein Interview zustande. Das detaillierte Vorgehen kann der Grafik entnommen werden (Abb. 1).
Heterogener Umgang mit AYA
Aus den Interviews ergab sich, dass die Zuweisung zur jeweiligen Abteilung unterschiedlich erfolgen kann. Einerseits werden AYA in erster Linie durch den Hausarzt/die Hausärztin überwiesen. Andererseits kann eine Zuweisung auch durch eine spezialisierte Fachperson innerhalb der Behandlungsstätte erfolgen. Schliesslich kann eine Zuweisung auch im Rahmen eines Transitionsgesprächs stattfinden. Damit soll insbesondere auch die Nachsorge gewährleistet werden.
Die Befragung dazu, über welche Altersspanne Patient/-innen auf der jeweiligen Station behandelt werden oder werden sollten, hat ergeben, dass hier ein Graubereich besteht. Grundsätzlich ist das Alter ein formales Zuweisungskriterium, und die Kinderonkologie nimmt Patient/-innen bis 18 Jahre auf, während auf der Erwachsenenonkologie Patient/-innen ab 18 Jahren behandelt werden. Dieses Vorgehen entspricht auch den Vorgaben der HSM. Von dieser starren Altersgrenze gibt es in der Praxis jedoch Abweichungen. Ein Spital vermutet diese Abweichung aufgrund der erst kürzlich erfolgten Anhebung der Altersgrenze von 16 auf 18 Jahre. Aus den Interviews hat sich einstimmig ergeben, dass das Alter eine künstliche Abgrenzung für die Zuweisung darstellt und starre Vorgaben zur Zuweisung allein aufgrund des Alters unerwünscht sind. Vielmehr ist die Tumorart ausschlaggebend, nämlich ob es sich um einen typischen Kinder- bzw. Erwachsenentumor handelt.
Ein inoffizielles Kriterium der Zuweisung von AYA stellt die psychosoziale Situation der Patient/-innen dar. Je nach Autonomiebedürfnis und Grad der Selbständigkeit sind Patient/-innen in der Pädiatrie oder in der Erwachsenenonkologie besser aufgehoben, was von den Expert/-innen gemäss eigenen Angaben auch berücksichtigt wird. Alle Interviewpartner/-innen haben betont, dass eine Einzelfallbetrachtung notwendig ist und die individuellen Bedürfnisse der Patient/-innen im Vordergrund berücksichtigt werden sollten.
Übergang zwischen der pädiatrischen Station und der Station für erwachsene Onkologiepatient/-innen
Die Befragung der Spitäler verdeutlichte eine unterschiedliche Handhabung des Übergangs von AYA aus einer pädiatrischen Onkologiestation zu einer Onkologiestation für Erwachsene. Der Ablauf hängt insbesondere von der internen Spitalorganisation und Vernetzung zwischen den einzelnen Onkologiezentren ab.
Es gaben fünf von acht Spitälern an, sie hätten kein Standard-Prozedere für den Übergang. Der Übergang würde in diesen Spitälern durch die Kinderonkologie an die Hand genommen. Dazu kontaktiere das behandelnde ärztliche Personal der pädiatrischen Onkologie die zukünftig behandelnden Mediziner/-innen der Erwachsenenonkologie und vereinbarte eine Sprechstunde für die betroffene Person. Betont wurde auch die aktive Unterstützung der AYA beim Übergang. In diesen fünf Spitälern finden jedoch regelmässig interdisziplinäre Tumorboards statt. Ein drittes der fünf Spitäler (Erwachsenenonkologie) berichtete zudem den Beizug einer externen Fachärztin zur Übernahme der Nachsorge bei Erwachsenen, die in der Kindheit eine Krebserkrankung hatten.
In drei der befragten Spitäler etablierten sich sogenannte Transitionssprechstunden. Die Kinderonkologie begleitet die betroffenen AYA eng beim Übergang in die Erwachsenenonkologie. Der Übertritt wird bereits ein Jahr im Voraus geplant, wobei Mediziner/-innen der pädiatrischen Onkologie und der Erwachsenenonkologie zusammen mit den Betroffenen eine gemeinsame Sprechstunde abhalten, in welcher auch das weitere Vorgehen geplant wird und im sog. Survivorship Care Plan festgehalten wird. Es werden insgesamt zwei gemeinsame Sprechstunden organisiert, wobei diese vor dem Übertritt in die Kinderonkologie und im ersten Jahr danach auf die Erwachsenenonkologie abgehalten werden. Zwei weitere Spitäler, welche die Transitionssprechstunden nicht anbieten, haben zudem berichtet, dass sie das Konzept kennen und grundsätzlich begrüssen würden, allerdings die Fallzahlen in ihrem Spital zu gering wären, dass es sich lohnen würde.
Alle befragten Spitäler gaben an, dass unter Umständen auch über 18-Jährige während einer laufenden Behandlung auf einer pädiatrischen Station verbleiben dürfen. Es wurde zudem ausgeführt, dass in der Regel die Nachsorge von Kinderkrebsbetroffenen im Kinderonkologiezentrum bleibt.
Die Expert/-innen äusserten zudem, ausser den standesrechtlichen Empfehlungen keine Kenntnis von spitalübergreifenden oder gar schweizweiten schriftlichen Vorgaben zu Follow-up-Richtlinien zu haben. Gemäss ihrer Kenntnis sei der Übergang spitalintern geregelt und eine Einzelfallbetrachtung. Eine Ausnahme bilden die Transitionssprechstunden mit dem Survivorship Care Plan.
Erfahrungen und Bedürfnisse von AYA-Patient/-innen in der Onkologie
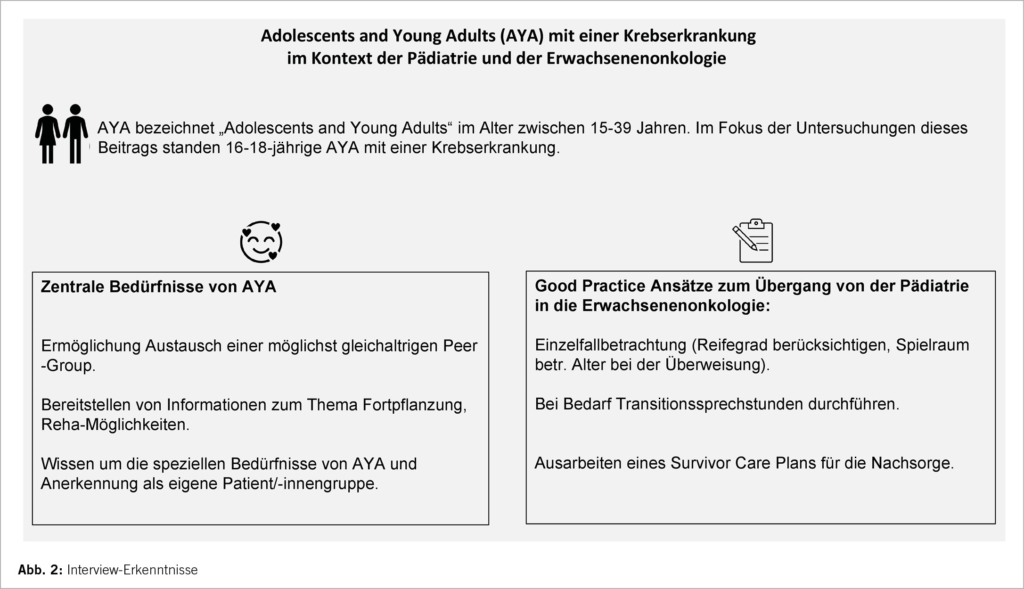
Die befragten Spitäler anerkennen alle, dass AYA im Alter von 16 bis 18 spezielle Bedürfnisse haben.
Das am häufigsten genannte Bedürfnis betrifft die Physioonkologie während der Behandlung bzw. Reha nach der Behandlung. Insgesamt sprach sich die Hälfte der befragten Spitäler für die Wichtigkeit von Angeboten für AYA im Rahmen von Physiotherapie und Reha aus. Auch internationale Zusammenarbeiten seien interessant, weil beispielsweise in Deutschland Angebote bestünden, die Kinder und junge Erwachsene in eigene Interessensgruppen bei der Reha aufteilten. Drei der befürwortenden Spitäler erklärten, dass es im Rahmen von Reha-Behandlungen bei AYA oft zu Problemen mit der Kostenübernahme durch die Krankenkasse käme.
Vier der befragten Spitäler sprachen sich für die Stärkung der Reproduktionsmedizin für AYA in Folge einer Krebsbehandlung aus. So könnte beispielsweise ein interdisziplinäres Team sich auch schon bei AYA verstärkt mit Fragen der Reproduktionsmedizin auseinandersetzen und AYA entsprechend aufklären.
Drei Spitäler bewerteten die Psychoonkologie zur Stärkung der psychischen Stabilität und des Selbstbewusstseins als wichtig. Insbesondere wurde von zwei Spitälern der Austausch in einer AYA-Peer-Group positiv gewertet.
Als klarer Vorteil für die Behandlung von AYA auf einer Kinderonkologie wird von drei Expert/-innen angegeben, dass die pädiatrischen Stationen einen anderen Stellenschlüssel für das Personal haben. Ausserdem sei das Betreuungsteam der pädiatrischen Kliniken interdisziplinärer aufgestellt und es seien mehr Ressourcen vorhanden. Diese Massnahmen fördern die Patient/-innen intensiver und holistischer.
Als Vorteil von Behandlungen von AYA auf Erwachsenenstationen wurde hingegen angegeben, dass AYA eher auf Augenhöhe wahrgenommen werden. Es wurde berichtet, dass AYA in der Erwachsenenonkologie in der Regel autonomer sind und bspw. ohne Begleitung der Eltern zur Nachsorge kommen und sich daher viel offener zu ihren Problemen äussern können.
Zur Frage, ob eigene Abteilungen oder Zentren für AYA mit Krebs geschaffen werden sollten, besteht Zurückhaltung. Kritik bestand seitens eines Spitals insbesondere daran, dass sich eigene Units aufgrund der verhältnismässig kleinen Zahlen von Patient/-innen nicht lohnen würden. Wenn es eine eigene Unit für AYA gäbe, wäre laut diesem Spital eine Anlaufstelle in der Schweiz genügend. Die weiteren Meinungen zur Ausgestaltung von Angeboten für AYA divergierten ebenfalls stark: Ein Spital schlug eine spezielle AYA-Sprechstunde vor. Zwei weitere Spitäler waren der Meinung, dass dem Wunsch von AYA-Patient:innen, auf welcher Station sie behandelt werden möchten, Rechnung getragen werden sollte. Ein anderes Spital erklärte, dass die Altersgrenze nicht auf 16 bis 18 Jahre beschränkt sein sollte, sondern Patient/-innen bis zu 25 Jahren umfassen müsste, damit auch weitere Krebserkrankungen, wie Brustkrebs, beinhaltet seien (Abb. 2).
Copyright bei Aerzteverlag medinfo AG
Kompetenzzentrum Medizin – Ethik – Recht Helvetiae (MERH)
Universität Zürich
Rechtswissenschaftliche Fakultät
Freiestrasse 15
8032 Zürich
Kompetenzzentrum Medizin – Ethik – Recht Helvetiae (MERH)
Universität Zürich
Rechtswissenschaftliche Fakultät
Freiestrasse 15
8032 Zürich
Kompetenzzentrum Medizin – Ethik – Recht Helvetiae (MERH)
Universität Zürich
Rechtswissenschaftliche Fakultät
Freiestrasse 15
8032 Zürich
Die Autorinnen haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Vgl. Internet: <https://jamanetwork.com/journals/jamaoncology/fullarticle/2800540>, zuletzt besucht am 22.05.2023.
2. Jährlich erkranken ca. 340 Kinder und Jugendliche (im Alter von 0-19 Jahren) an Krebs in der Schweiz, vgl. Internet: <https://www.kinderkrebs-schweiz.ch/aktuell/uebersicht-kampagnen/mein-kind-hat-krebs>, zuletzt besucht am 29.04.2023; <https://www.kinderkrebsregister.ch/statistiken-und-berichte/#:~:text=Krebs%20bei%20Kindern%20und%20Jugendlichen,Schweiz%20eine%20Krebserkrankung%20diagnostiziert%20wurde.>, zuletzt besucht am 22.05.2023.
3. Gesundheitsdirektion (GDK) Erläuternder Bericht für die Zuordnung des Bereichs zur hochspezialisierten Medizin vom 26.08.2021, S. 16, <https://www.gdk-cds.ch/fileadmin/docs/public/gdk/themen/hsm/HSM-Bereiche/BT_PaedOnco_Re1_Zuord_SchlussBT_Pub_20210907_def_d.pdf>, zuletzt besucht am 22.05.2023 (nachfolgend: GDK, Erläuternder Bericht, S. …).
4. PeterMac Center, Melbourne, USA, <https://www.petermac.org/patients-and-carers/children-and-young-people/adolescents-and-young-adults-aya-for-patients>, zuletzt besucht am 22.01.2024
5. UT Health San Antonio, Department of Pediatrics, Texas, USA <https://lsom.uthscsa.edu/pediatrics/divisions/hematology-oncology/clinical-programs/adolescent-and-young-adult-program/>, zuletzt besucht am 22.01.2024
6. Zum Ganzen STAUDINGER SINA, Unterstützungsprogramme für junge Krebspatienten, in: Schweizerische Zeitschrift für Sozialversicherung und berufliche Vorsorge, 2020, S. 17.