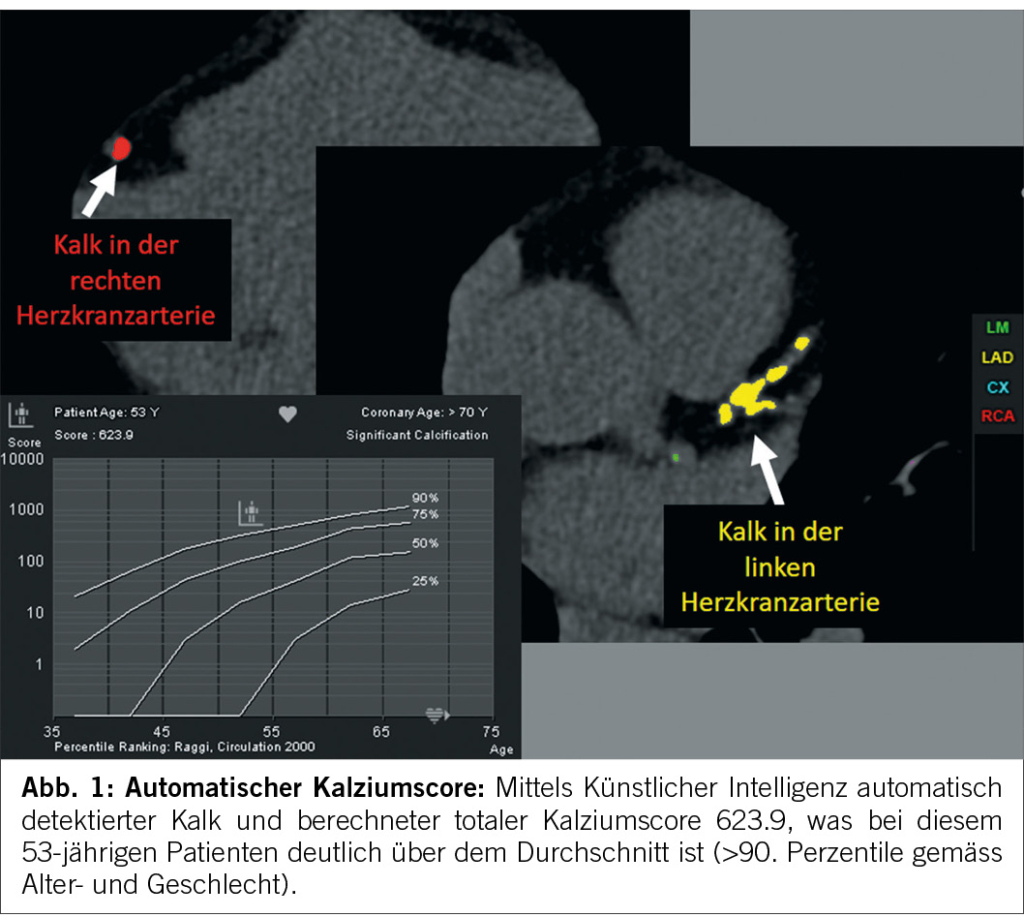
Manche Ansätze, die ursprünglich nur für Forschungszwecke entwickelt wurden, haben später ihren Weg in kommerzielle Produkte gefunden und sind bereits im klinischen Alltag im Einsatz. Ein Beispiel für eine bereits eingesetzte Methode ist die automatische Erkennung der Koronarverkalkung im nativen CT, um den Kalziumscore automatisch zu berechnen. Hier werden Voxel, die eine Abschwächung von 130 Hounsfield Units oder mehr aufweisen, automatisch markiert und dem korrekten Koronargefäss zugeordnet. Am Ende wird der Kalziumscore automatisch berechnet und in Relation gesetzt zu den Perzentilen gemäss Alter und Geschlecht (Abb. 1). Dies dient der schnellen Risikostratifizierung, insbesondere von Patienten, bei denen die Entscheidung bezüglich einer Statintherapie aufgrund der Laborwerte und klinischen Daten allein ungenügend ist.
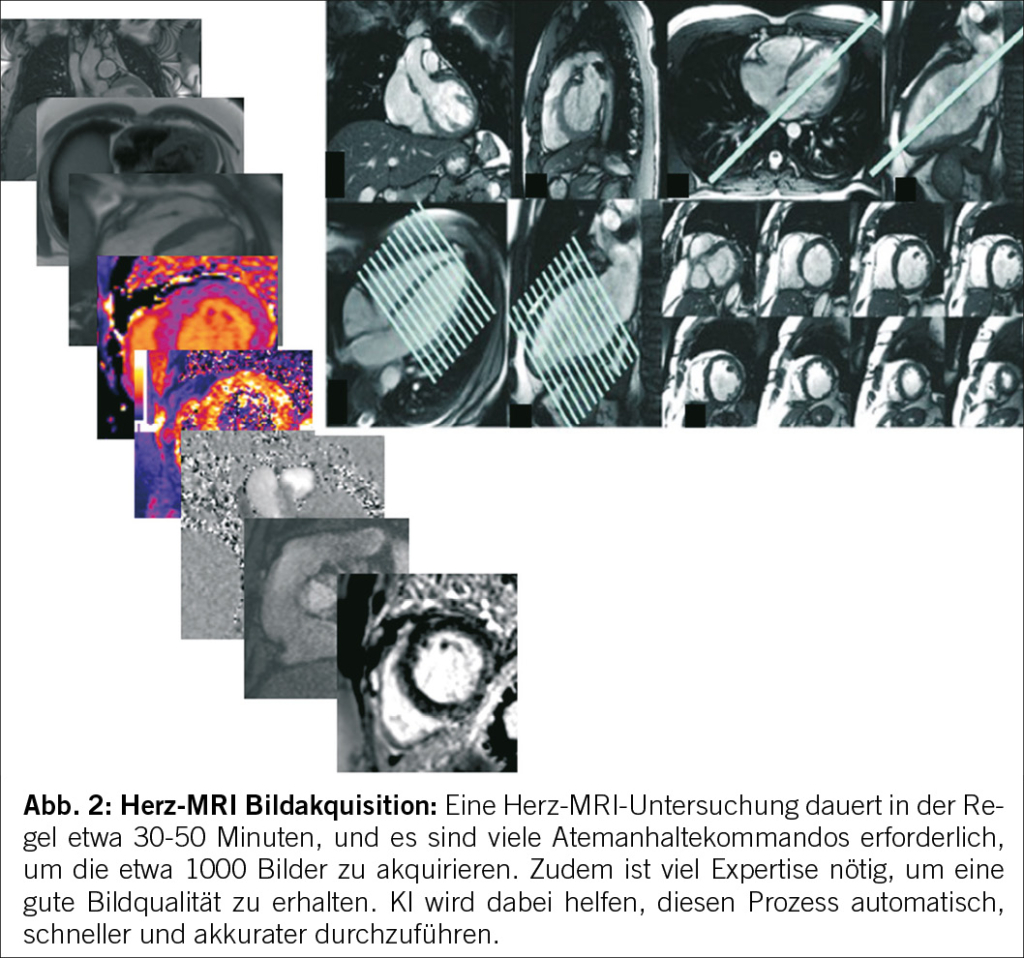
Eine andere Anwendung von KI ist im Bereich des Herz-MRIs. Bei einer Herz-MRI-Untersuchung werden circa 1000 Bilder in verschiedenen Ebenen und mit unterschiedlichen Sequenzen aufgenommen, die viele Atemanhaltekommandos erfordern. Die Planung dieser Untersuchung ist komplex und nur für speziell ausgebildete und erfahrene Ärzte und Radiologiefachpersonen möglich (Abb. 2). Eine schnellere Untersuchungszeit wäre hier natürlich wünschenswert. Der neue Algorithmus von Heart Vista soll hier Abhilfe schaffen und dabei helfen, Herz-MRI-Untersuchungen mit weniger Fachkenntnissen und deutlich schneller durchzuführen. Dies wird unter dem Slogan «One Click MRI» beworben, wobei das neue Produkt bis zu sechsmal schneller ist als wenn ein Mensch die MRI Untersuchung durchführt, zudem weniger oder sogar keine Atemkommandos benötigt und deutlich weniger Artefakte, insbesondere bei Arrhythmien aufweist. Ein weiteres Herz- MRI Beispiel ist die automatische Segmentierung des Endokards und Epikards in der Diastole sowie in der Systole. Normalerweise ist dies zeitintensiv, da jede Schicht und jede Phase (typischerweise wird das Herz in 10-14 Schichten zu je 8 mm gescannt, in ca. 25-30 Phasen) bearbeitet werden muss. Dies führt einerseits zu einem erheblichen Aufwand und andererseits zu Unterschieden in den Messwerten zwischen verschiedenen Untersuchern (Interrater-Variabilität) sowie auch innerhalb des gleichen Untersuchers (Intrarater-Variabilität), wenn die gleiche Person den gleichen Patienten später nochmals analysiert. Diese automatische Konturerkennung erfolgt innerhalb von Sekunden und ist sehr genau und hilft diese Messwertunterschiede zu minimieren.
Ein weiteres Produkt für die kardiale Bildgebung kommt von der Firma Caption AI, welches eine innovative Technologie für die Echokardiographie bietet, die medizinisches Personal durch Live-Anleitungen unterstützt, um qualitativ hochwertige Ultraschallbilder zu erfassen. Ein Qualitätsmesser beurteilt live die diagnostische Qualität der Bilder und die Software gibt Anleitungen, wie der Schallkopf gedreht oder gekippt werden soll, um die Bildqualität zu verbessern. Die Anzeige färbt sich grün, sobald die optimale Bildqualität erreicht ist und gleichzeitig werden die Messungen automatisch erhoben. Zudem speichert das System automatisch nur die besten Bilder jeder Scansitzung, was auch Nicht-Experten ermöglicht, am Schluss einen Datensatz an diagnostisch auswertbaren Bildern zu gewinnen.
Eine weitere Firma, US.ai aus Singapur, bietet eine Technologie an, die während der Echokardiographie alle Messwerte laufend generiert und zudem direkt einen Bericht inklusive der Wahrscheinlichkeitsbewertung der Diagnose erzeugt. Dies wird ein enormer Zeitgewinn sein für die Kardiologen:innen und wird auch helfen, schnell zu entscheiden, welche weiteren Abklärungen indiziert sind.
KI-Technologien zur Segmentierung und Erkennung von Herz-Gefässerkrankungen werden in Zukunft nicht nur dazu beitragen, Diagnosen präziser, personalisierter und schneller zu stellen, aber auch zunehmend ganzheitliche Rollen zu übernehmen. Diese umfassen korrekte Diagnosestellung und den Vorschlag zur individualisierten Therapie, beispielsweise bei der Aortenklappen Stenose durch optimale Klappenselektion (Grösse der Klappe, Zugang minimalinvasiv oder chirurgisch) oder wie eine medikamentöse Therapie aussehen soll (z.B. bei der kardialen Amyloidose oder Entschied einer Defibrillator Implantation bei der hypertrophen Kardiomyopathie) oder Empfehlungen zum weiteren Patienten Monitoring (z.B. wie man kardiale Sarkoidose Patienten nachkontrollieren soll). In dieser Zukunft werden Ärztinnen und Ärzte hauptsächlich eine überwachende und bestätigende Experten Rolle einnehmen, anstatt die Analysen und Berechnungen direkt selber durchzuführen.
Copyright bei Aerzteverlag medinfo AG
PhD, FESC, FACC, FSCCT, FSCMR
Leiter kardiale Bildgebung
Universitätsklinik für Kardiologie
Inselspital Bern
Freiburgstrasse 18
3010 Bern
christoph.graeni@insel.ch
Es besteht keine Beteiligung des Autors an den erwähnten Produkten, weder in Bezug auf deren Entwicklung noch in finanzieller Hinsicht.
1. https://www.captionhealth.com/technology
2. https://vista.ai/
3. https://cleerlyhealth.com/
4. https://us2.ai/
5. https://cleerlyhealth.com/
6. Griffin WF et al. JACC Cardiovasc Imaging . 2022 Feb 15;S1936-878X(22)00001-8.
7. Ash FM et al. Circ Cardiovasc Imaging . 2019 Sep;12(9):e009303.
8. Louhai A. et al. JACC Cardiovasc Imaging. 2023 Nov 27:S1936-878X(23)00473-4.
9. Gräni C. Eur Heart J. 2023 Dec 1;44(45):4793-4795