Das Vulvakarzinom ist ein seltener bösartiger gynäkologischer Tumor, der vor allem bei älteren Frauen auftritt. Die häufigsten klinischen Symptome sind Juckreiz oder Schmerzen an der Vulva, die mit einem Knoten oder einem Geschwür einhergehen können. Es gibt keine Evidenz für ein Screening in einer unselektierten Population. Jede verdächtige Läsion sollte biopsiert werden, um eine Invasion auszuschliessen. Der häufigste Subtyp ist das Plattenepithelkarzinom, das 90 % der invasiven Vulvakarzinome ausmacht. Die Behandlung des Vulvakarzinoms hängt von der Histologie und dem chirurgischen Staging ab. Die primäre Behandlung des Vulvakarzinoms ist die Operation, aber eine primäre oder begleitende Chemoradiotherapie ist eine Alternative, insbesondere bei fortgeschrittenen Tumoren. Die Behandlung sollte individuell erfolgen und von einem multidisziplinären Team in einem Krebszentrum mit Erfahrung in der Behandlung von Vulvakarzinomen durchgeführt werden.
Vulvar cancer is a rare gynaecological malignancy that mainly affects older women. The most common clinical symptoms are vulvar pruritus or pain, which may be associated with a lump or an ulcer. There is no evidence to support screening in an unselected population. Any suspicious lesion should be biopsied to exclude invasion. The most common subtype is squamous cell carcinoma, which accounts for 90% of invasive vulvar cancers. Treatment of vulvar cancer depends on histology and surgical staging. Surgery is the main treatment for vulvar cancer, but primary or concurrent chemoradiotherapy is an alternative, especially for advanced tumors. Treatment should be individualised and carried out by a multidisciplinary team in a cancer centre experienced in treating vulvar cancer.
Key words: Vulvar cancer; Staging; Treatment; Surgery; Chemoradiotherapy
Introduction
Vulvar cancer is rare, accounting for approximately 4-6% of cancers diagnosed in the female genital tract and less than 1% of all cancers in women (1, 2). The 5-year survival rate for vulvar cancer that has not spread beyond the vulva is almost 87%, and drops to less than 50% if it has spread to surrounding tissues or organs and/or regional lymph nodes (1, 3). There are several different types of vulvar cancer, with squamous cell carcinoma (SCC) being the most common, accounting for about 90% of all vulvar cancers, followed by vulvar melanoma, adenocarcinoma, basal cell carcinoma, sarcoma and undifferentiated vulvar cancer (2-4). Vulvar SCC originates from the squamous epithelium of the vulva and is divided into HPV-dependent and HPV-independent subtypes (2-4). Other common risk factors in addition to HPV include 1. a history of anogenital cancer, especially cervical cancer, 2. vulvar lichen sclerosus and vulvar lichen planus, 3. HIV infection or a weakened immune system, 4. smoking, and chronic local irritation, for example from long-term pessary use (2-4).
Diagnostic workup and staging
The diagnosis of vulvar cancer involves several diagnostic tests including physical examination, colposcopy, tissue biopsy and imaging. The pathology report of the preoperative biopsy should include at least the histological type, depth of invasion, molecular testing for HPV, and p53 immunohistochemistry is recommended for HPV-independent carcinoma (4). Computed tomography (CT) and magnetic resonance imaging (MRI) scans may be helpful in identifying enlarged lymph nodes in the groin or pelvis, the extent of spread, or other metastases for treatment planning (5). Fluorodeoxyglucose positron emission tomography CT (PET-CT) can also be used to assess and detect inguinofemoral lymph node involvement and is additionally used when metastatic disease is suspected or in the recurrence scenario, particularly when exenteration is considered (4, 6).
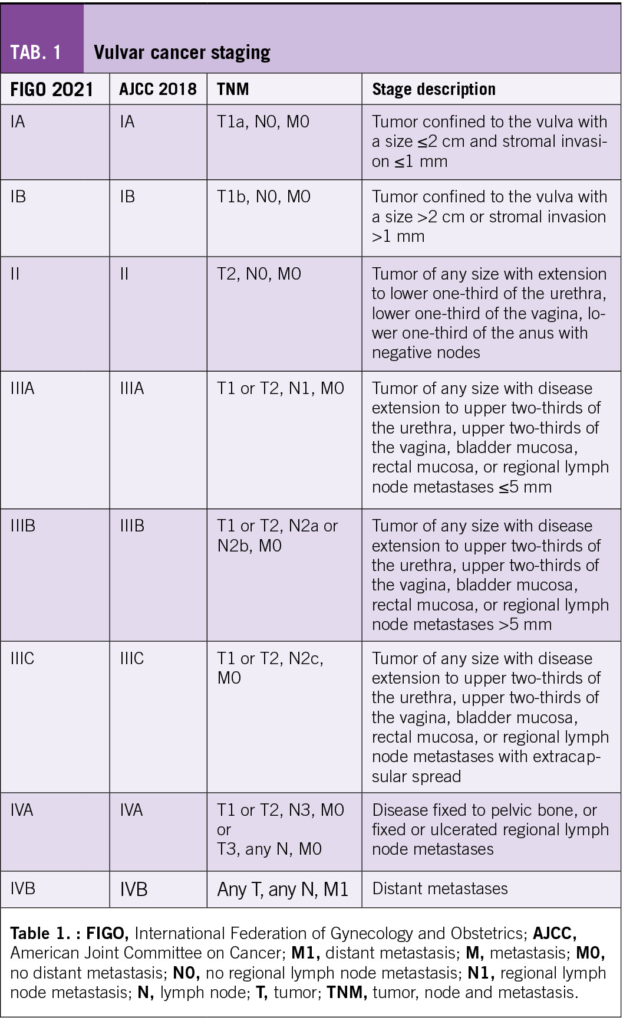
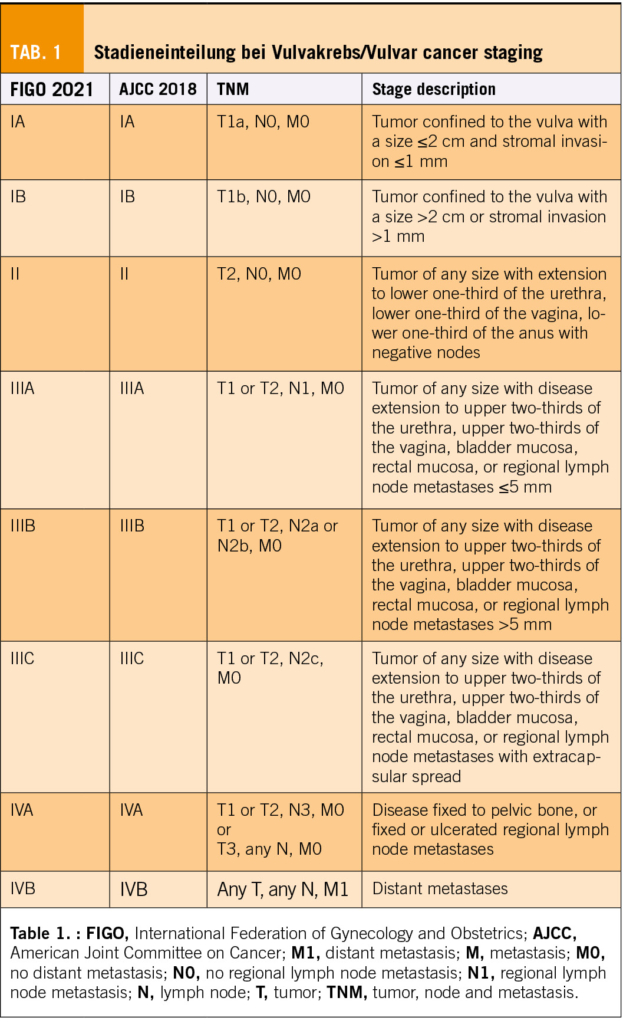
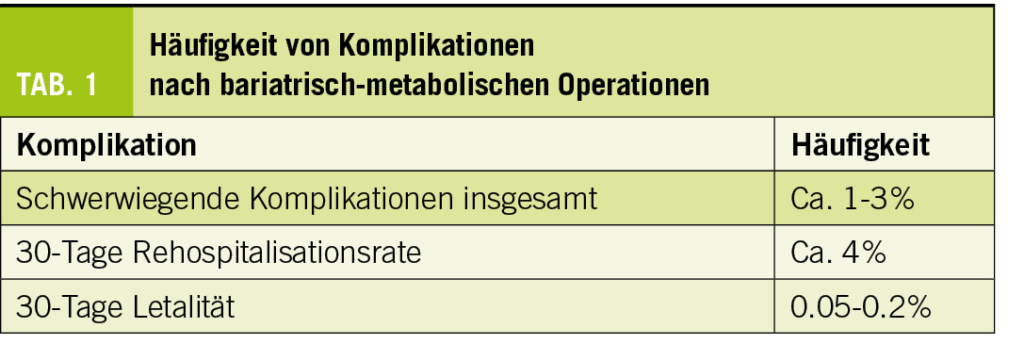
Vulvar cancer can be staged using the FIGO staging system and TNM classification (Table 1). However, due to lack of evidence to base treatment on the FIGO 2021 staging, the TNM classification is advised (4).
Treatment algorithm
Vulvar cancer affects predominantly elderly women and comorbidities increasing with age may prove challenging when planning management. Current guidelines for the management of vulvar cancer are based on retrospective or comparative studies and, because of its rarity, on data from cervical cancer. The management of vulvar cancer should be individualised and provided by a multidisciplinary team in a cancer centre experienced in the management of vulvar cancer. This care should include sexual medicine and psycho-oncology to provide advice on post-treatment vaginal dysfunction.
Early stage
(FIGO: IA and TNM: T1a, N0, M0)
Radical local excision is recommended with the aim of achieving tumour-free pathological margins. A minimum pathological margin of >2-3 mm appears to be sufficient, but the optimal margin remains to be determined (4). In addition, patients with early stage disease (depth of invasion ≤1 mm) do not require deep groin treatment (4, 6). Depending on the extent of the disease, radical wide local excision, partial or complete radical vulvectomy or even pelvic exenteration may be used. If skin grafting is needed, it should be done by a multidisciplinary team with a plastic/reconstructive surgeon.
Adjuvant radiotherapy should be given when (1) invasive disease extends to the pathological margins of the primary tumour and further surgical excision is not possible, and (2) in the case of close but clear pathological margins, radiotherapy may be considered to reduce the incidence of local recurrence. There is currently no consensus on a pathological margin distance threshold below which adjuvant radiotherapy should be recommended (4). Adjuvant radiotherapy should be started within 6 weeks of surgery if possible.
Radiotherapy is mainly used in the adjuvant setting for early stage vulvar cancer. However, individual women who are unable to tolerate surgery may be treated with primary radiotherapy with or without chemotherapy (2, 4).
Locally advanced stage
(FIGO: IB-IVA and TNM: T1b, N0, M0 – T3, any N, M0)
Treatment of advanced vulvar cancer often involves several treatment modalities. Primary chemoradiotherapy should be considered in advanced stages to avoid exenterative surgery (4). Radiosensitising chemotherapy, preferably with weekly cisplatin, is recommended. In addition, individual women who are unfit for surgery may be treated with primary radiotherapy with or without chemotherapy.
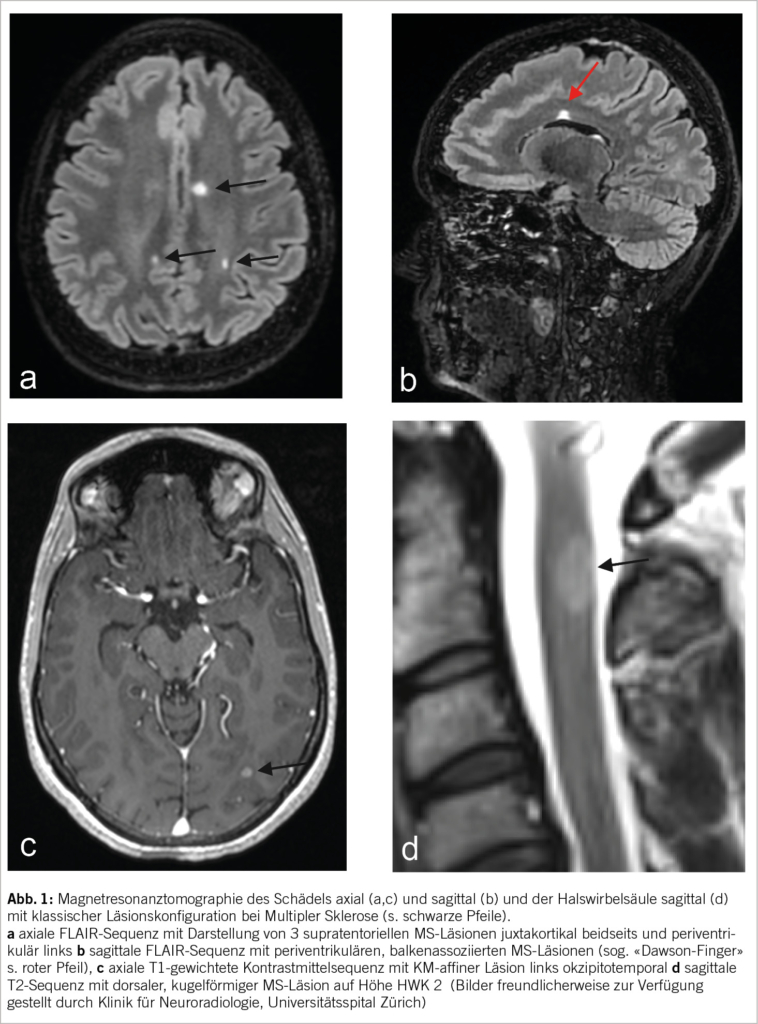
Surgery remains the main treatment for locally advanced vulvar cancer. Radical local excision with inguinal treatment is recommended (2-4, 7). Sentinel lymph node sampling is recommended in patients with stage > pT1a and unifocal cancers < 4 cm, without obvious lymph node spread on clinical examination and imaging (Figure 1). A preoperative lymphoscintigram is recommended to allow preoperative identification, location and number of sentinel lymph nodes. A radioactive tracer is used to identify the sentinel lymph node, with optional use of blue dye or indocyanine green (4). Intraoperative assessment should be performed to avoid a second surgical procedure. There is a risk of missing micrometastases (≤2 mm), but inguinofemoral lymphadenectomy can be safely omitted in favour of radiotherapy for micrometastatic disease (4). An inguinofemoral lymphadenectomy of the affected area should be performed if metastatic disease (>2 mm) is detected in the sentinel lymph node or if no sentinel lymph node is found (2, 4). Bilateral sentinel lymph node sampling is required for tumours involving the midline, and if unilateral metastasis is detected, the incidence of contralateral metastasis is low and further treatment can be limited to the affected groin (4).
Inguinofemoral lymphadenectomy through a separate incision is recommended for tumours ≥ 4 cm and/or multifocal invasive disease. If the tumour is > 1 cm from the midline, ipsilateral inguinofemoral lymphadenectomy is recommended. In addition, contralateral inguinofemoral lymphadenectomy should be performed if the ipsilateral nodes show metastatic disease. Re-excision is the treatment of choice if the cancer extends to the pathological margins of the primary tumour (2-4).
Adjuvant radiotherapy to the vulva should be considered when 1. invasive disease extends to the pathological excision margins of the primary tumour and further surgical excision is not possible, and 2. to reduce the incidence of local recurrence in cases with close but clear pathological margins. In cases with > 1 metastatic lymph node and/or the presence of extracapsular lymph node involvement, adjuvant radiotherapy to the inguinofemoral region should be considered (2, 4).
Metastatic
(FIGO: IVA and TNM: Any T, any N, M1)
Metastatic vulvar cancer is a palliative condition. There are limited treatment options and no standard of care for metastatic vulvar cancer. Therefore, the best supportive care should be discussed with the patient as an alternative to medical treatment. As more than one third of vulvar cancer cases occur in older women, it is important to carefully assess the eligibility of these patients for cancer-specific treatment, taking into account overall life expectancy and specific goals related to the cancer diagnosis, before initiating a comprehensive pre-treatment evaluation (2, 4).
First-line platinum-based chemotherapy should be considered, with cisplatin or carboplatin and paclitaxel as the preferred regimen (2, 4). Based on the data from cervical cancer, adding pembrolizumab in cases with PD-L1 expression and CPS≥1 and/or bevacizumab to platinum-based chemotherapy may be considered in selected first-line patients, although these drugs are not approved for vulvar cancer (8). There is no standard treatment after progression to platinum-based first-line chemotherapy. Immune-checkpoint and epidermal growth factor receptor-targeted inhibitors may be considered as monotherapy. However, there is no specific approval for any of these drugs. Therefore, enrolment of metastatic vulvar cancer patients in clinical trials is strongly encouraged.
Treatment should be managed by a multidisciplinary team and early referral to a palliative care specialist is recommended. Palliative care may include medications, radiotherapy, surgery and psycho-oncological therapies that can lead to improved outcomes and quality of life (9).
Local recurrent disease
Restaging by CT (or PET-CT) of the thorax/abdomen/pelvis should be performed. The recommended treatment is radical excision when possible, followed by postoperative radiation in radiotherapy naive patients. Additionally, inguinofemoral lymphadenectomy should be performed if the depth of invasion is > 1 mm and previous sentinel lymph node removal only was performed (4). The indications for postoperative radiotherapy are comparable to those for the treatment of primary disease. If surgical treatment is not possible, chemoradiotherapy should be used (2, 4).
Follow-up
Local recurrences are most common in the first 2 years after treatment, and because therapy is highly dependent on further excision or radiotherapy, detection of recurrence as early as possible is necessary. Therefore, after primary surgical treatment, the ESGO vulvar cancer guidelines (4) recommend follow-up every 3-4 months for the first 2 years after the initial postoperative follow-up of 6-8 weeks, then every 6 months for the third and fourth years, and from then on long-term follow-up, which should include clinical examination of the vulva and groin with biopsy if suspected, and review of symptoms (10). Follow-up after definitive (chemo)radiotherapy is the same, with the exception of a first follow-up 10-12 weeks after completion of definitive (chemo)radiotherapy with CT or PET-CT to document complete remission. Close follow-up is also required to check for injury or tightness and scarring of vulvar and vaginal tissues. Some women may be advised to use vaginal dilators as a prophylactic measure.
Copyright bei Aerzteverlag medinfo AG
Frauenklinik, Universitätsspital Basel
Spitalstrasse 21
4031 Basel
Leiterin Frauenklinik & Gynäkologisches Tumorzentrum
Chefärztin Gynäkologie/Gyn. Onkologie
Frauenklinik
Universitätsspital Basel
Spitalstrasse 21
4031 Basel
viola.heinzelmann@usb.ch
Die Autoren haben keine Interessenkonflikte angegeben.
1. [https://www.cancer.net/cancer-types/vulvar-cancer/statistics].
2. Olawaiye AB, Cuello MA, Rogers LJ. Cancer of the vulva: 2021 update. Int J Gynaecol Obstet. 2021;155 Suppl 1(Suppl 1):7-18.
3. Koh WJ, Greer BE, Abu-Rustum NR, Campos SM, Cho KR, Chon HS, et al. Vulvar Cancer, Version 1.2017, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw. 2017;15(1):92-120.
4. Oonk MHM, Planchamp F, Baldwin P, Mahner S, Mirza MR, Fischerova D, et al. European Society of Gynaecological Oncology Guidelines for the Management of Patients with Vulvar Cancer – Update 2023. Int J Gynecol Cancer. 2023;33(7):1023-43.
5. Lin G, Chen CY, Liu FY, Yang LY, Huang HJ, Huang YT, et al. Computed tomography, magnetic resonance imaging and FDG positron emission tomography in the management of vulvar malignancies. Eur Radiol. 2015;25(5):1267-78.
6. Nikolic O, Sousa FAE, Cunha TM, Nikolic MB, Otero-Garcia MM, Gui B, et al. Vulvar cancer staging: guidelines of the European Society of Urogenital Radiology (ESUR). Insights Imaging. 2021;12(1):131.
7. Lawrie TA, Patel A, Martin-Hirsch PP, Bryant A, Ratnavelu ND, Naik R, Ralte A. Sentinel node assessment for diagnosis of groin lymph node involvement in vulval cancer. Cochrane Database Syst Rev. 2014;2014(6):CD010409.
8. Colombo N, Dubot C, Lorusso D, Caceres MV, Hasegawa K, Shapira-Frommer R, et al. Pembrolizumab for Persistent, Recurrent, or Metastatic Cervical Cancer. N Engl J Med. 2021;385(20):1856-67.
9. Krakauer EL, Kane K, Kwete X, Afshan G, Bazzett-Matabele L, Ruthnie Bien-Aime DD, et al. Essential Package of Palliative Care for Women With Cervical Cancer: Responding to the Suffering of a Highly Vulnerable Population. JCO Glob Oncol. 2021;7:873-85.
10. Salani R, Khanna N, Frimer M, Bristow RE, Chen LM. An update on post-treatment surveillance and diagnosis of recurrence in women with gynecologic malignancies: Society of Gynecologic Oncology (SGO) recommendations. Gynecol Oncol. 2017;146(1):3-10.