Die Definition der chronischen Niereninsuffizienz (CKD) wird mit den Formeln mit Kreatinin und Cystatin C beschrieben. Es wird die glomeruläre Filtrationsrate (eGFR estimated) berechnet nach CKD-EPI (ml/min/1.73m2). Die 24 h Urinsammlung für die Clearance ist häufig durch einen Messfehler bei der Urinsammlung kompromittiert, so die Ausführungen von Frau Dr. Kathrin Fausch, Kantonsspital Graubünden.
Die Definition der KDIGO Kidney Disease Improving Global Outcomes lautet: >3 Monate Funktionseinschränkung, histologische/strukturelle Veränderungen, Proteinurie/Hämaturie
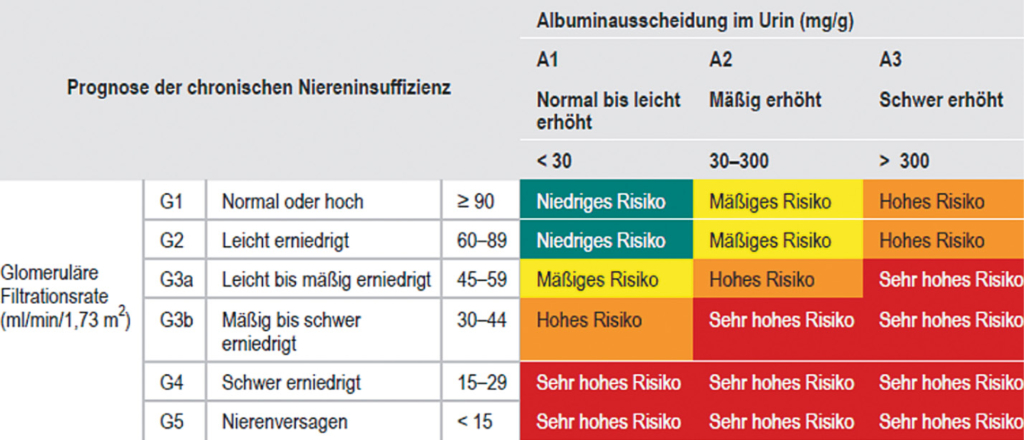
Einteilung und Prognose
CGA: Grunderkrankung (Causa), GFR, Albumin
Epidemiologie
Je nach Definition beträgt die Prävalenz der chronischen Nierenerkrankung (CKD) bei Frauen im gebärfähigen Alter bis 6% in high income countries, bis 3% der schwangeren Frauen, CKD ≥ Stadium 3 (eGFR < 60 ml/min/1.73m2) Prävalenz 0.5%.
Präkonzeptionelle Beratung
Von der Placenta zur Niere: Präeklampsie kann einen bleibenden Nierenschaden verursachen, via AKI tubulären Schaden, oder Podozytenverlust.
Von der Niere zur Placenta: CKD kann plazentäre Dysfunktion induzieren, mit einem erhöhten Risiko für Frühgeburt, Schwangerschafts-assoziierte hypertensive Krankheiten und Präeklampsie.
Das Risiko für schwere Niereninsuffizienz ist zusätzlich erhöht bei Diabetes mellitus, Hypertonie, Autoimmunerkrankung, Proteinurie >1g/d. Signifikant höheres Risiko für schlechteres Schwangerschafts-Outcome auch bei Nierenerkrankungen mit (noch) normaler Nierenfunkton *Aborte, Frühgeburtlichkeit, Präeklampsie, IUGR, vorzeitige Plazentalösung, IUFT, Verschlechterung der Nierenfunktion.
Eine chronische Nierenerkrankung verläuft oft klinisch und biochemisch unauffällig, bis die Nierenschädigung fortgeschritten ist. Symptome sind ungewöhnlich, bis die glomeruläre Filtrationsrate auf <25 % des Normalwerts sinkt, und mehr als 50 % der Nierenfunktion kann verloren gehen, bevor das Serumkreatinin über 120 μmol/l ansteigt. Frauen, die mit Serumkreatininwerten über 124 μmol/l schwanger werden, haben ein erhöhtes Risiko für einen beschleunigten Rückgang der Nierenfunktion und einen schlechten Ausgang der Schwangerschaft.
Das Kreatinin sollte vor der Schwangerschaft bestimmt werden, dies erlaubt das Risiko für Nierenfunktionsverschlechterung während und nach Schwangerschaft zu erfassen.
Hereditäre Nierenerkrankungen:
ADPKD (Autosomal-dominante polyzystische Nierenerkrankung)
ADTKD, Komplementerkrankungen → genetische Beratung
Teratogene Medikamente für die Behandlung von Nierenerkrankungen: Cyclophosphamid, Mycophenolat, RAAS-Inhibitoren, Diuretika
Nierentransplantierte und immunsupprimierte Patientinnen:
sichere Immunsuppressiva in der Schwangerschaft sind Azathioprin, Tacrolimus, Cyclosporin A, Hydroxychloroquin, Steroide.
Nierenfunktion in der Schwangerschaft
Die folgenden Werte sollten während der Schwangerschaft angestrebt werden. Blutdruck 10-20 mmHg, Nierenvolumen, Renaler Plasmafluss und GFR ca.
50%, Kreatinin (36-45 µmol/l), Harnstoff (3mmol/l), Harnsäure (190-256 µmol/, Proteinurie bis 300 mg täglich.
Kontrolle der Nierenfunktion in der Schwangerschaft
Die üblichen Schätzformeln sind nicht validiert, Cystatin C ist ebenfalls nicht validiert, die 24 h Urinsammlung ist der Goldstandard.
Ausserhalb der Spanne einer normalen Schwangerschaft liegen die folgenden Kreatinin-Werte:
1. Trimester: >0.86mg/dl (>76µmol/l)
2. Trimester: >0.81mg/dl (>72µmol/l)
3. Trimester: >0.87mg/dl(>77µmol/l)
Ein Serum-Kreatinin von 77µmol/l ist bei schwangeren Frauen also pathologisch. Es steht für eine verminderte eGFR und sollte weiter abgeklärt werden (DD akutes Nierenversagen, DD bisher unbekannte vorbestehende chronische Nierenkrankheit).
Die Kontrolle der Nierenfunktion in der Schwangerschaft umfasst eine Quantifizierung der Proteinurie (Spoturin mit Protein/Kreatinin Quotient) oder eine 24 h Sammlung (Messfehler!) bei jeder Frau mit Nierenerkrankung zu Beginn der Schwangerschaft als Baseline-Wert, Urinstix >1+: Quantifizierung >300 mg/24 h pathologisch (>30mg/mmol bzw. 0.3 mg/mg) → Nephrologie (vorbestehende Proteinurie?). Proteinurie >300mg/d vor der 20 SSW: präexistente Nierenerkrankung.
CKD und Schwangerschaft
Eine vorbestehende Nierenerkrankung ist ein Hochrisiko-Faktor* für Präeklampsie. Massnahmen sind
– ASS 100 mg täglich (75-150 mmHg) ab Frühschwangerschaft (12 SSW)
– Präeklampsie-Screening 1. Trimester
– Präeklampsie-Monitoring: Blutdruck und Proteinurie,
fetaler Doppler, >20 SSW
sFlt-1/PLGF (<38 schliesst PE in nächsten 2 Wochen mit hoher Sicherheit aus)
– Bestimmung von Ferritin und Transferrinsättigung
– Bestimmung von Vitamin D
– Heimblutdruckmessungen
* St.n hypertensiver Schwangerschaftserkrankung,
Autoimmunerkrankung, arterielle Hypertonie, Diabetes Typ 1,2
Therapie der CKD in der Schwangerschaft
Trinkmenge individuell je nach CKD-Stadium, Bestimmung von Calcium, Phosphat, PTH, 25 OH Vit D 1x/Trimester. Gabe von 25 OH-Vitamin D, Calcitriol. Keine nicht-calciumhaltigen Phosphatbinder. Keine Calcimimetika. Labetalol, Nifedipin, Alpha-Methyldopa. Keine ACE-Hemmer, Sartane, Diuretika, SGLT2-Hemmer. Zielblutdruck 110/70 – 135/85 mmHg. Eisengabe i.v (Fe-III Derivate), Ziel-Ferritin >200ng/l, Transferrinsättigung>25%. ESA (Erythropoietin stimulierende Agenzien) bei Hb<10g/dl. Ziel-Hb 10-11.5 g/dl
Diagnose der Präeklampsie bei CKD
CKD ohne Proteinurie und Hypertonie:
– neu Hypertonie >140/90
– mind 1 neu aufgetretene Organmanifestation
– pathologischer sFLT/PLGR Quotient (<38 Präeklampsie
unwahrscheinlich
CKD mit vorbestehender Hypertonie und Proteinurie:
– schwere Hypertonie >160/>110mmHg
– Verdoppelung der Antihypertensiva
– Verdoppelung der Proteinurie seit 1.Trimenon
– pathologischer sFLT/PLGR Quotient
Akute Niereninsuffizienz in der Schwangerschaft
KDIGO Guidelines 2012
Diabetische Nephropathie in der Schwangerschaft
«Nierenkomplikationen» sind ein passagerer Anstieg der Proteinurie bis zum nephrotischen Syndrom. Schwangerschaft und Anzahl Geburten sind kein Risikofaktor für die Entwicklung einer diabetischen Nephropathie. Bei CKD ist das Risiko für Progression erhöht. 10% der Patientinnen mit fortgeschrittener CKD sind dialysepflichtig nach Entbindung. «Schwangerschaftskomplikationen» sind bei 70% erfolgt die Entbindung vor der 37. SSW, 35-66% erleiden eine Präeklampsie, abhängig von der Schwere der Nephropathie (CKD, Albuminurie). Wichtig sind Blutzucker- und Blutdruckkontrolle. BZ- und BD-Kontrolle.
Lupusnephritis
Vor der Schwangerschaft sollte der Lupus klinisch 6 Monate symptomfrei sein. Eine interdisziplinäre und präkonzeptionelle Beratung ist empfehlenswert.
Eventuell Nierenbiopsie vor SS, ASS 100-150 mg und LMWH, Hydroxychloroquin weiterführen, Immunsuppression vor SS muss mit Nephrologen geklärt werden. Nephrologische Überwachung der Lupusnephritis-Aktivität alle 4-8 Wo. Lupus flare, Anti Ro (SSA) oder anti La (SSB) fetale Echokardiographie ab 16 SSW, (fetaler AV- Block).
Die aktive Lupusnephritis hat das schlechteste Schwangerschaftsoutcome St.n Lupusnephritis. Antiphospholipid-Antikörper ist ein Risikofaktor.
Lupusnephritis <> Präeklampsie (Götestam Skorpen, C et al, Eular Leitlinien. Ann Rheum Dis 2016, Moroni G et al, Autoimmun. 2016)
Antiphospholipidsyndrom APS
Arterielle oder venöse Gefässverschlüsse oder SS-Komplikationen* bei Nachweis Antiphospholipid-Antikörper aPL**
* ungeklärter Tod eines Feten ab 10 SSW, Geburt vor 34 SSW wegen Eklampsie, schwerer PE oder Plazentainsuffizienz 3 Spontanaborte vor 10 SSW ohne anderweitige Ursache
** Lupusantikoagulanz (LA), Antikardiolipinantikörper (aCL), Anti-Beta2-Glykoprotein-I-Antikörper (AB2GPI) >2 Antikörper: 40% Lebendgeburten trotz ASS und LMWH, 50% Päeklampsie. 3 Antikörper: 30% Lebendgeburten
EUREKA Algorithmus für Risikoeinschätzung
Glomerulonephritiden und Schwangerschaft
Risiko eines Nierenfunktionsverlusts abhängig von GFR und Blutdruck. Es existieren wenige Studien (Lupus Nephritis, IgA-Nephropathie):
– Nephritis-Aktivität <> Präeklampsie
– Restriktive Biopsie-Indikation (rapid progressive Glomerulonephritis, Nephrotisches Syndrom)
– Risiko: Schwangerschaftskomplikationen abhängig von GFR und Blutdruck
– Immunsuppression (cave teratogene Medikamente)
Patientinnen mit angeborenen Erkrankungen der Nieren und ableitenden Harnwege (CAKUT)
Sie haben ein Erhöhtes Infektrisiko. Antibiotische Dauerprophylaxe?
Eine milde Dilatation bis 20mm des Nierenbeckens rechts >links häufig
Sonographie mit Ableitung der Resistive Indices (RI >0.7) statt CT. Behandlung konservativ
Schwangerschaft nach Nierentransplantation
Frühestens 1 Jahr nach TPL und stabile TPL- Funktion: Immunsuppressiva: Calcineurin-Inhibitoren, Azathioprin, Steroide
Erhöhter Funktionsverlust bei erniedrigter GFR, erhöhte Proteinurie, Hypertonie, Abstossung 5-9%
Lebend-Nierenspenderinnen: Hypertonie, Präeklampsie (x6), fetale Wachstumsrestriktion, FG, Gestationsdiabetes. Der perinatale Outcome ist erniedrigt bei erniedrigter GFR.
– Cave bei Sectio (Lage TPL)
Schwangerschaft bei Dialysepatientinnen
Konzeption vor oder nach Dialysestart beeinflusst Outcome ca. 70% Lebendgeburt, 16.9% spontaner Abort, 5.2%, therapeutischer Abort, 8.3% Totgeburt, 82.8% preterm birth, 19.6 %Präeklampsie/Hypertonie.
Lange und tägliche Hämodialyse, Peritonealdialyse möglich. Trockengewicht wöchentlich evaluieren: 0.3-0.5kg/Wo ab 2.Trimenon. BD <140/90 mmHg, keine intradialytischen Blutdruckabfälle. Harnstoff vor Dialyse <16 (12.5) mmol/l.
Peripartales Management
Volumenmanagement, Blutdruckmanagement, nephrologische Mitbetreuung
Zeitpunkt der Geburt bei CKD-Patientinnen:
– Geburtshilfliche Indikation
– Nephrologische Indikation
o Nierenfunktionsverschlechterung
o Symptomatische Hypabuminämie
o Therapierefraktäre Hypertonie
o Überwässerung
Postpartales Management
Keine NSAR postpartal bei CKD (Progression CKD, Volumenretention). Nephrologische Kontrolle spätestens 6 Wochen postpartal bei Patientinnen mit chronischen oder akuten Nierenerkrankungen.
Weiteres Management optimalerweise postpartal direkt mit Nephrologen klären.
riesen@medinfo-verlag.ch