Am 26. und 27. Februar 2024 fand in St. Gallen die traditionelle Fortbildung für Klinische Onkologie statt. Unter der Leitung von Prof. Martin Früh, Chefarzt a. i. der Klinik für Medizinische Onkologie und Hämatologie am Kantonsspital St. Gallen, präsentierten renommierte Expertinnen und Experten aktuelle Entwicklungen aus Radioonkologie, Systemtherapie, Thorax , Gynäko und Hämatologie. Ziel der Veranstaltung war es, die Brücke zwischen wissenschaftlicher Evidenz und klinischer Anwendung zu schlagen – für ein interdisziplinäres Publikum aus Onkolog/innen, Hausärzt/innen und Pflegefachpersonen. Dieser Bericht fasst die wesentlichen Inhalte zusammen.
Strahlentherapie und Systemtherapie – Was machen wir 2026?

Dr. Dr. Sebastian Christ (Radioonkologie, Universitätsspital Zürich) skizzierte den Wandel von einer sequenziellen zu einer biologisch integrierten Kombinationsbehandlung. Strahlentherapie und Arzneimitteltherapie sind heute beide hochwirksam. Die entscheidende klinische Frage lautet daher nicht mehr, ob beide Verfahren kombiniert werden sollen, sondern wie, wann und bei welchen Patienten.
Wandel des Paradigmas
Über Jahrzehnte dominierte ein sequenzielles Vorgehen: Die Radiotherapie diente der lokalen Tumorkontrolle, die Systemtherapie der Kontrolle systemischer Tumormanifestationen. Mit modernen Bestrahlungstechniken wie IMRT, IGRT, SBRT und MR-gesteuerter Radiotherapie sowie mit neuen medikamentösen Optionen, darunter Immuncheckpoint-Inhibitoren, zielgerichtete Substanzen, ADCs und Zelltherapien, rückt heute das Konzept einer integrierten Präzisionsonkologie in den Vordergrund.
Die Kombination beider Modalitäten kann die Wirksamkeit steigern, erhöht jedoch zugleich das Risiko überlappender Toxizitäten. Dadurch wird das therapeutische Fenster enger. Erforderlich sind daher eine präzisere biologische Planung und eine enge interdisziplinäre Abstimmung.
Evidenz und klinische Trends
• Chemoradiation bleibt Goldstandard, gestützt durch Level 1A Evidenz.
• IO/RT Kombinationen (Immune Checkpoint Inhibitor + Bestrahlung) zeigen etwa 30 % Mortalitätsreduktion, sind aber toxizitätssensitiv.
• Die Integration erfolgt zunehmend anhand molekularer Biomarker, ctDNA und präzisionsgesteuerter Sequenzierung
Plattformstudien wie CONCORDE untersuchen die Kombination konventioneller Radiotherapie mit neuen immunonkologischen und zielgerichteten Substanzen. Die Anwendung wird damit nicht mehr allein technisch, sondern zunehmend biologisch gesteuert. Die klassische Sequenztherapie entwickelt sich zur gezielten Synergietherapie.
Fazit
Strahlentherapie und Systemtherapie entwickeln sich zu komplementären, an der Tumorbiologie ausgerichteten Behandlungsstrategien. Entscheidend sind eine patientenspezifische Sequenzierung, die frühe Abstimmung im Tumorboard und die konsequente Einbindung biologischer Parameter in die klinische Planung.
Neoadjuvante und perioperative Systemtherapie beim nicht kleinzelligen Bronchialkarzinom

Dr. Dr. Diego P. D. Kauffmann Guerrero (LMU München) stellte aktuelle Konzepte zur neoadjuvanten und perioperativen Immunchemotherapie beim resektablen NSCLC vor. Ziel dieser Strategien ist es, durch präoperative Kombinationen aus Chemotherapie und Immuncheckpoint-Inhibitoren eine anhaltende Antitumorimmunität zu induzieren und die Heilungsraten zu verbessern.
Rationale und Studienlage
Die Kombination von Operation und Immuntherapie soll der postoperativ oft geschwächten Immunantwort entgegenwirken. Frühe Daten der NADIM Studie zeigten deutlich höhere pathologische Komplettremissionsraten (pCR).
Mehrere randomisierte Studien stützen inzwischen diesen Ansatz:
• In CheckMate 816 verlängerte Nivolumab in Kombination mit Chemotherapie das ereignisfreie Überleben deutlich gegenüber Chemotherapie allein (23,7 vs. 10,5 Monate; HR 0,4) und erhöhte die pCR-Rate, ohne die Toxizität wesentlich zu steigern.
• CheckMate 77T zeigte für eine neoadjuvante Nivolumab-basierte Strategie ebenfalls eine signifikante Verbesserung des ereignisfreien Überlebens.
• In AEGEAN führte Durvalumab plus Chemotherapie zu höheren Komplettremissionsraten bei günstigem Sicherheitsprofil.
• KEYNOTE 671 und RATIONALE 315 bestätigten vergleichbare Vorteile auch für Pembrolizumab beziehungsweise Tislelizumab.
• Die laufende Studie IMpower030 untersucht Atezolizumab im perioperativen Setting.
Adjuvante Therapien
• IMpower 010 zeigte, dass Atezolizumab nach adjuvanter Chemotherapie das krankheitsfreie Überleben verbessert, insbesondere bei PD-L1-Expression ≥ 1 %.
• In KEYNOTE 091 verbesserte Pembrolizumab das krankheitsfreie Überleben unabhängig vom PD-L1-Status.
• NADIM Adjuvant deutet auf ein reduziertes Rezidivrisiko unter Nivolumab in Kombination mit adjuvanter Chemotherapie hin.
• ANVIL prüft bei mehr als 600 Zentren in den USA, ob sich nach Resektion eine Verbesserung des Gesamtüberlebens um 30 % erreichen lässt.
Bei EGFR mutierten Tumoren überwiegen Exon 19 Deletionen und L858R Mutationen; diese Patient/-innen bedürfen getrennter Therapiepfade.
Neoadjuvanz oder Perioperativtherapie?
Neue IASLC Analysen (2024) zeigen eine weitere Verbesserung von Überleben und Rezidiv-freiheit, wenn Nivolumab perioperativ – also prä und postoperativ – angewendet wird. Die Kombination scheint überlegen gegenüber reiner Neoadjuvanz.
Take Home Messages
• Die Neoadjuvante Therapie mit Immunchemotherapie erhöht pCR und verbessert EFS.
• Perioperative Schemata zeigen zusätzlichen Vorteil bei ähnlicher Sicherheit. Molekulare Testung (EGFR, ALK, PD L1) und präzises Staging (PET CT, cMRT) sind verpflichtend.
• Patient/-innen mit hohem PD L1 und N2 Befall profitieren besonders.
• Bei vollständiger Remission (pCR) ist eine anschliessende adjuvante IO Therapie nicht obligat.
Innovationen beim kleinzelligen Bronchialkarzinom (SCLC)

Univ. Prof. Dr. Annelen Beckmann (UKM/WTZ Münster) stellte aktuelle Entwicklungen beim SCLC vor – einer Tumorentität, die nur 12–15 % aller Lungenkarzinome ausmacht, aber besonders aggressiv verläuft. Das Gesamt 5 Jahres Überleben liegt bei rund 8 %, wobei nur ein Drittel der Patient/-innen zum Diagnosezeitpunkt ein begrenztes (Kurativ ) Stadium aufweist.
Stadien und Prognose
Nach der Marburger Klassifikation wird zwischen
• Limited Disease (LD): Tumor auf eine Thoraxhälfte beschränkt, potenziell Kurativ.
• Extensive Disease (ED): metastasierte, palliative Situation – unterschieden.
In frühen Stadien liegt das 5 Jahres Überleben bei 20–30 %, im fortgeschrittenen Stadium nach zwei Jahren bei nur 5–10 %.
Leitlinien und Therapiestandard
Laut ESMO Guidelines (2021/2023) ist eine platinbasierte Chemotherapie + Immuncheckpoint Inhibitor (Atezolizumab od. Durvalumab) der aktuelle Standard in der Erstlinie bei ES SCLC. Ergänzend wird eine frühe Bildgebung (CT/MRT), thorakale Strahlentherapie bei LD sowie eine prophylaktische Hirnbestrahlung (PCI) bei Therapieansprechen empfohlen.
Medianes Gesamtüberleben: 12–13 Monate.
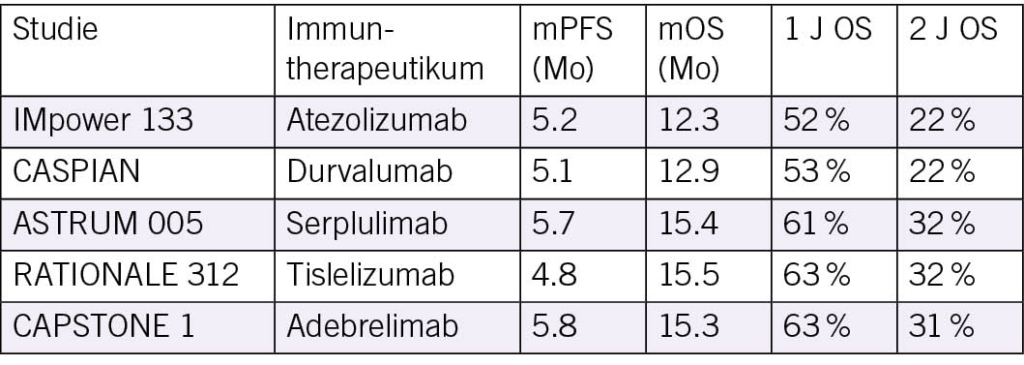
Phase III Studien zur Erstlinie
Praxiserkenntnisse
Kombination aus Chemo und Immuntherapie verbessert Überleben und Langzeitkontrolle deutlich.
• Real World Daten zeigen vergleichbare Wirksamkeit für Atezolizumab und Durvalumab – beide gelten als gleichwertige Optionen.
Zukünftige Therapielandschaft
1. Linie: Platin + Etoposid + ICI → anschliessende IO Erhaltung
2.–3. Linie: Topotecan, Lurbinectedin oder neue Antikörper (Tarlatamab u. a.)
Regelmässige zerebrale MRT Kontrollen bzw. PCI bleiben zentral für Langzeitüberleben. Ein kleiner Teil der Patient/-innen erzielt dauerhafte Remissionen, wie in der CASPIAN Studie, wo Durvalumab + Platin/Etoposid das OS signifikant verbesserte bei unverändert gutem Sicher-heitsprofil.
Fazit
Das SCLC, lange eine domänenspezifisch limitierte Erkrankung, profitiert nun nachweislich von kombinierten Chemo Immuntherapien. Diese markieren den ersten echten Therapiefortschritt seit Jahrzehnten und bilden die neue Behandlungsbasis für alle Patient/-innen mit fortgeschrittener Erkrankung.
Zielgerichtete Systemtherapie beim lokalisierten NSCLC

Prof. Dr. Dr. Sonja Loges (Universitätsklinikum Mannheim) erläuterte die zunehmende Bedeutung zielgerichteter Therapien bei frühem nicht kleinzelligen Lungenkarzinom (NSCLC, Stadium IB–IIIB) und ihre Integration in neoadjuvante und adjuvante Konzepte.
Molekulare Basis und Zielstrukturen
EGFR Mutationen (Exon 19 Deletion, L858R) treten in ≈ 85–90 % der typischen Fälle auf. Sie aktivieren Wachstums-Signalwege, die durch EGFR Tyrosinkinase Inhibitoren (TKI) blockierbar sind. ALK Fusionen (3–5 % der NSCLC, meist EML4 ALK) werden mit ALK Inhibitoren wie Alectinib gezielt behandelt – mit deutlich verbesserter Prognose.
Neoadjuvanz
Osimertinib senkt laut ADAURA Studie das Rückfallrisiko um 79 % (DFS Vorteil) und verbessert das Gesamtüberleben. In der Neoadjuvanz allein oder in Kombination mit Chemo zeigte es ähnliche MPR Raten (~25 %) und geringfügig höhere pCR Raten, wirkt aber überwiegend zytostatisch.
Alectinib (NAUTIKA1/ALINA) bewirkte eine MPR von 60 % und pCR von 25 % – damit deutlich effektiver und als neuer Standardkandidat für ALK positive Patient/-innen bewertet.
Adjuvante Therapie und fortgeschrittene Stadien ADAURA und ALINA:
• Osimertinib dreifacht das PFS vs. Placebo (HR 0.49) und reduziert ZNS Rezidive.
• Alectinib zeigte einen signifikanten DFS Vorteil gegen platinbasierte Chemotherapie (p < 0.001).
Beide Substanzen werden jetzt auch für den perioperativen Einsatz diskutiert.
Neue Daten (Stadium III, inoperabel)
Die LAURA Studie belegt für Osimertinib nach definitiver Radiochemotherapie eine deutliche Verlängerung des progressionsfreien Überlebens gegenüber Placebo bei EGFR mutiertem Stadium III NSCLC – die erste effektive Option in dieser Gruppe.
Fazit
• Osimertinib ist Standard für reseziertes EGFR mutiertes NSCLC (Stadium IB–IIIA) und vielversprechend bei nicht resezierbarem Stadium III.
• Alectinib setzt sich für ALK positive Patient/-innen in Neoadjuvanz und Adjuvanz durch.
• Beide Therapien erfordern eine frühe molekulare Diagnostik (EGFR, ALK, PD L1).
• Die Gesamtdauer der TKI Therapie und die optimale Sequenzierung gegenüber Chemo Immunregimen werden noch evaluiert. [W1.1]
Onkologika: Zu welchem Preis?

Dr. med. et Dr. iur. Kerstin Natalie Vockinger (Universität und ETH Zürich) analysierte die Preisentwicklung, Vergütungssysteme und Evidenzgrundlagen neuer Krebsarzneimittel in der Schweiz und international.
Preisbildung und Kriterien in der Schweiz
Für eine Kostenübernahme durch die obligatorische Krankenversicherung (OKP) müssen Leistungen wirksam, zweckmässig und wirtschaftlich sein.
Die Wirtschaftlichkeit wird mittels therapeutischen Quervergleichs und internationalem Preisreferenzsystem bewertet.
Artikel 71 a-e KVV regeln Einzelfallvergütungen (z. B. bei Off Label Use) für Arzneimittel ohne Spezialitätenlisteneintrag, wenn kein gleichwertiges Alternativprodukt verfügbar ist und ein hoher therapeutischer Nutzen besteht.
Internationale Vergleiche und Preisdynamik
In den USA finden bis 2026 erstmals staatliche Preisverhandlungen statt (Inflation Reduction Act). Bislang keine Preisregulierung → explosiver Kostenzuwachs:
• USA: + 19,7 % jährlich (31 700 → 228 600 USD zwischen 2011–2022), Krebsmedikamente > 650 % teurer als Nicht Onkologika.
• Schweiz: + 3,2 % pro Jahr (29 000 → 41 400 USD), Onkologika > 720 % teurer als Nicht Krebsmedikamente.
Ursachen: steigende F&E Kosten, Marktdruck und gesellschaftliche Zahlungs- bereitschaft für «Lebenszeitgewinne».
Challenge II – Zeit bis zur Kostenübernahme
Medianzeit von Zulassung bis Erstattung:
CH Schweiz 5,8 Mon. | DE 7,4 | US 9,2 | FR 12,9 | GB 17,7.
Nach 1 Jahr sind in Deutschland ca. 74 %, in der Schweiz 63 % der neuen Mittel vergütet.
Ein «Submission Gap» verzögert den Marktzugang in Europa und Schweiz um 13–18 Wochen nach USA. Das internationale Kooperationsprojekt Project Orbis hat diese Lücke bereits spürbar reduziert und verkürzt Zulassungsverfahren.
Challenge III – Evidenz und Marktzugang
Steigende Zahl von Medikamenten erhält beschleunigte Zulassungen auf Basis von Surrogatendpunkten oder Single Arm Studien.
Folge: zunehmende Unsicherheiten bei klinischer Relevanz und Kosten Nutzen Abwägung.
→ Managed Entry Agreements, häufig mit vertraulichen Rabatten, sind ein Zwischenschritt. Entscheidend bleibt die Balance zwischen rascher Verfügbarkeit und robuster Evidenz – einschliesslich post marketing Validierung.
Fazit für die Praxis
• Die Initialpreise für Krebsarzneien steigen weltweit kontinuierlich.
• Preisbildung und Erstattung müssen zugunsten schnellerer Verfügbarkeit und gleichzeitig gerechter Ressourcenverteilung angepasst werden.
• Ein stärkerer Fokus auf klinischen Outcome, Transparenz bei Rabatten und qualitätsgesicherte Evidenzbewertung ist unverzichtbar.
Lebensqualität aus Patientensicht
Onkologisches Basisscreening (oBS)

Prof. Dr. Birgitt von Oorschot (Deutsche Krebsgesellschaft) präsentierte die Arbeit der interdisziplinären Arbeitsgruppe «Patient Reported Outcome – Supportivbereich (PRO S)», die 2023 gegründet wurde, um patientenberichtete Ergebnisse (PROs) systematisch in die onkologische Routineversorgung zu integrieren.
Ziel und Konzept
Das onkologische Basisscreening (oBS) ermöglicht eine bedarfsgerechte Supportiv und Palliativversorgung. Es beruht auf Leitlinien und Evidenz und vermeidet das «Giesskannenprinzip»: Nur wer tatsächlich Unterstützung braucht, soll intensiv betreut werden.
Ziele sind Erhöhung der Patientensicherheit, passgenaue Interventionen sowie optimale Ressourcennutzung im multiprofessionellen Team.
Praktische Umsetzung
Das KeSBa Projekt (Braulke et al., 2023) belegt, dass die onkologische Fachpflege eine tragende Rolle bei Symptom und Belastungsscreenings einnehmen kann. Empfohlen wird eine Einbettung in pflegerische Sprechstunden zur Beratung und Verlaufskontrolle.
Seit 2025 ist das strukturierte Belastungsscreening Pflicht im DKG Zertifizierungssystem. Erfasst werden mindestens vier Dimensionen:
1. psychosoziale Belastung,
2. onkologische Symptome,
3. Mangelernährungsrisiko,
4. sozialrechtliche Belange – optional geriatrische und Fatigue Risiken.
Leitfadenbasierte Instrumente wie DT (Distress Thermometer), HADS, MIDOS/IPOS und NRS sind empfohlen. Die aktualisierte DKG Handlungsempfehlung (2024) sorgt für standardisierte Erhebung und Dokumentation; verantwortlich ist die onkologische Fachpflege. Nutzen der ePROs (electronic Patient Reported Outcomes) Elektronische Symptomfragebögen erhöhen die Therapiesicherheit, verbessern die Adhärenz, optimieren das Nebenwirkungsmanagement und reduzieren nicht geplante Krankenhausaufenthalte. Gleichzeitig stärken sie das Patienten Empowerment und fördern eine aktiv mitgestaltete Therapie.
Fazit
Die Integration von PROs in Supportivstrukturen stellt einen entscheidenden Fortschritt in der Patientenzentrierung dar. Das oBS wird zukünftig zentrale Voraussetzung für qualitätsgesicherte Onkologie Zertifizierung sein und verbessert nachweislich Lebensqualität sowie Versorgungseffizienz.
Patient/-innen Coaching bei gastrointestinalen und Hauttumoren
GI Tumoren: Rolle der Cancer Nurse
DGKP Claudia Pressnig (AKH Wien) betonte den zunehmenden Stellenwert von Pflegeberatung und Patient/-innen Coaching im onkologischen Alltag. Durch ambulante Therapieformen, steigende Patientenzahlen und zunehmende Komplexität muss Pflege heute längerfristig strukturierte Betreuung leisten.
Die Cancer Nurse übernimmt die Funktion einer zentralen Ansprechperson, koordiniert Schnittstellen und bietet kontinuierliche Begleitung. Ihr Einsatz verbessert Symptomkontrolle, Selbstmanagement und Therapietreue, reduziert Angst, Hospitalisationen und Abbrüche und stärkt die interdisziplinäre Kommunikation.
Schwerpunkte der Patient/-innen Edukation:
• Fatigue, Übelkeit, Erbrechen, Haut /Nagel /Haarveränderungen, orale Zytostatika, Ernährung.
• Beratung beeinflusst nicht nur Symptomlast, sondern auch die Gesundheitskompetenz.
Beteiligte Faktoren sind individuell und sozioökonomisch – von Motivation und Familienunterstützung bis zu Therapiekomplexität und Polypharmazie. Essentiell ist, dass Pflege Nebenwirkungen aktiv anspricht und nicht auf Patient/-innen-Fragen wartet.
Hauttumoren und Langzeitbetreuung

Linda Morgan (Universitätsspital Zürich) berichtete über die Versorgung im Dermato Onkologischen Zentrum mit > 10 000 ambulanten Patientenkontakten jährlich. Rund 3 500 neue Melanomfälle treten in der Schweiz pro Jahr auf; etwa 300 Menschen sterben daran.
Neue Therapien BRAF und MEK Inhibitoren, PD 1 /CTLA 4 Checkpoint Inhibitoren und deren Kombinationen haben das Überleben fortgeschrittener Melanome substanziell verbessert. Gleichzeitig erfordert die Immunaktivierung ein Management immunvermittelter Nebenwirkungen («irAEs»), die Organtoxizitäten verursachen können und eine frühe, strukturierte Pflegeintervention verlangen. Das Melanom wird zunehmend als chronische Krebserkrankung verstanden. Zentrale Aspekte des Langzeitmanagements sind:
• Survivorship Programme und psychosoziale Stabilisierung,
• Erwartungs und Entscheidungsbegleitung (Shared Decision Making),
• Koordination zwischen Onkologie, Pflege und Psychoonkologie.
Aufgaben der Pflegeexpertin «Skin Cancer» vor und während der Therapie:
• Begleitung zu Arztgesprächen und Aufklärung zur Therapie,
• Anleitung im Nebenwirkungsmanagement, Erfassung somatischer und psychosozialer Belastung,
• frühe Toxizitätsintervention und Förderung der Therapieadhärenz.
Fazit
Cancer Nurses und Pflegeexpert/innen sind essentielle Brückenbauer zwischen medizinischer Therapie und Patientenrealität. Ihr Beitrag zur Nebenwirkungskontrolle, Kommunikation und Kontinuität verbessert nachweislich Behandlungserfolg und Lebensqualität.
Antibody-Drug-Conjugates (ADCs) in der Gynäkologie

Univ.-Prof. Dr. Dr. Sabine Heublein (Universitätsklinikum Ulm) stellte die wachsende Rolle von Antikörper-Wirkstoff-Konjugaten (ADCs) in der Therapie gynäkologischer Tumoren vor. ADCs vereinen die Zielgenauigkeit monoklonaler Antikörper mit der zytotoxischen Potenz klassischer Chemotherapeutika.
Zugelassene Vertreter sind:
• Trastuzumab Emtansin (T-DM1) und Trastuzumab Deruxtecan (T-DXd) bei HER2-positiven Tumoren
• Sacituzumab Govitecan und Tisotumab Vedotin bei fortgeschrittenen Karzinomen
• Mirvetuximab Soravtansin bei FRα-positivem Ovarialkarzinom
• Datopotamab Deruxtecan in klinischer Prüfung
In der MIRASOL-Studie zeigte Mirvetuximab signifikante Verbesserungen des progressionsfreien Überlebens (PFS) und des Gesamtüberlebens (OS) gegenüber einer Chemotherapie bei gleichzeitiger Reduktion hochgradiger Nebenwirkungen. Die häufigste spezifische Toxizität waren okuläre Epithelschäden.
Die DESTINY-PanTumor02-Studie (Phase II) bestätigte einen anhaltenden Nutzen von T-DXd, mit der besten Wirksamkeit bei HER2-IHC-3+-Tumoren.
Datopotamab Deruxtecan zeigte in TROPION-03 eine robuste Aktivität bei metastasierten Ovarial- und Endometriumkarzinomen.
Fazit
ADCs entwickeln sich damit zu einem neuen Grundpfeiler der zielgerichteten gynäkologischen Onkologie.
Fortgeschrittenes Zervixkarzinom

Dr. Frederik Fuchs (LMU München) gab ein Update zur Therapie des fortgeschrittenen Zervixkarzinoms.
Grundlagen und Risiken
Das Zervixkarzinom ist nach wie vor die vierthäufigste Krebserkrankung der Frau und ist stark mit einer HPV-Infektion assoziiert (> 90 %). Zu den wichtigsten Risikofaktoren zählen Rauchen, Immunsuppression, früher Geschlechtsverkehr und ein niedriger sozialer Status.
Therapieprinzipien
In den Stadien IB–IIA haben Operation und Radiotherapie vergleichbare Heilungsraten. Die Therapieentscheidung erfolgt unter Berücksichtigung von Alter, Menopausenstatus und Tumorgrösse.
Standard beim lokal fortgeschrittenen Stadium ist die Radiochemotherapie (RT plus Cisplatin 40 mg/m² wöchentlich) mit anschliessender HDR-Brachytherapie (≥ 90 Gy).
Die Brachytherapie bleibt essenziell für die lokale Kontrolle. Ein Verzicht zugunsten von IMRT-/SBRT-Boost-Konzepten ist mit einer höheren Mortalität assoziiert.
Neue Evidenz
• EMBRACE II: präzisionsgesteuerte, MR-basierte Brachytherapie und Teletherapie mit 5-Jahres-OS von 82 % und einer lokalen Kontrolle von 94 %
• KEYNOTE-A18: Zusatz von Pembrolizumab zur Radiochemotherapie mit einer Risikoreduktion für Progression und Tod um 43 % bei unverändertem Sicherheitsprofil
• INTERLACE: kurze Induktionschemotherapie vor Standard-RT mit signifikanter Verbesserung von OS und PFS
Fazit
Die Integration von Immuntherapie und Induktionschemotherapie in die etablierte Radiochemotherapie verbessert die Langzeitergebnisse. Die Brachytherapie bleibt unverzichtbar. Ihr Erhalt ist entscheidend für das Erreichen kurativer Behandlungsziele.
Therapie des fortgeschrittenen Ovarialkarzinoms

Prof. Isabell Witzel, Direktorin der Klinik für Gynäkologie und des gynäkologischen Krebszentrums am Universitätsspital Zürich, präsentierte zunächst die Zahlen zur Krebsinzidenz und Mortalität in der Schweiz für das Jahr 2022.
Warum ist dieses Thema wichtig?
Für das Ovarialkarzinom existiert kein effektives Screening, die Erkrankung wird häufig erst in einem späten Stadium diagnostiziert, und die Mortalität ist hoch. Daher kommt der Qualitätssicherung eine besondere Bedeutung zu.
Ein effektives Screening-Programm konnte bislang nicht etabliert werden. In der UK Collaborative Trial of Ovarian Cancer Screening (UKCTOCS) wurden 200 000 Frauen im Alter von 50 bis 74 Jahren untersucht. Verglichen wurden ein jährliches Screening mittels CA-125 plus transvaginalem Ultraschall (TVUS), TVUS allein sowie keine Untersuchung. Nach 16 Jahren zeigte sich in allen Gruppen eine Ovarialkarzinomrate von 1 % und eine Mortalität von 0,6 %. Fazit daraus: Ein Screening zur Früherkennung des Ovarialkarzinoms kann derzeit nicht empfohlen werden. Der Schweizer Ansatz umfasst daher kein nationales Screening-Programm in der Allgemeinbevölkerung, sondern fokussiert auf Aufklärung, Familienanamnese sowie genetische Beratung und Testung zur Identifikation von Hochrisikopatientinnen, etwa bei BRCA1/2-Mutationen oder Lynch-Syndrom. Bei gynäkologischen Eingriffen nach abgeschlossener Familienplanung sollte eine opportunistische Salpingektomie erwogen werden, um potenzielle Hochrisiko- oder Vorstufenläsionen in den Eileitern zu entfernen. Dies entspricht einem multimodalen Präventionsansatz.
Management-Prinzipien in der Schweiz
Die Zentralisierung der Versorgung im Bereich der hochspezialisierten Medizin ist das Ergebnis eines mehrjährigen, gesundheitspolitisch geprägten Prozesses. In diesem Rahmen dürfen in der Schweiz ab Januar 2026 nur noch ausgewählte Spitäler Patientinnen mit Ovarialkarzinom behandeln.
Die Behandlung erfolgt in spezialisierten onkologischen Zentren mit multidisziplinären Teams aus Gynäkologen, Onkologen, Pathologen, Radiologen und Genetikern. Hinzu kommen standardisierte Behandlungspfade sowie ein registerbasiertes Monitoring. Das fortgeschrittene Ovarialkarzinom ist als chronische Erkrankung mit multiplen Rezidiven zu verstehen.
Neue Optionen
Pembrolizumab
In der ENGOT-ov65/KEYNOTE-B96-Studie ergaben sich unter Pembrolizumab in Kombination mit wöchentlichem Paclitaxel plus Bevacizumab statistisch signifikante und klinisch relevante Verbesserungen des progressionsfreien Überlebens unabhängig vom PD-L1-Status. Zudem zeigte sich ein Vorteil im Gesamtüberleben bei Patientinnen mit PD-L1 CPS ≥ 1 bei beherrschbarem Sicherheitsprofil.
Mirvetuximab Soravtansin (ADC) beim platinresistenten Rezidiv
Bei Patientinnen mit platinresistentem, FRα-positivem Ovarialkarzinom führte Mirvetuximab Soravtansin gegenüber einer Chemotherapie zu signifikanten Vorteilen hinsichtlich progressionsfreiem Überleben, Gesamtüberleben und objektiver Ansprechrate.
Trastuzumab Deruxtecan (T-DXd) – DESTINY-PanTumor02
Der grösste Nutzen wurde in der IHC-3+-Population beobachtet. Die Daten stützen die potenzielle Rolle von T-DXd als tumoragnostische Therapie bei Patientinnen mit HER2-exprimierenden soliden Tumoren.
Operation im Rezidiv
Wie die DESKTOP-III-Studie zeigte, war bei Frauen mit rezidivierendem Ovarialkarzinom eine zytoreduktive Chirurgie gefolgt von Chemotherapie mit einem längeren Gesamtüberleben assoziiert als eine alleinige Chemotherapie.
Das Follow-up erfolgt in den ersten drei Jahren alle drei Monate, im vierten und fünften Jahr alle sechs Monate und danach jährlich. Es umfasst die gynäkologische Untersuchung sowie die transvaginale Sonographie. Eine Tumormarker-Kontrolle erfolgt nur unter Maintenance-Therapie. Eine CT von Thorax und Abdomen beziehungsweise ein PET-CT wird nur bei klinischem Verdacht auf ein Rezidiv durchgeführt.
Fazit
- Es gibt derzeit kein effektives Screening-Programm.
- Ein multimodaler Ansatz mit genetischer Testung kann Hochrisikopatientinnen identifizieren; opportunistische Salpingektomien im Rahmen gynäkologischer Eingriffe können präventiv relevant sein.
- Die Behandlung sollte zentralisiert erfolgen, auch wenn dieser Prozess nur schrittweise umgesetzt wird.
- Die Therapie umfasst Chirurgie, Chemotherapie und Erhaltungstherapie.
- Eine genetische Testung und HRD-Testung bei Patientinnen mit Ovarialkarzinom ist wichtig, um Kandidatinnen für eine Erhaltungstherapie mit PARP-Inhibitoren zu identifizieren.
- Es besteht ein strukturiertes Follow-up-Programm über fünf Jahre.
Hämatologisch onkologische Therapieinnovationen
CAR T Zellen und bispezifische Antikörper bei grosszelligen B Zell Lymphomen (LBCL)

Dr. Martin Fehr (Kantonsspital Münsterlingen) stellte aktuelle Immuntherapien für rezidivierte oder refraktäre diffuse grosszellige B Zell Lymphome (DLBCL) vor – mit Fokus auf CAR T Zell und bispezifische Antikörper Therapien (bsAb).
Grundlagen
• CAR T Zellen: autologe T Lymphozyten, mit chimären Antigenrezeptoren ausgestattet, die Tumorzellen nach CD19 Erkennung eliminieren.
• Bispezifische Antikörper: binden gleichzeitig an CD3 (T Zelle) und CD20 (Tumorzelle) und aktivieren eine gerichtete zytotoxische Immunreaktion.
Toxizitäten und Management
Cytokine Release Syndrom (CRS) und ICANS (Neurotoxizität) sind häufigste Nebenwirkungen:
• CRS: Fieber, Hypotonie, Hypoxie → Therapie mit Tocilizumab (IL 6 Blockade) und Corticosteroiden.
• ICANS: Neurologische Symptomatik (Tremor, Aphasie, Lethargie) → Dexamethason (leicht) bzw. Methylprednisolon (schwer). Beide Syndrome sind reversibel, erfordern aber standardisiertes Grading und interdisziplinäres Notfallmanagement.
Bispezifische Antikörper – aktuelle Daten
Epcoritamab (subkutan) und Glofitamab (i.v.) bilden neue Säulen ab der zweiten Therapielinie.
• Epcoritamab (EPCORE NHL 1): 42 % komplette Remissionen, anhaltende Langzeitwirkung, meist milde CRS/ICANS Episoden.
• Glofitamab: hohe Wirksamkeit, aber über 50 % Grad 3/4 Nebenwirkungen, Behandlungsdauer max. 12 Zyklen.
Bispezifische AK ermöglichen kontinuierliche, teils ambulante Behandlung und sind auch für Patient/-innen nach CAR T geeignet («Bridging» oder Sequenztherapie).
CAR T Zell Therapie – Klinische Effekte
Zugelassene Produkte: Tisagenlecleucel (Tisa cel), Axicabtagen (Axi-cel) und Lisocabtagen (Liso-cel). Evidenz aus Phase II/III Studien: ZUMA 7: Axi-cel → signifikant besseres Gesamtüberleben (OS) in zweiter Linie versus Standard.
• TRANSFORM: Liso cel → höheres PFS und dauerhafte Remissionen.
• Schuster et al., NEJM 2019: Tisa cel → langanhaltendes Ansprechen bei stark vorbehandeltem DLBCL.
Real World Daten zeigen: vergleichbare Wirksamkeit bei breiterer Patientenauswahl; Axi cel mit höherer Rate schwerer Neurotoxizität (Grad ≥ 3).
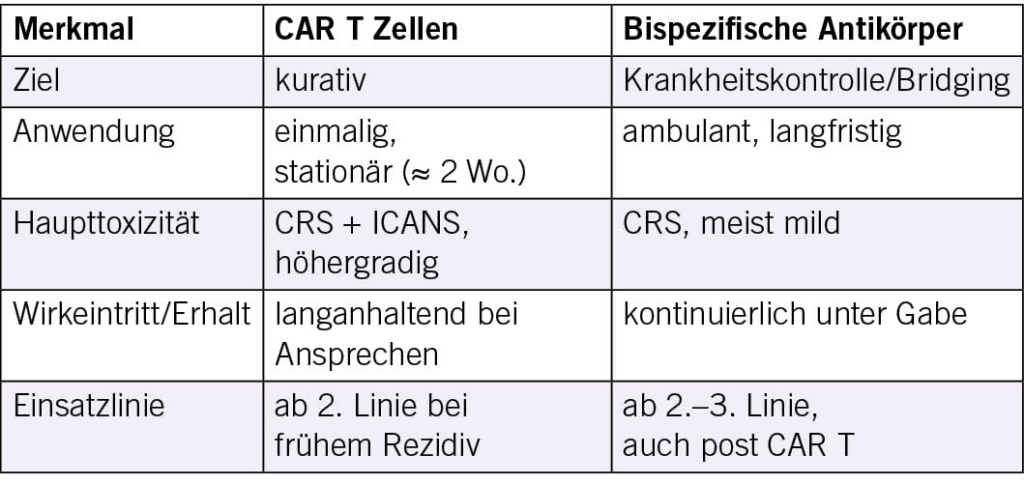
Vergleich CAR T vs. bispezifische Antikörper
Neue Perspektiven: Sequenz oder Kombination (Car T → bsAb oder umgekehrt) werden aktuell in Studien evaluiert z. B. STARGLO (Glofitamab + GemOx).
Fazit
CAR T Zellen und bispezifische Antikörper haben die Therapie des r/r DLBCL grundlegend verändert.
• CAR T: potenziell kurativ bei frühem Einsatz.
• bsAb: flexibel, ambulant und wirksam als Bridging oder Zweittherapie.
Künftige Strategien setzen auf intelligente Kombinationen und individualisierte Sequenzplanung zur Verlängerung der Remissionen.
Rezidivtherapie beim Multiplen Myelom

Dr. Thomas Lehmann (Kantonsspital St. Gallen) stellte die aktuellen Konzepte zur Behandlung des rezidivierten und refraktären Multiplen Myeloms (MM) vor – anhand eines klinischen Beispiels einer 56 jährigen Patientin mit Standardrisiko Zytogenetik und erstem Spätrezidiv nach autologer Transplantation und Lenalidomid Erhaltung.
Rezidivdefinition und klinische Bewertung
Nach der IMWG Klassifikation unterscheidet man:
• Klinisches Rezidiv: neue Osteolysen, Organdysfunktion oder Hyperkalzämie.
• Biochemisches Rezidiv: Verdoppelung des M Proteins oder ≥ 10 g/l Zunahme in zwei Messungen.
• Therapierefraktär: Progress innerhalb von 60 Tagen nach letzter Behandlung.
Für die Therapieentscheidung relevant sind Alter, Frailty, Komorbiditäten und Zytogenetik sowie Dauer und Qualität vorangegangener Antworten.
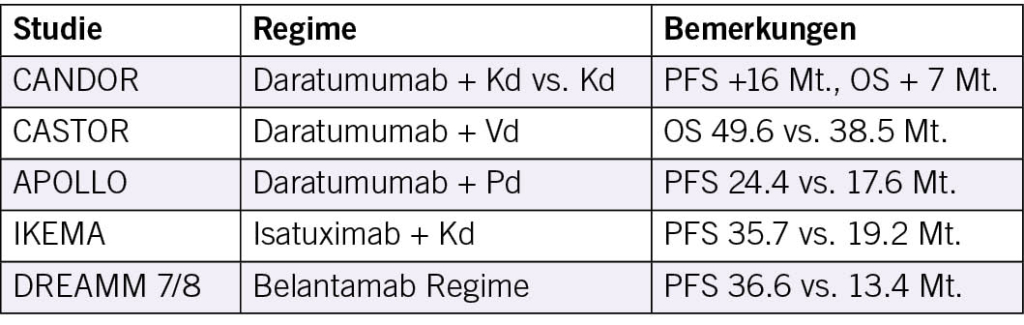
Evidenz für Hauptregime und Studien
Rezidive nach Lenalidomid Erhaltung nehmen zu; daher haben CD38 Antikörper (Daratumumab, Isatuximab) und neue Proteasom Inhibitoren oder IMiDs eine zentrale Rolle:
Weitere Optionen sind Selinexor basierte Triplets (BOSTON Studie: PFS 13,9 vs. 9,5 Monate) und Salvage ASCT, deren Vorteil bereits in randomisierten Studien bestätigt, aber nicht signifikant ist.
Neue Wirkprinzipien und bispezifische Antikörper (BiTEs)
Mit Tec Dara (Teclistamab + Daratumumab) zeigen Daten aus MajesTEC 3 signifikante Verbesserungen gegenüber Standard Triplets (DPd / DVd) bei rezidivierten und IMiD refraktären Verläufen. Zunehmend werden auch BCMA und GPRC5D gerichtete Therapien (CAR T, BiTE) in die früheren Linien verschoben, mit dem Ziel dauerhafter MRD Negativität.
Therapiesequenz und Patientenfaktoren
Entscheidend für die Therapiewahl:
1. Erkrankung: Tempo, Organbeteiligung, Cytogenetik.
2. Patient: funktionales Alter (Frailty), Komorbidität, Therapietoleranz.
3. Vorbehandlung: Art und Ansprechen der individuellen Exposition.
4. Zulassung/Verfügbarkeit: CAR T Zellen und BiTE aktuell ab Linie 3.
Strategisches Vorgehen: Sequenzierung entlang biologischer Zielstrukturen (CD38 → IMiD → Proteasom Inhibitor → BCMA) und früher Einsatz immunologischer Therapiebausteine.
Fazit
Das moderne Rezidiv Management des Multiplen Myeloms erfordert eine präzise, molekulargestützte Therapiesequenzierung. CD38 basierte Triplets bleiben Standard; BCMA gerichtete CAR T Zellen und BiTEs eröffnen neue Optionen für Refraktärstadien – mit dem langfristigen Ziel funktioneller Kuration.
Prämaligne Stadien: MGUS und Smoldering Multiple Myeloma (SMM)

Prof. Dr. Felicitas Hitz (Kantonsspital Münsterlingen) beleuchtete die Bedeutung von monoklonalen Gammopathien als prämaligne Erkrankungen und die aktuellen Strategien zur Risikostratifikation und Frühintervention.
MGUS – Monoklonale Gammopathie unbestimmter Signifikanz
MGUS ist eine häufige, asymptomatische Präkanzerose mit einer Inzidenz von 3–5 % bei Personen über 50 Jahren. Sie ist durch ein M Protein < 30 g/l, < 10 % Plasmazellinfiltration und Fehlen von Endorganschäden (CRAB Kriterien) definiert. Das Progressionsrisiko liegt bei etwa 1 % pro Jahr.
Risikostratifikation (Mayo Clinic Modell):
Je ein Punkt für M Protein > 15 g/l, IgA/MGUS Subtyp, und abnorme Leichtketten-Ratio.
• 0 Punkte → nur 5 % Progression nach 20 Jahren.
• 3 Punkte → Progressionsrisiko ≈ 60 %.
Sonderformen
IgM MGUS: 1 % Progression / Jahr → Waldenström Makroglobulinämie oder Amyloidose.
• Non-IgM und Leichtketten MGUS: seltenere Verläufe → Multiples Myelom.
• Epidemiologische Aspekte: Erstgradige Verwandte von Patient/-innen mit Myelom tragen ein > 2,4-fach erhöhtes Risiko; bei Personen afrikanischer Abstammung liegt es über 5-fach höher.
Die isländische iStopMM Studie (> 80 000 Teilnehmende) bestätigte eine MGUS Prävalenz von 0,5 % ab 40 Jahren und prüft Nutzen eines populationsbasierten Screenings – Langzeitresultate stehen noch aus.
SMM – Smoldering Multiple Myeloma
SMM gilt als Übergang zwischen MGUS und aktivem Myelom mit höherer Tumorlast, aber ohne klinische Symptomatik.
Progressionsrisiko: ca. 50 % innerhalb von 5 Jahren bei Hochrisiko Profil.
Risikomodelle:
• PETHEMA (2007): ≥ 95 % aberrante Plasmazellen + Immundefizienz = High-Risk.
• Mayo 2018: ≥ 2 der Faktoren (M Protein > 2 g/dl, Plasmazellen > 20 %, FLC Ratio > 20).
• IMWG 2020: kombinierter Score > 12 definiert Hochrisiko.
Frühe Intervention und Behandlungsstrategien
Traditionell war Beobachtung («watch and wait») Standard. Neue Daten stützen bei hohem Risiko eine aktive Therapie:
• Lenalidomid ± Dexamethason: verzögert die Progression signifikant (QuiRedex, ECOG E3A06).
• Daratumumab (AQUILA Phase 3): reduziert Progressions- und Sterberisiko im Vergleich zur Beobachtung.
• GEM CESAR (Phase 2): intensives «kurativeres» Schema (KRd → ASCT → Konsolidierung + Erhaltung) erreichte dauerhafte MRD Negativität bei > 20 % der Patient/-innen über vier Jahre.
Empfehlungen 2025
• Kein Routinescreening in der Allgemeinbevölkerung; Screening bei familiärem oder ethnisch definiertem Risiko empfohlen.
• Diagnostische Abgrenzung zwischen MGUS, SMM und aktivem Myelom muss klar bleiben – Biomarker basierte Stratifizierung ist entscheidend.
• Risikoadaptiertes Monitoring nach MGUS/SMM Kategorie
(Verlaufsintervall, FLC, M Protein, Bildgebung).
• Bei High-Risk SMM: frühe Behandlung mit Lenalidomid oder Daratumumab-basierten Schemata im kontrollierten Rahmen.
• Langfristiges Ziel: frühe MRD Negativität und potenzielle Kuration im präklinischen Stadium.
Gesamtfazit der Fortbildung
Die 36. St. Galler Fortbildung 2024 zeigte deutlich:
• Immun und zielgerichtete Therapien haben in allen grossen Tumorentitäten klinische Standards nachhaltig verändert.
• Präzisionsmedizin und biologische Integration ersetzten rein sequenzielle Behandlungslogik.
• Pflege, Supportivmedizin und Patient/-innen Einbindung sind integraler Bestandteil moderner Onkologie.
• In der Hämatologie wird der Übergang von chronischer Kontrolle zur potenziellen Kuration greifbar.
Die Veranstaltung unterstrich die Verantwortung aller Behandlungsdisziplinen, Evidenz und Praxisnahe Individualisierung zu verbinden, um Patient/-innen eine sichere, hochqualitative und zugängliche Onkologie zu ermöglichen.
riesen@medinfo-verlag.ch