Die multidisziplinäre Behandlung von Weichteilsarkomen (Englisch, soft tissue sarcoma, STS) ist in verschiedenen Guidelines festgehalten, so beispielsweise in den ESMO Guidelines 2021, in der deutschen S3-Leitlinie 2021 für STS und in Onkopedia 2019. Trotz vieler klarer Statements für das diagnostische und therapeutische Vorgehen bei STS, bleiben viele Fragen unbeantwortet oder kontrovers. Prospektive Studien fehlen zu vielen der über 100 STS Subtypen, die in der 5. WHO-Klassifikation 2020 beschrieben sind. Biologisch unterschiedliche Sarkome gleichermassen zu behandeln ist problematisch. Die Inzidenz liegt auch bei den häufigsten STS Subtypen, wie den Lipo- und Leiomyosarkomen bei < 1/100’000/Jahr, womit die STS definitiv in die Kategorie der seltenen Tumore gehören.
Die Idee
Onkologische Konsensuskonferenzen zu kontroversen Standpunkten in Diagnostik, Therapie und Nachsorge von Karzinomen, über welche international renommierte Experten abstimmen, haben in der Schweiz bereits eine lange Tradition. Weltweit bekannt sind die St. Galler Brustkrebskonferenz, heute «International Breast Cancer Conference (bcc)» genannt, die 2021 zum 17. Mal durchgeführt wurde und die «Advanced Prostate Cancer Consensus Conference (APCCC)», welche seit 2015 ausgetragen wird. Beide Konferenzen erreichen durch ihre Internationalität und den Konsensus-bildenden Austausch der Experten hohe Aufmerksamkeit.
Eine Konsensuskonferenz schien uns für STS umso nötiger, als das Erreichen einer genügenden Evidenz über prospektiv kontrollierte Studien an der Seltenheit der einzelnen STS-Subtypen immer wieder gescheitert ist. Und doch braucht es akzeptierte Vorgehensweisen im klinischen Alltag, verbindliche Therapiestandards und Qualitätsindikatoren. Diese sollen die Grundlage bieten für Behandlungspfade, Verhandlungen mit den Krankenversicherern, für Argumente in der Politik und für die Planung klinischer Studien in internationaler Zusammenarbeit.
Im Oktober 2020 hatten wir die CSSS-Initiative an der EORTC Soft Tissue and Bone Sarcoma Group (STBSG) Halbjahresversammlung vorgeschlagen und dafür viel positives Echo erhalten. 2021 formulierten acht verschiedene interdisziplinäre Arbeitsgruppen in 22 Zoom-Sitzungen «Statements of Controversy» für STS, welche anschliessend von einer Kern-Expertengruppe in 220 Fragen umformuliert wurden. Diese Fragen wurden 62 internationalen Sarkom-Experten aus unterschiedlichen Disziplinen zur Abstimmung vorgelegt und anschliessend ausgewertet. Die Resultate der Umfrage haben wir am 20 und 21.5.22 in St. Gallen präsentiert und angeregt diskutiert. Die CSSS Diskussionsteilnehmer wurden eingeladen, über 62 Fragen erneut abzustimmen, um spezielle Diskussionspunkte zu vertiefen. Bei der ersten und der zweiten Umfrage gab es Fragen mit Einfachauswahl und solche, bei denen mehrere Antworten erlaubt waren. Zusätzlich war bei jeder Frage die Option «Enthaltung» möglich, wenn man sich in diesem Bereich nicht kompetent fühlte oder den Eindruck gewann, die Frage sei nicht eindeutig gestellt. Bei 33% oder mehr Enthaltungen wurde die Frage für die Auswertung gestrichen. Wir definierten in CSSS einen Konsensus bei ≥ 75% und einen klaren Konsensus bei ≥ 95% Übereinstimmung.
Wichtigste Erkenntnisse aus der Konsensus Konferenz (CSSS)
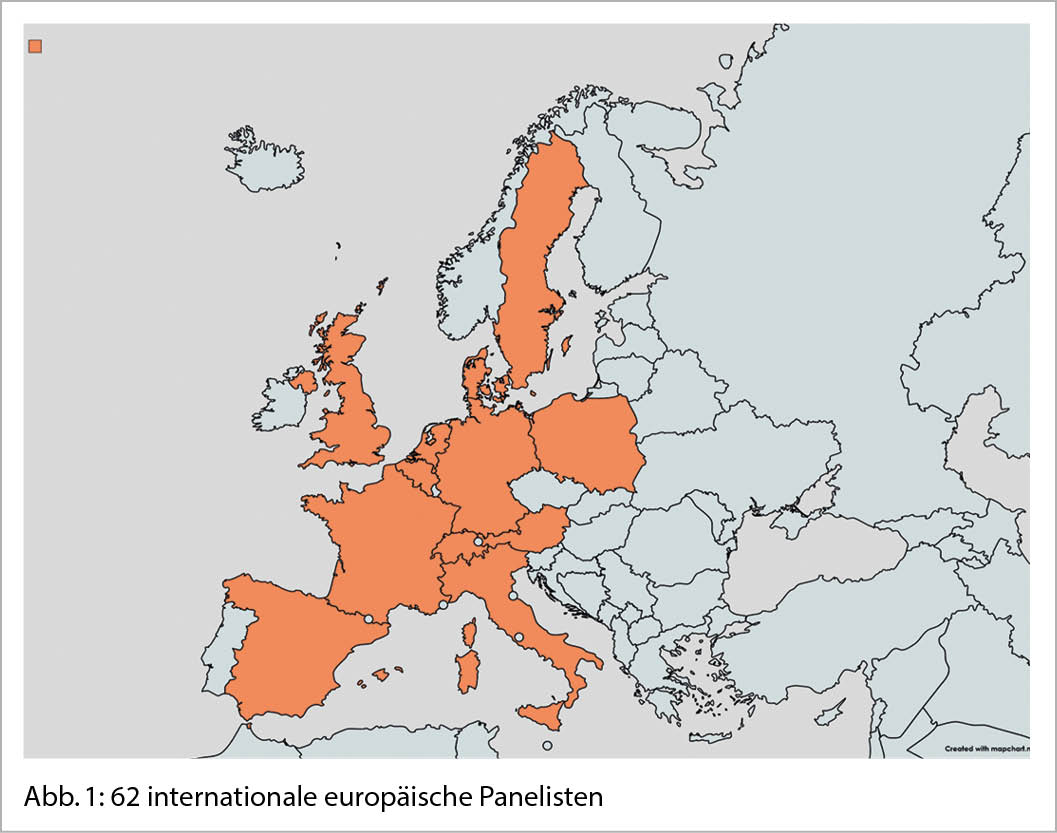
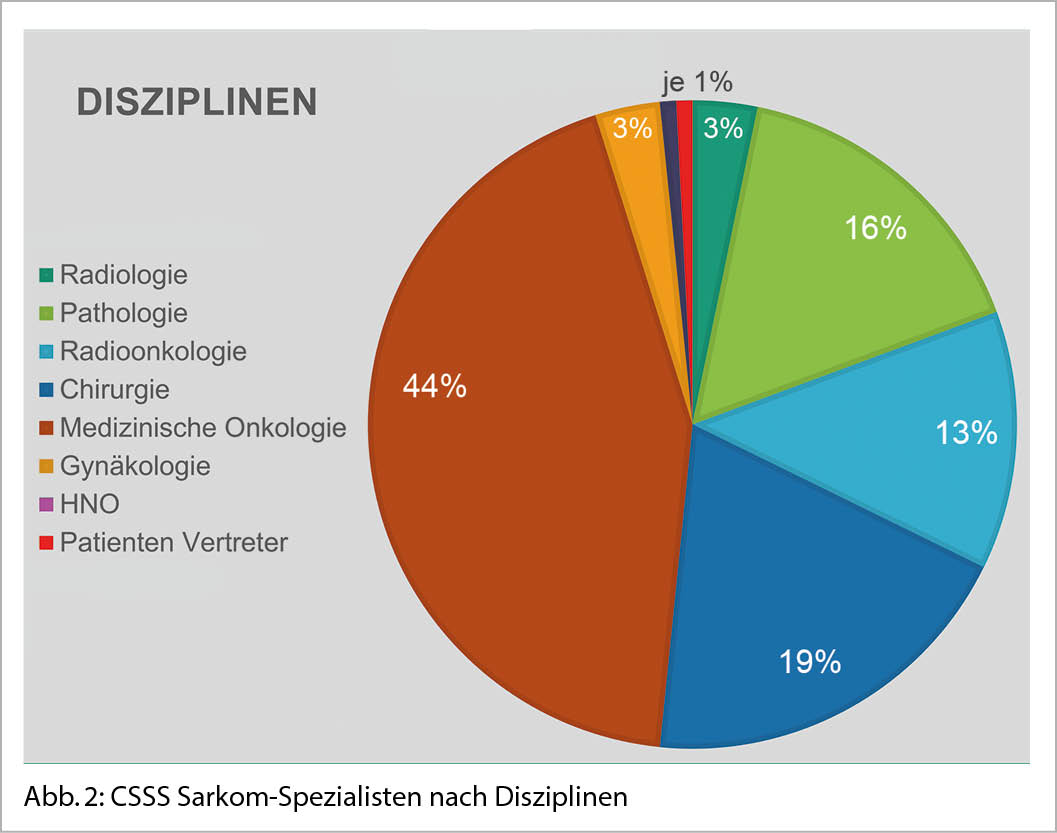
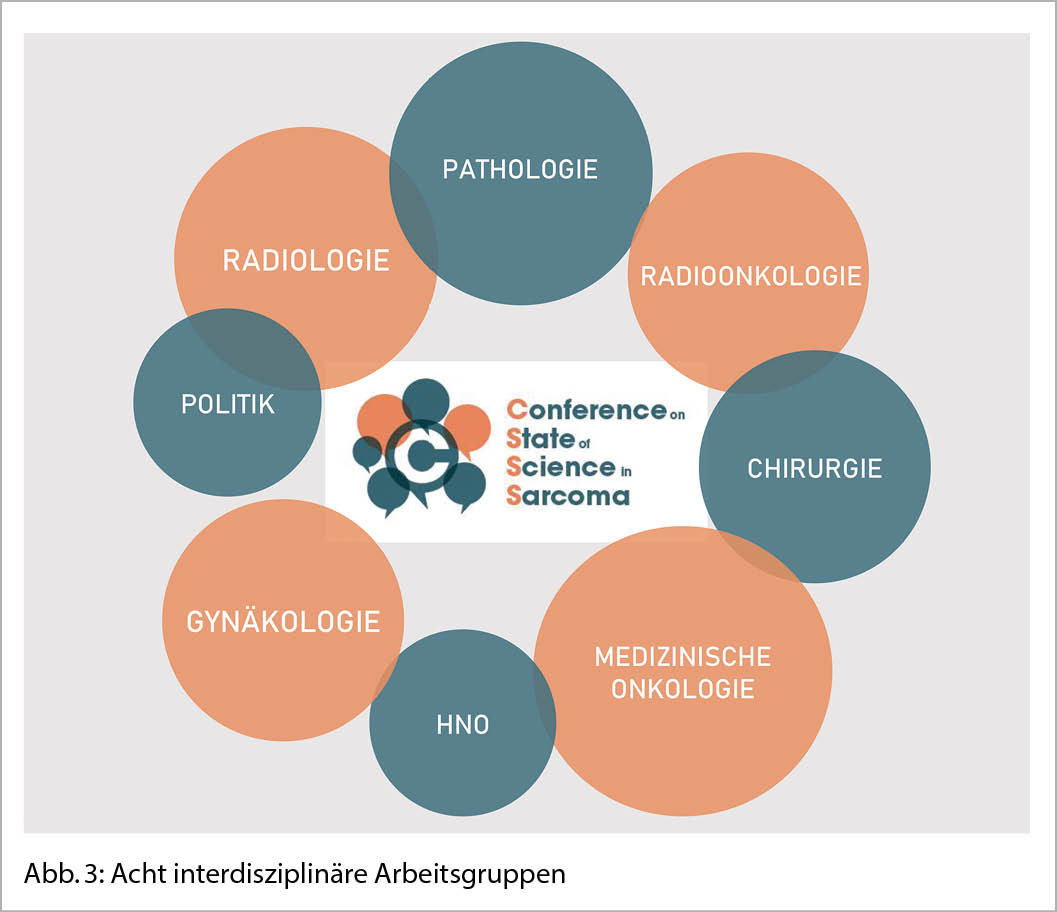
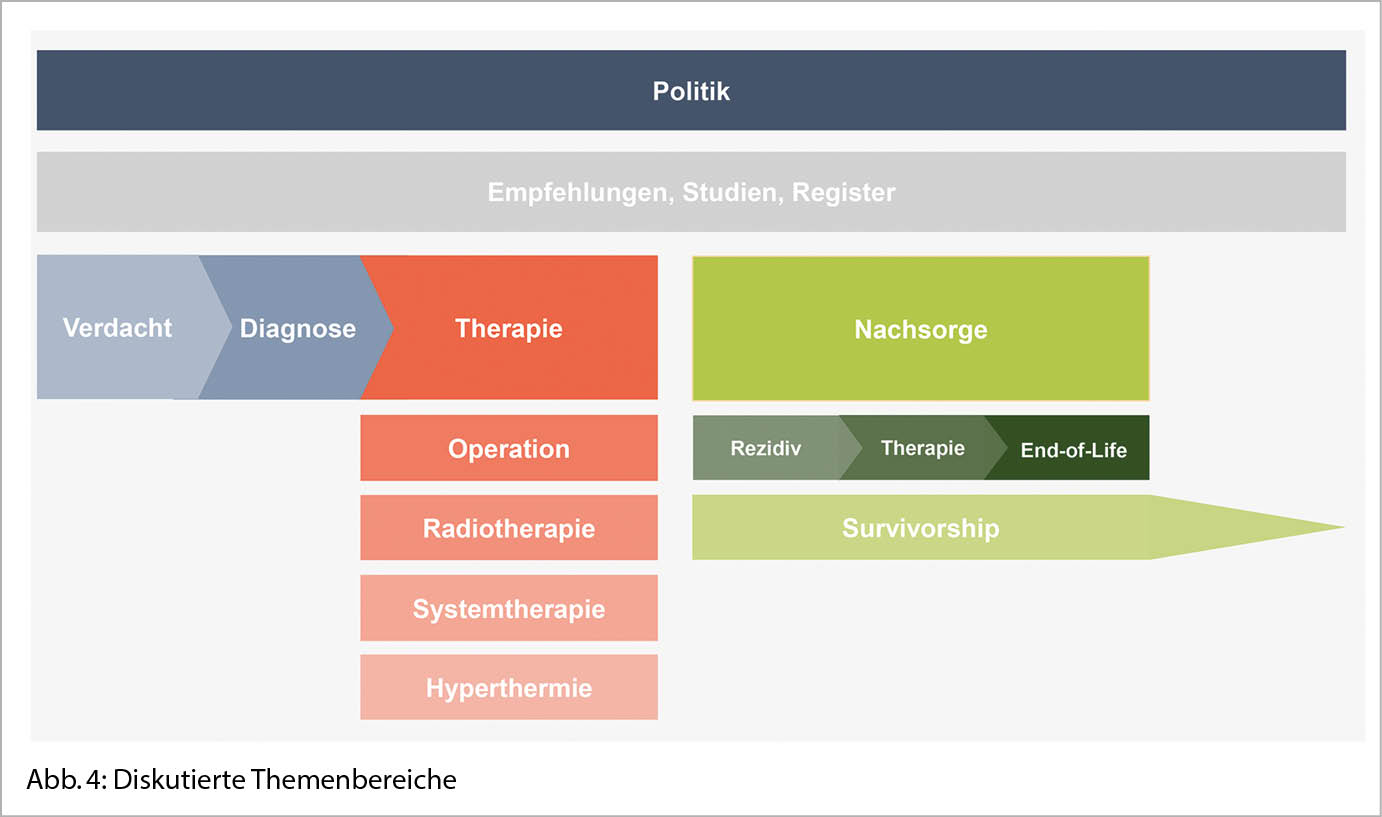
Auch in Zeiten der Pandemie ist ein internationaler Austausch über eine Zeitperiode von eineinhalb Jahren sehr effizient und kostengünstig gelungen. Zweiundsechzig europäische und schweizerische Sarkomspezialisten aller Disziplinen (Abb. 1 und 2) haben in acht Arbeitsgruppen (Abb. 3) folgende Themen diskutiert (Abb. 4).
1. Diagnostik
Sarkom-Pathologie und -Radiologie sind die beiden Grundpfeiler der STS Diagnostik. Sie komplementieren sich, was eine gute Kommunikation beider Disziplinen voraussetzt. Kriterien für das Grading von STS sind bereits aus dem Biopsiematerial (geführt durch eine zuvor veranlasste Bildgebung) von Bedeutung, bieten doch präoperative Therapien bei Hochrisiko-STS in mehrfacher Hinsicht Vorteile für einen kurativen Therapieansatz. Eine Standardisierung von Pathologieberichten mit integrierten Angaben zu den radiologischen Befunden wird gefordert. Gleiche Anforderungen werden an das postoperative Response Assessment gestellt. Ein klarer Konsens (100% Zustimmung) besteht darin, dass mesenchymale Tumoren mit ungewöhnlicher Morphologie, biologischem Verhalten oder molekularen Aberrationen zwingend von einem Referenz-Sarkom-Pathologen beurteilt werden müssen. Folgenden Kriterien, die ein Referenz-Pathologen erfüllen soll, wurde mehrheitlich zugestimmt: Vorhandensein von Qualitätskontrollen in der Diagnostik am Institut, regelmässige Teilnahme am interdisziplinären SarkomTumorboard, Zusammenarbeit mit validierten Laboren für die molekulare Diagnostik, regelmässiger Austausch mit Referenzpathologen, Kenntnisse zu den neuesten diagnostischen Techniken (Antikörper, molekulare Assays), regelmässige Durchführung von NGS, Ausbildung für mindestens 1 Jahr an einem Institut mit einem Referenz-Pathologen, wissenschaftliche und Ausbildungsfunktionen auf dem Gebiet der Sarkom-Pathologie, mehr als 100 STS Primärdiagnosen pro Jahr.
2. Perioperatives STS Management
Viel zu diskutieren gab das perioperative STS Management. Zwar gibt es Daten zur perioperativen Systemtherapie bei Hochrisiko-STS, es fehlt aber bis dato eine Studie mit einem Observationsarm ohne eine entsprechende Systemtherapie. Unklar ist die genaue Definition von «Hochrisiko-STS», hier werden Grösse, Tiefe und Grading als Risikoindikatoren verwendet, alternativ wird das SARCULATOR Tool, welches jedoch nur einen Teil der STS Subtypen berücksichtigt, zur Risikoberechnung herangezogen oder auch molekulare Signaturen. Weiterhin fehlen robuste Daten zur Dauer einer perioperativen Systemtherapie, zum besten Zeitpunkt derselben (prä- oder postoperativ), zu den am besten geeigneten Medikamenten. Die Wahl der Substanzen ist wiederum erschwert durch die zahlreichen STS-Subtypen. Als optimaler primärer Endpunkte für eine künftige Studie zur perioperativen Systemtherapie, wurden DFS und OS als etwa gleichwertig beurteilt.
Ähnlich gibt es zur perioperativen Radiotherapie (RT) offene Fragen. Bei den Sarkomen – wie auch bei einigen andern Tumoren – werden zunehmend Kurzprotokolle angewendet, deren Gleichwertigkeit in Studien zurzeit gerade validiert wird mit entsprechenden Modifikationen der Dosis. Auch wenn bei der RT eine präoperative Applikation bevorzugt wird, konnten Argumente für eine postoperative Radiotherapie formuliert werden, nämlich Sorge vor Wundheilungsstörungen oder einer Diskrepanz zwischen Grading von Biopsie und initialer Bildgebung.
3. Operatives Vorgehen
Die Planung einer kurativen Resektion erfolgt nach initialer Bildgebung und histologischer Aufarbeitung der obligaten prätherapeutischen Biopsie am interdisziplinären Sarkom-Tumorboard. Dabei werden vom Chirurgen die Wahrscheinlichkeit einer R0-Resektion eingeschätzt und die dafür unterstützenden Vortherapien besprochen. Für Sarkome im Retroperitonealraum ist aus anatomischen Gründen oft nur eine R1-Resektion möglich und wird entsprechend akzeptiert. In Ausnahmefällen kann bei Extremitätensarkomen eine geplante marginale Resektion durchgeführt werden, wenn dadurch ein relevanter Funktionsverlust verhindert werden kann.
Anlass zu vielen Diskussionen gab die Indikation für eine Re-Resektion im Falle von positiven Resektionsrändern mit oder ohne makroskopischen Tumorrest. Diese Situation wird vor allem nach ungeplanten Resektionen angetroffen (sogenannte «Whoops»- Resektionen), die durch Antizipation und erhöhte Aufmerksamkeit vor allem unter Allgemeinchirurgen ausserhalb von Sarkom-Netzwerken verhindert werden müssen.
Ein klarer Konsens konnte darüber erreicht werden, dass die Prinzipien der Sarkom-Chirurgie auch für die Disziplinen der Kopf-Hals Chirurgie, der Dermatologie und der gynäkologisch tätigen Chirurgen gelten sollen.
4. Oligometastasierung
Um über therapeutische Optionen (kurativ versus palliativ) bei Oligometastasierung diskutieren zu können, musste zunächst über die Definition «Oligometastasierung bei STS» abgestimmt werden. Die Kriterien, welche favorisiert werden, sind: Anzahl der Läsionen (knapp die Hälfte der Panelisten stimmten dafür), gefolgt von Anzahl der betroffenen Organe, das Intervall zur Primärdiagnose und die Wachstumsdynamik der Läsionen und schlussendlich eine Vorgeschichte von STS Metastasen beim Patienten. Ein Konsensus konnte erreicht werden bei synchron aufgetretenen Lungenmetastasen zum Zeitpunkt der STS-Diagnose, wo zunächst eine Verlaufsbildgebung durchgeführt werden soll, bevor eine lokale Therapie angeboten wird.
5. Fortgeschrittene STS Erkrankung
Die Molekularpathologie wird immer relevanter für Therapieentscheidungen beim fortgeschrittenen STS. War bis vor kurzem eine Anthrazyklin Monotherapie (ev. kombiniert mit Ifosfamid bei Therapiedruck) als Erstlinientherapie in der palliativen Situation akzeptiert, so werden zunehmend zielgerichtete Therapieansätze in der ersten und weiteren Therapielinien gemäss molekularem Profil gefordert. Die Verfügbarkeit solcher Medikamente, die dafür aber nicht zugelassen sind, stellen grosse Hürden dar. Hier ist die Politik gefragt und eine nationale und internationale Harmonisierung des Vorgehens.
Da randomisierte Studien bei kleinen Fallzahlen häufig nicht realisierbar sind, werden Registerdaten, Daten zur Lebensqualität und zu Patient Reported Outcome (PRO) zur Argumentation mit den regulatorischen Behörden benötigt. All diese Schritte und Massnahmen sind nur, wie in unserer Konsensus Konferenz angeregt, mit internationaler Zusammenarbeit möglich und über Therapieprotokolle, welche von akademischen Konsortien, wie beispielsweise der EORTC, entworfen werden.
Konklusion und Ausblick
Nicht überraschend, gab es nur bei wenigen Fragen einen Konsens, oder gar einen klaren Konsens. Der positive Zugewinn, den wir aus solchen Konsens-Voten für den klinischen Alltag ableiten wollen, ist beispielsweise eine Verhandlungsbasis mit den Krankenkassen für eine off-label Therapieempfehlung. Verbleibende kontroverse Standpunkte sollen in prospektiven Studien in internationaler Kollaboration untersucht und geklärt werden. Dafür eignet sich die EORTC unter deren Patronat die CSSS Initiative entstanden ist.
Eine interessante Übereinstimmung fand sich bei der Suche nach standespolitischen Kriterien für Sarkom-Spezialisten der diversen Disziplinen (Qualitätskriterien).
Auf allgemeinen Wunsch der Panelisten soll CSSS 2024 wiederholt werden.
Die Resultate der ersten und der zweiten CSSS Umfrage sollen in einem Peer-Reviewed Paper publiziert werden.
Wir danken an dieser Stelle den 62 Panelisten, welche tatkräftig zum Gelingen dieser ersten Conference on State of Science in Sarcoma (CSSS) beigetragen haben.
Universitätsspital Zürich
Institut für Pathologie und Molekularpathologie
Schmelzbergstrasse 12
8091 Zürich
silvia.hofer@usz.ch
Leitender Arzt / Leitung Ambulatorium St. Gallen & Rorschach
Kantonsspital St. Gallen
Klinik für Med. Onkologie/Hämatologie
Rorschacher Strasse 95
9007 St. Gallen