Im Rahmen der Donnerstagskonferenz (DOKO) des Universitätsspitals Basel sprach Prof. Dr. med. Christian Meier, Basel, über die Therapie der Osteoporose. Zur Behandlung der Osteoporose steht heute eine breite Palette von Medikamenten mit unterschiedlichen Wirkmechanismen zur Verfügung. Trotz einer hohen Inzidenz Osteoporose-bedingter Knochenbrüche werden auch in der Schweiz gerade Hochrisikopatienten zu selten behandelt. Man spricht gar von einer «crisis of osteoporosis», wie der Referent anmerkte. Gelingt es, Unsicherheiten bezüglich der Therapie (z.B. Nebenwirkungen, Therapiedauer, Management nach Therapieende) auszuräumen, kann dies die Akzeptanz einer Osteoporose-Therapie deutlich verbessern.
Charakteristische Kennzeichen einer Osteoporose sind eine fortschreitende Verminderung der Knochendichte (BMD, bone mineral density) und eine Veränderung der Knochenarchitektur, was sich klinisch in einem erhöhten Risiko für Knochenbrüche zeigt.
Eine medikamentöse Behandlung der Osteoporose wird angestrebt, wenn die Patienten bereits eine Wirbel- oder proximale Femurfraktur erlitten haben, nach peripheren Frakturen infolge nur geringfügiger Traumata, nach dem Befund eines erhöhten Frakturrisikos mittels FRAX® (Fracture Risk Assessment Tool, WHO) und auch ohne Fraktur bei Feststellung eines erhöhten 10-Jahres-Frakturrisikos oder eines T-Scores (Lendenwirbelsäule oder Femur) von < - 2.5 (1).
Antiresorptive Behandlung
Zur antiresorptiven Behandlung werden zum einen Bisphosphonate eingesetzt. Bisphosphonate akkumulieren im Knochen und werden im Rahmen des Knochenumbaus freigesetzt, von Osteoklasten aufgenommen und hemmen deren Aktivität. Gerade neuere Vertreter der Bisphosphonate wie Alendronat oder Zoledronat zeichnen sich durch eine sehr hohe Affinität für den Knochen aus, was mit dem Vorteil einer ausgesprochen dauerhaften Langzeitwirkung einhergeht. Die Bisphosphonate sind die einzigen Medikamente zur Behandlung der Osteoporose, deren Wirkung deutlich über den Anwendungszeitraum hinaus anhält.
Denosumab, ein monoklonaler Antikörper, bindet RANKL (Receptor Activator of NF-κB Ligand), ein Protein, das Entwicklung, Funktion und Überleben von Osteoklasten sicherstellt und damit die Knochenresorption fördert. Denosumab erhöht die Knochendichte was sich in einer anhaltenden Reduktion des Frakturrisikos bei postmenopausalen Frauen gezeigt hat (2). Denosumab wird alle 6 Monaten subkutan appliziert, die Wirkung bleibt jedoch nur für die Dauer der Therapie bestehen. Ein Jahr nach Absetzen geht die Knochendichte wieder auf den Ausgangswert vor der Behandlung zurück (Rebound-Effekt). Bei gewissen Patienten (z.B. Frakturen vor Denosumab-Behandlung, keine Vorbehandlung, sehr geringe Knochendichte) steigt das Frakturrisiko nach einer Denosumab-Behandlung deutlich an. In seltenen Fällen kann es sowohl unter Bisphosphonaten als auch unter Denosumab zu einer Kiefer-Osteonekrose oder atypischen Femurfrakturen kommen.
Anabol wirkende Therapeutika
Teriparatid, ein Analogon des Parathormons, verstärkt die Knochenneubildung. Teriparatid wird bei Patienten nach Osteoporose bedingten Frakturen oder bei Glukokortikoid-induzierter Osteoporose mit ungenügendem Ansprechen auf andere Therapien zur Zweitlinienbehandlung eingesetzt. Im Vergleich mit Risedronat hat sich mit der anabolen Therapie bei schwerer Osteoporose eine deutliche Reduktion der Inzidenz vertebraler Frakturen gezeigt (3). Die überlegene Wirkung von Teriparatid wurde auch bei behandlungsnaiven Patienten deutlich, was für eine Erweiterung der Zulassung auch für die Erstlinientherapie spricht.
Romosozumab (bisher nur in Japan zugelassen) bindet das Protein Sklerostin, welches die Aktivität der Osteoblasten hemmt. Mit der Inhibition von Sklerostin stimuliert der monoklonale Antikörper die Knochenformation. Interessanterweise wird (im Gegensatz zu Teriparatid) auch die Knochenresorption gehemmt. Dies führt zu einer ausgeprägt starken anabolen Wirkung am Knochen mit einer Akkumulation neuegebildetem Knochens. Bei guter Verträglichkeit konnte mit Romosozumab (210 mg/Monat) eine Zunahme der Knochendichte der Lendenwirbelsäule nach 12 Monaten um 11.3% (verglichen mit Placebo - 0.1%, Alendronat + 4.1%, Teriparatid +7.1%) erreicht werden (4). Auch nach Absetzen von Romosozumab kommt es wieder zu einer Abnahme der Knochendichte.
Individualisierte Therapie der Osteoporose
Empfohlen wird eine individualisierte Osteoporosetherapie. Die Behandlung richtet sich nach der klinischen Beurteilung (Frakturrisiko, Alter etc.), der Wirksamkeit und Sicherheit der Therapeutika, den Kosten und der Patientenpräferenz. Letztere spielt für den Alltag häufig die grösste Rolle, wie der Referent betonte.
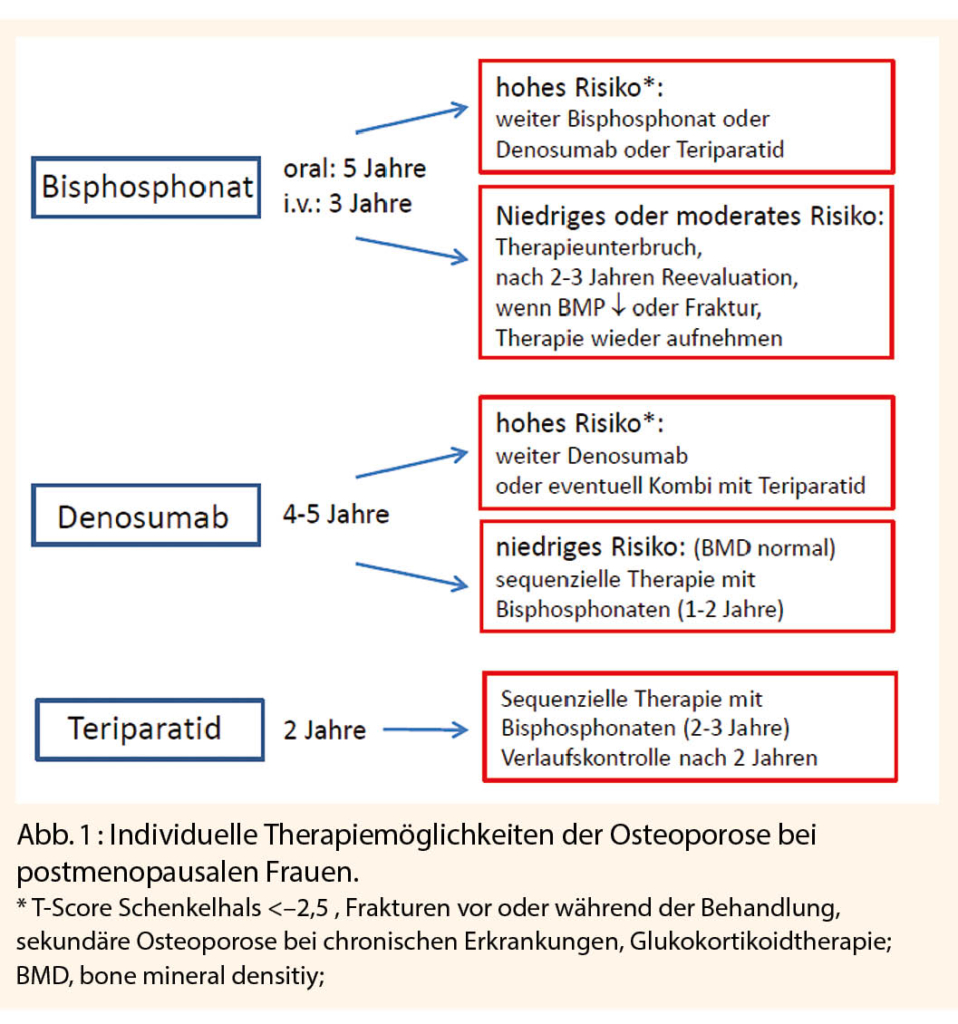
Orale Bisphosponate werden initial für 5 Jahre, intravenös verabreichte für 3 Jahre gegeben, für Denosumab liegt die Behandlungsdauer zunächst bei 4-5 Jahren (siehe Abb. 1). Bei niedrigem bis moderatem Risiko kann die Behandlung mit Bisphophonaten für 2-3 Jahre unterbrochen und die Situation dann reevaluiert werden. Bei abnehmender Knochendichte oder einer Fraktur kann die Behandlung wieder aufgenommen werden. In diesem Risikobereich kann bei Erreichen einer Normalisierung der BMD mit einer Denosumab-Therapie der monoklonale Antikörper abgesetzt werden, zwingend ist aber eine sequenzielle Therapie mit einem Bisphosphonat notwendig, um den Rebound-Effekt mit gesteigertem Knochenmassenverlust zu verhindern.
Bei hohem Frakturrisiko können Bisphosphonate sowie Denosumab nach Abwägen von Nutzen und Risiko auch länger angewandt werden. Alternativ kann nach einer Bisphosphonattherapie auch eine sequenzielle Therapie mit Denosumab oder Teriparatid in Erwägung gezogen werden. In einer Hochrisikosituation könnte auch eine Kombinationstherapie von Denosumab mit Teriparatid sinnvoll sein.
Die Anwendung von Teriparatid ist auf 24 Monate beschränkt. Auch hier sollte nach der Teriparatid-Therapie sequenziell mit einem Bisphophonat behandelt werden.
Besonders Patienten mit schwerer Osteoporose und hohem Frakturrisiko profitieren von einer sequenziellen Behandlung, beginnend mit einer Knochen aufbauenden Therapie (5).
Quelle: Prof. Dr. med. Christian Meier: Update Osteoporose: wie und wie lange behandeln? Donnerstagskonferenz am 23.3.2019; Fortbildungsreihe des Bereichs Medizin des Universitätsspitals Basel.
Quelle: Prof. Dr. med. Christian Meier: Update Osteoporose: wie und wie lange behandeln? Donnerstagskonferenz am 23.3.2019; Fortbildungsreihe des Bereichs Medizin des Universitätsspitals Basel.