Vom 20. bis 22. März 2025 fand der traditionelle Review Kurs Kardiologie Zürich organisiert von der Klinik im Park und der Agentur And Frank am Flughafen Zürich statt. Die Organisatoren hatten in Zusammenarbeit mit der Mayo Clinic Rochester wiederum ein reichhaltiges und spannendes Programm zusammengestellt. Der folgende Bericht fasst einige der zahlreichen Vorträge zusammen.
Herzfrequenz – up and down
Tachykardiopathie
Arrhythmie induzierte oder vermittelte Kardiopathie

Bei einer induzierten Arrhythmie (klassische Definition) ist die Arrhythmie die alleinige Ursache der ventrikulären Dysfunktion. Bei der vermittelten Arrhythmie verstärkt die Arrhythmie die ventrikuläre Dysfunktion und/oder verschlechtert die vorbestehende Herzinsuffizienz, stellte Dr. med. Eva Bühlmann, Cardiopark AG Zürich, einleitend fest. Die Inzidenz für Vorhofflattern (HF > 100/min, 10–20 %), Vorhofflimmern (HF > 100/min, 15–30 %), ventrikuläre Extrasystolen (VES) ist insgesamt gering, ca. 5.4 % in 5–6 Jahren, Kardiomyopathien können bereits ab 10 % VES-Häufigkeit auftreten.
Das Management dieser Erkrankungen erfordert eine frühzeitige Diagnosestellung, da sie bei adäquater Therapie potenziell reversibel sind. Insbesondere VES sollten bei neu aufgetretener linksventrikulärer Dysfunktion als Differenzialdiagnose in Betracht gezogen werden. Die klassische Klinik umfasst Symptome und Zeichen einer progredienten Herzinsuffizienz. Eine über mehr als 10–15 % des Tages anhaltende Tachykardie mit einer Herzfrequenz über 100/min gilt als bedrohlich. Allerdings existiert keine klar definierte Schwelle der Herzfrequenz, die per se zur Entwicklung einer Kardiopathie führt. Auch die Ruhefrequenz ist diagnostisch oft wenig aussagekräftig.
Eine proaktive Behandlung wird empfohlen, wobei die Wahl der Strategie von der zugrunde liegenden Arrhythmie abhängt – im Vordergrund stehen dabei Frequenzkontrolle versus Rhythmuskontrolle. Die potenziell kurative Ablation ist in vielen Fällen die Therapie der Wahl, insbesondere bei supraventrikulären Tachykardien (SVT), aber auch bei Vorhofflimmern, ventrikulären Tachykardien und VES. Persistierendes Vorhofflimmern ist vermutlich die am besten untersuchte Form, da es chronisch verläuft und eine hohe Prävalenz aufweist. Es ist mit einem erhöhten Risiko für Herzinsuffizienz assoziiert. Die diagnostische Herausforderung besteht darin, zu klären, ob die linksventrikuläre Schädigung primär durch eine zugrunde liegende Herzerkrankung oder durch die fehlende atriale Kontraktion in Verbindung mit einer schnellen, unregelmässigen ventrikulären Frequenz verursacht wird.
Unabhängig von der Ätiologie zeigt sich eine Verbesserung der linksventrikulären Funktion unter praktisch jeder Form der Therapie. Dies umfasst die medikamentöse Frequenzkontrolle ebenso wie die Rhythmuskontrolle mittels elektrischer Kardioversion, Antiarrhythmika oder Katheterablation. Auch Pacing in Kombination mit einer AV-Knoten-Ablation – nach vorheriger Implantation eines Schrittmachers (VVI) oder eines kardialen Resynchronisationssystems (CRT) – stellt eine wirksame therapeutische Option dar.
Conduction system pacing (LBBAP)
Dies könnte künftig eine Alternative zur «Pace and Ablate»-Strategie darstellen. Zunächst sollte jedoch eine grössere randomisierte kontrollierte Studie (RCT) zur Sicherheit und Wirksamkeit abgewartet werden. Bei CRT-Patientinnen und -Patienten mit Vorhofflimmern (VHFli) ist dieses häufig der Hauptgrund für eine suboptimale biventrikuläre Stimulation. Eine hohe BV-Stimulation ist oft nur durch eine Intensivierung der antiarrhythmischen Medikation oder durch eine gezielte Frequenzkontrolle erreichbar. Rhythmuskontrolle: Die Wiederherstellung des Sinusrhythmus ist ein wichtiger Faktor für die Erholung der linksventrikulären Funktion – vorausgesetzt, der Sinusrhythmus kann langfristig stabil gehalten werden. Der Erfolg einer Ablation ist am grössten, wenn die Patientinnen und Patienten strukturell herzgesund sind und das EKG weder einen Schenkelblock noch Repolarisationsstörungen zeigt.
Nach einem Vorhofremodelling sinkt die Chance auf einen langfristigen Ablationserfolg deutlich. Auch bei Patientinnen und Patienten mit Herzinsuffizienz führt die Rhythmuskontrolle zu einer Reduktion der Mortalität – dies wurde unter anderem in den Studien CASTLE-AF und AATAC-AF gezeigt.
Take Home Message
Die Störung ist potenziell reversibel. Das Krankheitsbild sollte erkannt und adäquat behandelt werden, da es prognostisch bedeutsam ist.
Tachykardien (> 100/Min.), Arrhythmien und Dyssynchronie sollten vermieden werden.
Schrittmacherindikation bei Bradykardie: Wieviel ist zu wenig?
Die Frage, wann eine Herzfrequenz «zu langsam» ist, hängt von verschiedenen Faktoren ab, insbesondere von Symptomen und der individuellen Situation, erläuterte PD Dr. med. David Hürlimann, Klinik Hirslanden Zürich.

Allgemeine Richtwerte für eine zu niedrige Herzfrequenz (Bradykardie)
Ein normaler Ruhepuls liegt bei 60–100 Schlägen pro Minute (BPM), eine Bradykardie wird bei einer Frequenz unter 60 BPM definiert. Eine zu niedrige Herzfrequenz kann insbesondere bei Sportlern oder im Schlaf gefährlich werden. Eine Bradykardie unter 30 BPM ist behandlungsbedürftig, da sie zu Ohnmacht oder Herzstillstand führen kann.
Gemäss den ESC-Leitlinien ist Pacing indiziert bei Patienten im Sinusrhythmus mit permanentem oder paroxysmalem Drittgrad- oder Zweitgrad-AV-Block Typ II, infranodalem 2:1-Block oder hochgradigem AV-Block – unabhängig von Symptomen (Empfehlung I/C).
Pacing sollte in Betracht gezogen werden bei Patienten mit symptomatischem Zweitgrad-AV-Block Typ I oder wenn in der elektrophysiologischen Untersuchung ein intra- oder infra-His-Block festgestellt wird (Empfehlung IIa/C).
Die Empfehlungen der ACC/AHA sind in folgender Abbildung zusammengefasst:
Abb.: Empfehlungen für permanentes Pacing bei chronischer Therapie/Management der Bradykardie wegen Sinusknotendysfunktion (SND)
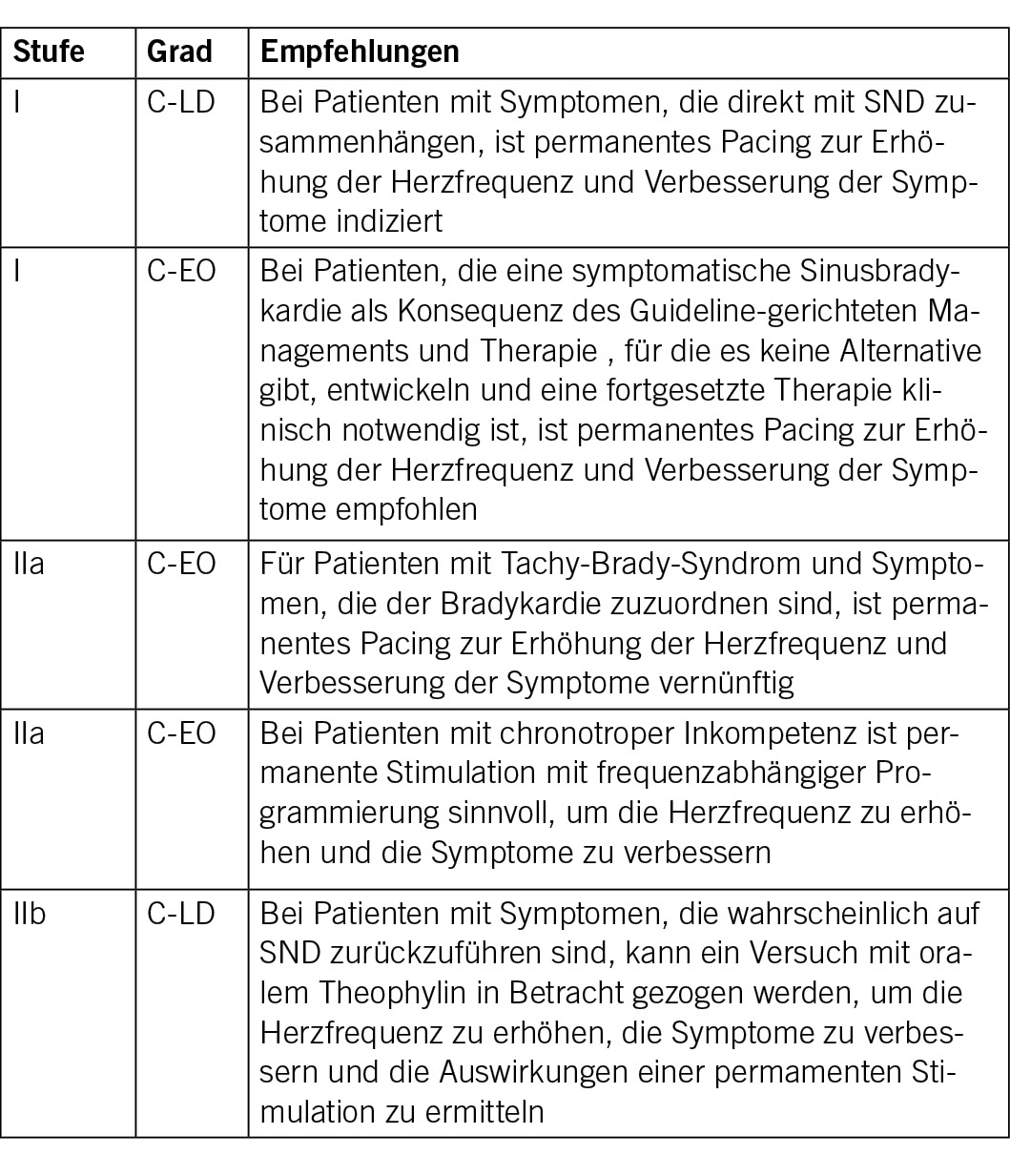
Stimulation bei Sinusknotenerkrankung
Für die Herzschrittmachertherapie bei asymptomatischem Sick-Sinus-Syndrom (SSS) wurde, im Gegensatz zur Stimulation bei AV-Block, nie ein prognostischer Nutzen belegt. Daher kann das SSS nur dann als geeignete Indikation für permanente Stimulation angesehen werden, wenn die durch das SSS verursachte Bradykardie symptomatisch ist. Die Etablierung eines Zusammenhangs zwischen Symptomen und einer Bradyarrhythmie ist ein wesentlicher Schritt bei der Entscheidungsfindung. Bei Patienten mit Synkope und asymptomatischen Pausen > 6S aufgrund eines Sinusarrests, kann Stimulation indiziert sein.
Zusammenfassung
– Die Frage, was zu langsam ist, lässt sich nicht eindeutig beantworten.
– Die Guidelines helfen uns nur beschränkt weiter.
– Eine Symptomkorrelation ist zentral (insbesondere beim Sick Sinus).
– Die Entscheidung muss individuell getroffen werden (Alter, Komorbiditäten, Patientenpräferenz etc.).
Was ist LBBA-Pacing? Was gibt es für Entwicklungen bei den Schrittmachern?

Left Bundle Branch Area Pacing (LBBA-Pacing) ist eine Stimulationstechnik, die das Erregungsleitungssystem des Herzens im Bereich des linken Schenkelblocks stimuliert, um eine physiologische Stimulation mit einem engen QRS-Komplex und einer verbesserten linksventrikulären Aktivierungszeit zu erreichen. Es wird verwendet um möglichst ohne Nebenwirkungen auszukommen. Dabei werden die Kabel aus der rechten Herzkammer durch die Herzgefässwand mit der linken Kammer verbunden, was für einen synchronen Herzschlag sorgt. Diese neue Methode kann einer möglichen Herzinsuffizienz entgegenwirken.
PD Dr. med. Alexander Breitenstein, USZ, präsentierte zudem elektrodenlose Schrittmacher für die Vorhofstimulation, ventrikuläre Stimulation (AVEIR®VR leadless Pacemaker) und die Zweikammerstimulation (AVEIR® DR Dual Chamber Pacemaker System).
Koronarien
Koronare Herzkrankheit (KHK) durch Stress und Sport – ein Paradox?

Das Sportparadox: Sport als Auslöser von Herzerkrankungen und plötzlichem Herztod. Prof. Dr. med. Christian Schmied, HerzGefässZentrum im Park, Zürich, stellte den Fall eines 31-jährigen professionellen Athleten vor, der sich präsentierte, um seine Herz-CT-Ergebnisse zu diskutieren. Der Patient fühlt sich gesund, ist aber gestresst, hat atypische Brustschmerzen, nimmt regulär «Snus», keine anderen Drogen oder reguläre Medikation, NSAR selten, Familienanamnese unverdächtig. Der Referent zeigte die Beziehung zwischen dem Trainingsumfang und dem Gesundheitsrisiko, welches eine U-Form darstellt mit der «optimalen» Bewegungsdosis zwischen keiner Bewegung (höchstes Risiko) und extremer Bewegungshypothese (hohes Risiko). Der grösste Nutzen der Bewegung liegt bei 75 Min/d (9 h/Woche), 4000–5000 kcal/Woche.
Koronare Atherosklerose bei Spitzensportlern
Die Vermutung, dass langfristiges Ausdauertraining zu einer paradoxen Zunahme von Atherosklerose der Herzkranzgefässe führen kann, wurde mit der Master@Heart-Studie bestätigt. Ausdauersportler mit lebenslangem intensivem Training hatten mehr koronare Plaques als fitte und gesunde Personen mit einem ähnlich niedrigen kardiovaskulären Risikoprofil. Emotionaler Stress verstärkte dieses Problem zusätzlich.
Zusammenfassung
Der Referent fasste seine Ausführungen wie folgt zusammen: Regelmässige intensive körperliche Betätigung kann in Verbindung mit anderen Faktoren (insbesondere emotionalem Stress) zu einer chronischen Entzündung führen, die ihrerseits zu koronarer Atherosklerose führt.
Die Unterscheidung zwischen gesundem und belastendem Sport ist schwierig (Selbstreflexion ist entscheidend).
Ist die Koronarsklerose erst einmal etabliert, ist eine Modifizierung /Stabilisierung der Plaque zwingend erforderlich.
Ob regelmässige körperliche Betätigung (und in welcher Intensität) als «natürlicher» Plaque-Stabilisator dient, bleibt umstritten. Eine generelle Bewegungseinschränkung bei KHK wäre jedoch fatal. Verlässliche Ergebnisdaten in diesem Bereich werden dringend benötigt, stellte der Referent abschliessend fest.
Ballon – Stent – beschichtete Stents- beschichtete Ballons – wie weiter?

«Die perkutane koronare Intervention geht zurück auf Prof. Andreas Grüntzig 1977, der die erste perkutane transluminale Koronarangioplastie in Zürich durchführte», sagte Prof. Dr. med. Raban Jeger, Stadtspital Triemli, Zürich. Jacques Puel und Ulrich Sigwart führten 1986 die Bare-Metal Stents ein. Das Problem dieser Intervention ist die In-Stent-Restenose. In der RAVEL-Studie war das Myokardinfarkt-freie Überleben und die Zielgefäss-Vaskularisierung mit einem Sirolimus beschichteten Stent 94.1 % vs. 70.9 % mit einem Standard Stent. In einer gross angelegten, auf individuellen Patientendaten basierenden Studie von Madhavan MV et al (JACC 2020) traten zwischen 1 und 5 Jahren nach der PCI bei allen Stenttypen sehr späte Stent-bezogene Ereignisse mit einer Rate von ~ 2 %/Jahr auf, ohne dass ein Plateau erkennbar war. Die Studienautoren folgern, dass neue Ansätze erforderlich sind, um die langfristigen Ergebnisse nach der PCI zu verbessern.
Die Geschichte der PCI ist durch mehrere technologische Meilensteine geprägt:
1977: Erste Ballonangioplastie (PTCA) durch Andreas Grüntzig
1986: Einführung des ersten metallischen Stents (BMS) durch Ulrich Sigwart
1999: Einführung medikamentenbeschichteter Stents (DES)
2000: Entwicklung bioresorbierbarer Stents (BRS)
2006: Einführung medikamentenbeschichteter Ballons (DCB)
In der AIDA-Studie wurde ein bioresorbierbares Gerüst (Scaffold), das Everolimus freisetzt, mit einem ebenfalls Everolimus-freisetzenden, metallischen Stent verglichen – bei Patienten, die sich einer PCI unterzogen. Das Ergebnis:
→ Kein signifikanter Unterschied bei der Rate des Zielgefässversagens.
→ Allerdings: Das bioresorbierbare Gerüst war mit einer höheren Rate an Gerätethrombosen innerhalb von zwei Jahren verbunden.
Folgen des Misserfolgs von «Absorb»
Der Absorb-Stent war das bisher am besten untersuchte BRS. Die enttäuschenden Ergebnisse aus den ABSORB-Studien führten zu einem erheblichen Rückschlag. Dennoch sind aktuell rund 34 bioresorbierbare Gerüste von 22 Firmen in der Entwicklung.
Gründe für das Scheitern von Absorb waren 1) Schwache mechanische Eigenschaften, 2) Dicke und breite Streben: Dadurch schlechtere Verankerung und grösserer «Fussabdruck», was zu Unterexpansion und Vorsprüngen führen kann, was schliesslich zu einer erhöhten Thrombogenität führt, 3) eine längere Bioresorptionszeit in Kombination mit einem Versagen der Verkapselung der Streben, bevor der Demontage-Prozess beginnt.
Angesichts der Vielfalt der bioresorbierbaren Materialien (auch unter den PLLA) und der unterschiedlichen mechanischen Eigenschaften und Bioresorptionsprofile jedes neuen BRS könnte man einen erheblichen Unterschied in den frühen und späten klinischen Ergebnissen erwarten. Tatsächlich haben Daten aus First-in-Man (FIM) und Zulassungsstudien unterschiedliche klinische Ergebnisse gezeigt. In der Tat stützen frühe klinische Beweise aus FIM-Studien keinen Klasseneffekt. Das Fehlen eines Vergleichskriteriums hindert uns jedoch daran, endgültige Schlussfolgerungen zu ziehen. Weitere klinische Nachweise sollten das Fehlen (oder Vorhandensein) eines Klasseneffekts bestätigen.
Das Freesolve Scaffold stammt aus der BIOMAG-I-FIH-Studie. Es basiert auf dem geprüften Osiro Mission Liefersystem, hat dünne Streben, eine Biolute®-resorbierbare Beschichtung sowie die Biomag®-proprietäre Magnesiumlegierung. Ein neues Tantalum-Marker-Konzept sorgt für bessere Visibilität. Nach 12 Monaten zeigten sich keine definitiven oder wahrscheinlichen Scaffold-Thrombosen, keine kardialen Todesfälle, keine Zielgefäss-Myokardinfarkte und eine 2.6 % Ziel-Läsionsversagensrate.
Medikamentenbeschichtete Ballons bei koronarer Herzkrankheit: Der dritte Bericht der internationalen DCB Consensus Group (Jeger R et al) hebt hervor: DES haben immer noch einige Einschränkungen bei bestimmten klinischen und anatomischen Bedingungen. DCBs sind eine neuartige therapeutische Strategie für die koronare Herzkrankheit. Neben der ISR zeigen neue Daten mögliche Indikationen für die native koronare Herzkrankheit. Zukünftige Forschungen werden sich auf alternative Wirkstoffbeschichtungen und andere mögliche Indikationen konzentrieren.
Zweit-Generations-DES sind heute der Goldstandard in der interventionellen Kardiologie, weisen aber eine kontinuierliche jährliche Eventrate von 2 % auf. Während PLLA-basierte BRS zuvor gescheitert sind, sind neue Mg-basierte BRS in klinischer Erprobung. DCB zeigen bei richtiger Anwendung mindestens ähnlich gute Ergebnisse wie Zweit-Generations-DES. DCB in Kombination mit DES scheinen besser als DES allein zu sein («blended therapy»). Eine Kombination von DCB und BRS wäre eine ideale Kombination («leaving nothing behind»).
«Leaving nothing behind» «No Stents»

Ein Patient wünschte ausdrücklich einen Stent. Doch wie Dr. med. Daniel Weilenmann, St. Gallen, erläuterte, war auch POBA – die «plain old balloon angioplasty», also die klassische Aufdehnung einer Koronararterie ohne Stent – sicher und dauerhaft. Bei einem Stent kann es hingegen zu einer durchflussbegrenzenden Dissektion, einem TIMI-Flow < 3 oder einer akuten Rekoalition kommen. Prädiktoren einer Restenose bei neueren Generationen von DES sind: patientenbezogene Faktoren wie die optimale medikamentöse Therapie, die Wahl eines neuen Generationen-DES, läsionsbezogene Risikofaktoren sowie implantationsbezogene Risikofaktoren, die auch vom Operateur beeinflusst werden können. Für kleine Gefässe gilt: DCB ist DES überlegen. Auch in der SYNTAX-II-Studie bei Patienten mit Multivessel-Erkrankung (MVD) zeigte sich, dass weniger eingesetzte DES mit einem besseren klinischen Outcome assoziiert waren.
Schlussfolgerungen
Eine Behandlung ohne DES ist sinnvoll, wenn das angiographische Resultat zufriedenstellend ist. Die Evidenzlage für DCBs bei In-Stent-Thrombose und bei kleinen Gefässen ist eindeutig. Zudem gibt es eine zunehmende Evidenz für den Einsatz von DCBs in allen PCI-Bereichen, einschliesslich chronisch totaler Okklusion (CTO) und beim akuten Koronarsyndrom (ACS). DCBs gelten als effizient und sicher. Weitere Studiendaten sind in Vorbereitung. Adaptieren Sie frühzeitig, um Ihre Patienten bestmöglich zu behandeln – und nicht bald als altmodisch zu gelten.
Neues bei GLP-1 und GLP-1/GIP-Rezeptoragonisten
Komorbiditäten bei Typ-2-Diabetes

In der Schweiz leiden 6.4 % der Bevölkerung an Typ-2-Diabetes (T2D). Davon sind 60–90 % adipös (11 % in der Allgemeinbevölkerung). Weitere Komorbitäten sind: 20–50 % der T2D-Patienten haben eine kardiovaskuläre Erkrankung, 25 % einen Insulinmangel, 25 % Herzinsuffizienz, 25 % eine chronische Niereninsuffizienz, 50–70 % haben eine mit metabolischer Dysfunktion assoziierte Fettleber, 30–40% eine mit metabolischer Dysfunktion assoziierte Steato-Hepatitis.
Prof. Dr. med. Roger Lehmann vom Universitätsspital Zürich erläuterte, dass makrovaskuläre Erkrankungen bei T2D mit steigendem HbA1c-Wert assoziiert sind: Bereits ab einem HbA1c von > 5.5 % steigt das Risiko für koronare Herzkrankheit oder Schlaganfall um 50–55 %.
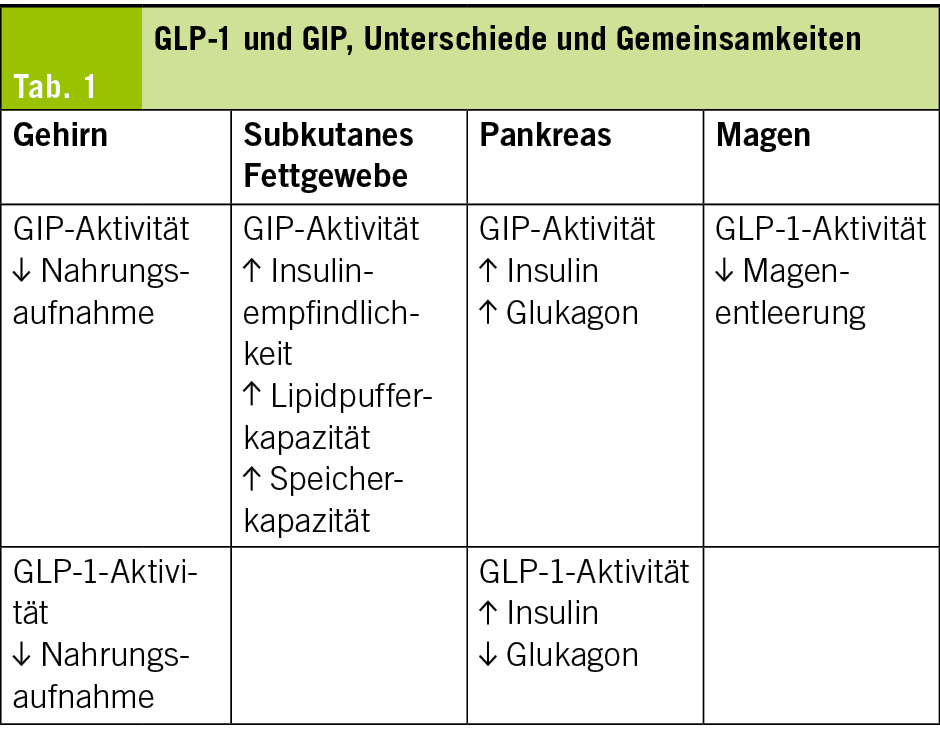
GLP-1-Rezeptoragonisten (GLP-1 RA) führen zu einer deutlichen Senkung des HbA1c. Die grösste Reduktion wird durch GLP-1RA/GIP-RA-Kombinationen erzielt, wie im SURPASS-2-Studienvergleich (Tirzepatid [Mounjaro®] vs. Semaglutid) gezeigt wurde: Alle drei Dosierungen von Mounjaro® waren wirksamer als Semaglutid 1 mg (Tab. 1).
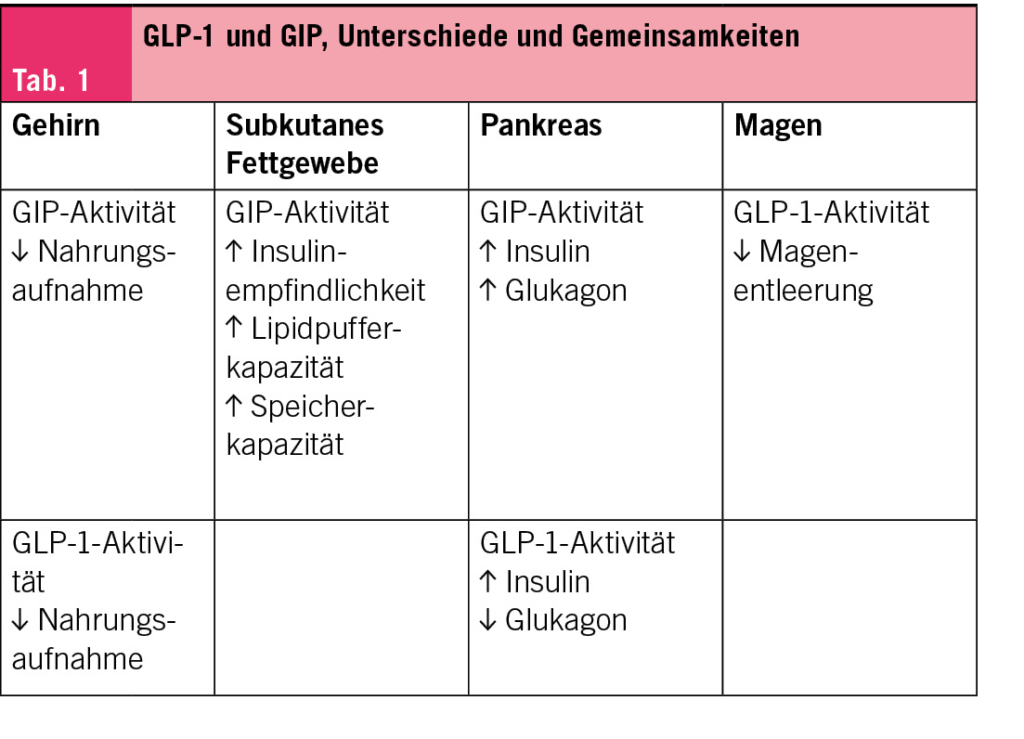
Komorbidität bei Adipositas
Adipositas ist eng mit einer Vielzahl schwerwiegender Erkrankungen verknüpft. Dazu zählen Typ-2-Diabetes (20–25 %), Schlafapnoe (40–45 %), Hypertonie (50–55 %), metabolisch-assoziierte Fettlebererkrankung (MAFLD) (50–70 %), Metabolische Dysfunktion-assoziierte Steatohepatitis (MASH) (30–35 %) und Dyslipidämien (65–70 %).
Gewicht- und Glukosemanagement
GLP-1 RA
Wirksamkeit: Höhere Dosen verbessern den Gewichtsverlust, steigern aber auch Nebenwirkungen. Dies gilt nicht für die Glukosesenkung. Die beste Wirksamkeit und kardiorenaler Schutz wird mit einer hohen Dosis Semaglutid erzielt.
GLP-1/GIP RA
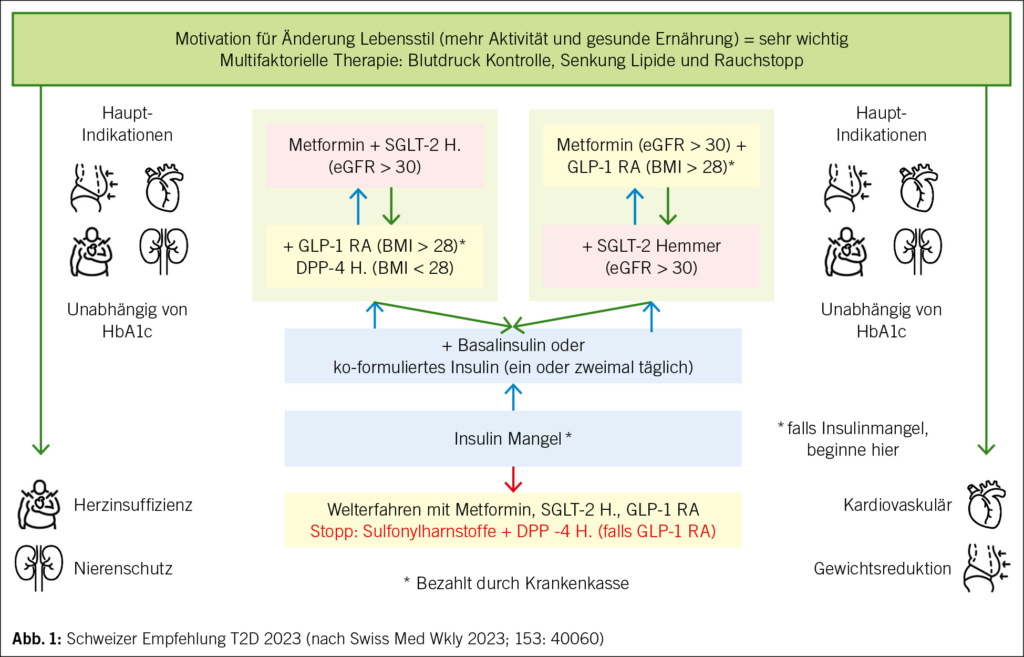
Tirzetrapid ist eine neue Substanz mit hoher Wirksamkeit. Die kardiovaskuläre Endpunktstudie läuft. Tirzetrapid ist ein dualer Agonist und hat womöglich weniger Nebenwirkungen als hoch dosierte GLP-1RA. 2,4 mg Semaglutid (Wegovy®) haben das Gewicht von 107.2 kg auf 89.2 kg gesenkt. Der Gewichtsverlust durch Semaglutid betrug 18 kg, durch den Wechsel zu Placebo 6 kg und durch Tirzetrapid 5–15 mg 24 kg. Die Lücke zwischen bariatrischer Chirurgie und medikamentöser Therapie schliesst sich (Abb. 1).
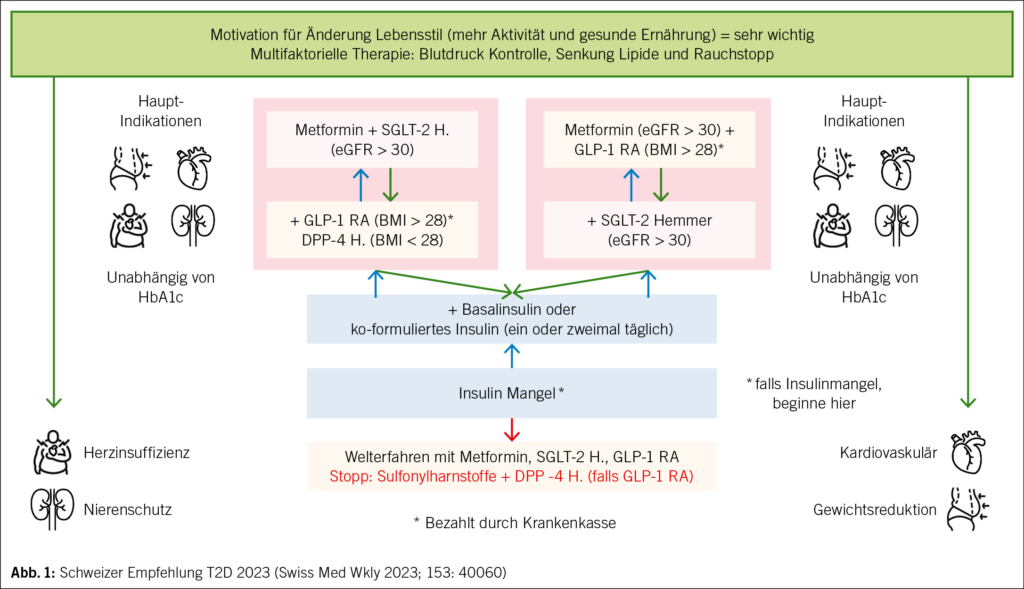
Aktuelle Studien
Die aktuelle Studienlage bestätigt den breiten Nutzen von GLP-1- und GLP-1/GIP-Agonisten über die glykämische Kontrolle hinaus.
Im FLOW-Trial (Perkovic V et al., NEJM 2024) konnte Semaglutid 1.0 mg subkutan eine signifikante Reduktion des primären Nierenendpunktes um 24 % erreichen. Zusätzlich zeigte sich in einer Subgruppenanalyse eine 27 %ige Senkung der zusammengesetzten Herzinsuffizienz-Ereignisse, einschliesslich kardiovaskulärem Tod. Diese Effekte traten unabhängig von einer bestehenden Herzinsuffizienz auf.
Auch bei metabolisch-assoziierten Lebererkrankungen gibt es Fortschritte: Die ESSENCE-Trial (Mitteilung Novo Nordisk) untersuchte 1200 Patienten mit MAFLD und/oder MASH. Nach 72 Wochen zeigten 37.0 % der Patienten unter Semaglutid 2.4 mg eine Verbesserung der Leberfibrose ohne Verschlechterung der Entzündung, im Vergleich zu 22.5 % unter Placebo. Zudem verschwand bei 62.9 % der Patienten unter Semaglutid MASH, ohne dass sich die Fibrose verschlechterte – ein klarer Vorteil gegenüber 34.1 % unter Placebo.
Tirzepatid überzeugte ebenfalls durch seine Wirksamkeit: In Studien führte der duale Agonist bei einer beachtlichen Anzahl von Patienten zum Verschwinden von MASH. Auch der neuere Wirkstoff Retatrutid zeigte vielversprechende Resultate, indem der hepatische Fettgehalt bei behandelten Patienten auf unter fünf Prozent gesenkt werden konnte (Synergy-MASH Trial und Phase-2-Obesity Trial).
Die SELECT-Studie (Linkoff AM et al., NEJM 2023) untersuchte 17 604 Patienten mit bestehender kardiovaskulärer Erkrankung, einem BMI ≥ 27 und ohne bekannten Diabetes mellitus. Über einen Zeitraum von 40 Monaten führte die Therapie mit Semaglutid zu einer 20 %igen Reduktion schwerwiegender kardiovaskulärer Ereignisse (MACE), mit einer absoluten Risikoreduktion von 1.5 % und einer Number Needed to Treat (NNT) von 67.
Zusätzlich unterstützt die Real-World-Evidenz den Einsatz von Kombinationstherapien. Die Kombination von GLP-1 RA mit einem SGLT2-Hemmer senkte das Risiko für 3-Punkte-MACE um etwa 30 % im Vergleich zu einer GLP-1-Monotherapie (NNT 30). Im Vergleich zur SGLT2-Hemmer-Monotherapie zeigte sich unter der Kombinationstherapie ebenfalls eine 29 %ige Risikoreduktion (NNT 32).
Dauer und Strategien der Therapie
Die Anwendung von GLP-1- und GLP-1/GIP-Agonisten sollte grundsätzlich kontinuierlich erfolgen, wobei eine individuelle Dosisanpassung wichtig ist, um den erreichten Gewichtsverlust langfristig zu stabilisieren. Alternativ sind auch intermittierende Ansätze – etwa nach dem Prinzip «Start–Stopp–erneuter Start» – möglich. In bestimmten Fällen kann auch eine einmalige Therapie über ein bis zwei Jahre erwogen werden, vorausgesetzt, sie wird von konsequenten Lebensstilmassnahmen begleitet.
Nutzen-Risiko-Abwägung
Die Vorteile der Therapie sind überzeugend: Ein umfassender kardiorenaler und hepatischer Schutz, eine Reduktion der Mortalität sowie Verbesserungen bei Apoplexierisiko, Blutdruck und Lipidprofil wurden nachgewiesen. Gastrointestinale Nebenwirkungen sind zwar häufig, bleiben aber in der Regel mild und ungefährlich. In Bezug auf das Kosten-Nutzen-Verhältnis sind SGLT2-Hemmer aktuell klar positiv bewertet. Bei GLP-1-Rezeptoragonisten ist die Einschätzung derzeit neutral, könnte sich jedoch mit sinkenden Kosten eindeutig ins Positive verschieben.
Lipide /Hormone/Aging
Primärprophylaxe Dyslipidämie

Zu Beginn präsentierte Prof. Dr. med. Jean-Paul Schmid, Gais, den Checkup eines gesunden, beschwerdefreien 35-jährigen Probanden ohne Medikation, dessen Cholesterinwert 6.3 mmol/l, Triglyceride 1.4mmol/l, HDL-Cholesterin 1.0mmol/l, LDL-Cholesterin 3.8 mmol/ö und Chol/HDL-Quotient 5.1 betrugen.
Sein BMI war 24.5kg/m2. Er wies eine positive Familienanamnese auf (Vater mit MI im Alter von 58 Jahren).
Risikoabschätzung mit dem AGLA-Rechner
Der AGLA-Rechner ist nur anwendbar bei scheinbar gesunden Personen im Alter von 20–69 Jahren, die nicht an einem Diabetes leiden.
Mit diesem Rechner ergab sich für den oben beschriebenen Patienten ein niedriges bis moderates Risiko von 0.9 %. Gemäss den ESC Guidelines zur kardiovaskulären Risikoprävention von 2021 wird ein Rauchstopp, Lebensstil-Empfehlungen und bei Alter 50–69 Jahre ein systolischer Blutdruck < 140 bis 130 mmHg, sofern toleriert, empfohlen (Klasse I) und ein LDL-Cholesterinwert < 2.6 mmol/l (Klasse IIa). Bei Alter ≥ 70 Jahre ebenfalls SBP < 140 bis 130mmHg und LDL-C < 2.6 mmol/l (Klasse IIb).
Der AGLA-Rechner ermittelt das Risiko, innert der nächsten 10 Jahre ein kardiovaskuläres Ereignis zu erfahren. Dieses Risiko wird bei jungen Probanden konsistent unterschätzt. Es wird deshalb die Ermittlung des lebenslangen Risikos empfohlen. Dieses wird beispielsweise mit dem LIFE-CVD2 Modell ermittelt, welches den Behandlungsnutzen abschätzt. Im vorliegenden Fall wurde keine Therapie empfohlen. Das lebenslange Risiko beträgt 18.9 %, keine Therapie, 0.0 % Risikoreduktion. Bei einer Therapie mit 2mg Rosuvastatin ergibt sich eine Riskoreduktion um 6.4 % und eine lebenslange NNT von 16, mit zusätzlich mediterraner Diät Risikoreduktion 9.6 % und lebenslange NNT von 10. Die gewonnen Lebensjahre bei einer Lebensewartung von 87 Jahren beträgt 2.8 Jahre.
Ein weiteres Patientenbeispiel betrifft eine 78-jährige Frau, TAVI, nachgewiesene Koronarsklerose Total Cholesterin 8.8 mmol/l, Triglyceride 1.3 mmol/l, HDL-C 0.9mol/l, LDL-C 4.4 mmol/l, Chol/HDL-C 6.6. Kardiovaskuläre Risikofaktoren, BMI23.8kg/m2 , behandelte Hypertonie (BD 135/85mmHg). Für die Berechnung des Risikos wurde der ESC SCORE2 OP-Algorithmus verwendet (anwendbar ab 70 Jahren). Das errechnetes Risiko betrug 14.8 %. Der Blutdruck sollte < 140 bis 130 mmHg (Klasse I) und das LDL-Cholesterin < 2.6 mmol/l betragen (Klasse IIb).
Präventionsziele gelten für alle
Sie betreffen sowohl gesunde Personen, bei denen eine Abschätzung des 10-Jahres-Risikos für kardiovaskuläre Erkrankungen vorgenommen werden sollte, als auch Patienten mit einem bereits etablierten kardiovaskulären Risiko, bei denen das residuelle Risiko im Vordergrund steht.
Besonderes Augenmerk gilt Personen mit spezifischen Risikokonditionen wie Diabetes mellitus, chronischer Nierenerkrankung (CKD) oder familiärer Hypercholesterinämie.
Die kardiovaskuläre Risikoschätzung sollte Grundlage einer informierten Diskussion sein – über das lebenslange Risiko für Herz-Kreislauf-Erkrankungen sowie über die individuellen Behandlungsvorteile. Dabei müssen persönliche Bedürfnisse und Präferenzen berücksichtigt werden, ebenso wie Faktoren wie Alter, Begleiterkrankungen, Gebrechlichkeit und Polypharmazie.
Lipidprobleme aus dem Alltag – ein Quiz

Frau Prof. Dr. med. Isabella Sudano, Kardiologie USZ präsentierte die Fallvignette einer 1986 geborenen Frau mit positiver Familienanamnese (Mutter (68) mit progredienter koronarer Herzkrankheit (ED mit ca. 54 Jahren), RF Hypertonie und Hypercholesterinämie. Der Vater (78) leidet an generalisierter Arteriosklerose, Aorta-Aneurisma infrarenal, koronarer Herzkrankheit (ED mit 57 Jahren). Seine Risikofaktoren waren Hypertonie und Hypercholesterinämie, Tabakkonsum, Diabetes und Hypercholesterinämie. Persönliche Anamnese Grösse 158, Gewicht 54, BMI 19 kg/m2, Blutdruck 116/73 mmHg, HF 81/Min.
Geschätztes kv Risiko. Alter 39, LDL-C 4.5 mmol/l, HDL-C 2.15 mmol/l, TG 1.06 mmol/lSBD 116 mmHg, Raucher ja. Für Patienten mit Diabetes mellitus Typ 2 ohne ASCVD und ohne Zielorganschäden wird der SCORE2 Diabetes-Rechner empfohlen. HDL 2.15 liegt ausserhalb der für die Berechnung zulässigen Werte , es wurde auf das Maximum 1.9 gesetzt. Das geschätzte Risiko betrug 0.6 %. (niedriges bis moderates Risiko). LIFE-CVD2 model: kein Interventionsziel, kein Statin, kein Zielblutdruck derzeitiges Risiko 9.5 %, Reduktion mit Behandlung 0 %. Steigerung der Schrittzahl pro Tag um 2000 Schritte, kein Statin, kein Blutdruck-Behandlungsziel. Derzeitiges Risiko 9.5 %, Reduktion durch Behandlung 1.6 %, Lebenslange NNT 61 Behandlung +2000 Schritte, 20 mg Atorvastatin.
Risikoreduktion 3.5 %, lebenslange NNT 28. Die Referentin zeigte eindrücklich, welchen Einfluss eine frühzeitig begonnene Statintherapie bereits im Kindesalter auf das ereignisfreie Überleben bei Patienten mit heterozygoter familiärer Hypercholesterinämie hat. Im Vergleich dazu war das ereignisfreie Überleben der Elterngeneration, die noch keinen Zugang zu dieser Therapie hatte, um mehr als 40 % kürzer.
Testosteron und DHEA: Welche Substitution macht Sinn bei Männern und Frauen?
Der alternde Mann: Erwartungen und Realität der Testosterontherapie

Lange Zeit galt Testosteron als Hoffnungsträger, um den alternden Mann zu «verjüngen» und seine Gesundheit zu verbessern. Doch wie Prof. Dr. med. Bernd Schultes (St. Gallen) feststellte, haben neue Studien diese Hoffnungen weitgehend entkräftet.
Für die Labordiagnostik werden heute folgende Empfehlungen gegeben: Eine Mehrfachbestimmung des Gesamttestosterons, mindestens zweimalig, sollte erfolgen. Die Blutentnahme sollte morgens zwischen 7 und 10 Uhr stattfinden, da zu dieser Zeit die höchsten Werte gemessen werden können. Zusätzlich wird die Messung des Sexualhormon-bindenden Globulins (SHBG) sowie die Berechnung des freien Testosterons empfohlen. Bei Verdacht auf sekundären Hypogonadismus sollte eine Differenzialdiagnostik unter Einschluss von LH, Prolaktin und Ferritin erfolgen, ergänzt durch eine weiterführende endokrine Abklärung. Die Indikation für eine MRI sollte dabei eher zurückhaltend gestellt werden.
Testosteronspiegel sind alters- und BMI-abhängig: Mit zunehmendem Alter und steigendem Körpergewicht sinkt das freie Testosteron, während es nach einem Magenbypass wieder ansteigt. Studien zeigten, dass bei adipösen Männern die Gabe von Aromatasehemmern den LH- und Testosteronspiegel steigen lässt, Estradiol hingegen abfällt. Jedoch hatte diese Intervention keinen nachweisbaren Effekt auf metabolische Parameter, körperliche Leistungsfähigkeit oder Stimmung.
Wirkung einer Testosteronbehandlung bei älteren Männern
Eine Zusammenfassung von sieben Placebo-kontrollierten Studien bei Männern über 65 Jahre mit Symptomen und einem Gesamttestosteronwert unter 9 nmol/l zeigte, dass die sexuelle Funktion durch eine Testosteronsubstitution deutlich verbessert werden konnte. Die körperliche Leistungsfähigkeit wurde subjektiv ebenfalls als besser empfunden, jedoch zeigte sich keine signifikante Verbesserung der Vitalität.
Metabolische Effekte
In zahlreichen kontrollierten Studien in verschiedenen Populationen mit niedrigen Testosteronwerten und Symptomen konnte eine eindeutige Verbesserung der Körperzusammensetzung festgestellt werden: Der Fettanteil nahm ab, während die Muskelmasse zunahm. Das Körpergewicht reduzierte sich moderat. Ergebnisse zum Glukosestoffwechsel waren gemischt, reichten von neutralen Effekten bis hin zu leichten Verbesserungen, auch bei Typ-2-Diabetes-Patienten. Die Lipidprofile zeigten tendenziell leichte Verbesserungen. Weniger erfreulich sind Hinweise aus einer kleinen Studie (n = 209) im New England Journal of Medicine (Basaria et al., 2010), die bei Männern über 65 Jahre mit eingeschränkter Mobilität eine Häufung kardiovaskulärer Ereignisse unter Testosteronsubstitution zeigte, was zum vorzeitigen Studienabbruch führte. Eine neuere Untersuchung zur kardiovaskulären Sicherheit ergab eine nicht signifikante Hazard Ratio von 0.96, wobei die Nichtunterlegenheit (p < 0,001) nachgewiesen wurde.
Indikation zur Testosteronsubstitution
Ein allgemeiner Konsens besteht darin, dass eine Testosterontherapie bei einem Gesamttestosteronwert unter 8 nmol/l (230 ng/dl) und entsprechender Symptomatik indiziert ist. Liegt der Wert über 12 nmol/l, besteht keine Indikation zur Therapie. Bei Werten zwischen 8 und 12 nmol/l sollte das freie Testosteron berechnet werden. Liegt dieser Wert unter 225 pmol/l (65 pg/ml), kann eine Therapie erwogen werden.
Risiken und Kontraindikationen der Testosterontherapie
Die Inzidenz von Prostatakarzinomen wird unter Testosteronsubstitution nicht erhöht. Allerdings kann der Hämatokrit ansteigen, ebenso können sich eine benigne Prostatahyperplasie (BPH) oder eine Schlafapnoe verschlechtern.
Absolute Kontraindikationen für eine Testosterontherapie sind ein bestehendes Prostatakarzinom, ein PSA-Wert über 4 ng/ml, Mammakarzinom, bestehender Kinderwunsch, ein Hämatokrit über 50 % sowie schwere Symptome einer BPH oder einer unbehandelten Schlafapnoe (letztere gelten als relative Kontraindikationen).
Testosteronbehandlung und Frakturrisiko
Eine aktuelle Publikation im New England Journal of Medicine (Snyder PJ et al., 2024) untersuchte den Zusammenhang zwischen Testosterontherapie und Frakturrisiko bei Männern mit Hypogonadismus. Entgegen der Erwartungen führte die Testosteronsubstitution nicht zu einer Reduktion des Frakturrisikos, sondern war mit einem signifikant erhöhten Risiko verbunden.
Dehydroepiandrosteron (DHEA) bei Frauen
Die Anwendung von DHEA bei Frauen mit primärer oder sekundärer Nebenniereninsuffizienz oder Anorexia nervosa zeigte in Studien nur geringe Vorteile hinsichtlich Lebensqualität und Stimmung. Positive Effekte auf Angstzustände oder sexuelle Funktionen konnten nicht eindeutig belegt werden. Bei gesunden Frauen wurden keine konsistent positiven Effekte auf Wechseljahrsbeschwerden, sexuelle Funktionen, kognitive Leistungen oder das allgemeine Wohlbefinden nachgewiesen.
Eine Ausnahme bildet die lokale Anwendung von DHEA, die bei vulvovaginaler Atrophie signifikante Vorteile zeigte. Die systemische Verabreichung von DHEA zur Verbesserung der Ovulationsinduktion bei Frauen mit reduzierter Ovarialreserve wird hingegen nicht empfohlen. Zu den Risiken einer hochdosierten oder langfristigen DHEA-Verabreichung zählen androgene und östrogene Nebenwirkungen, die insbesondere bei längerer Anwendung relevant werden.
Testosterontherapie bei Frauen
Ein globaler Konsensus (Davis SR et al., JCEM 2019) stellte fest, dass es keine einheitliche Definition für einen Androgenmangel bei Frauen gibt, da spezifische Cutoff-Werte für DHEAS oder Testosteron fehlen.
In der Praxis wird bei Frauen eher die Gabe von Testosteron als von DHEA bevorzugt. Positive Effekte wurden insbesondere hinsichtlich der sexuellen Funktion, vor allem der Libido, sowie bei urogenitalen Symptomen beobachtet. Selbst bei Patientinnen mit primärer oder sekundärer Nebenniereninsuffizienz wird eine Testosterontherapie jedoch nicht generell empfohlen. Zu beachten sind mögliche Nebenwirkungen wie Hirsutismus und Akne. Langfristige Sicherheitsdaten zur Testosterontherapie bei Frauen liegen derzeit nicht vor.
Prof. Dr. Dr. h.c. Walter F. Riesen
riesen@medinfo-verlag.ch