Lange Zeit wurde angenommen, dass die Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) eine Erkrankung des Kindes- und Jugendalters darstellt und mit zunehmendem Alter ausheilt. Mittlerweile geht man jedoch davon aus, dass die Symptomatik bei bis zu 50-80 % der betroffenen Kinder bis ins Erwachsenenalter persistieren kann (2, 4, 7). Dabei weisen die verschiedenen Symptome jedoch entwicklungsabhängige Veränderungen auf und können somit je nach Alter in unterschiedlichen Ausprägungen vorliegen (19). In diesem Artikel werden die diagnostischen Kriterien, differentialdiagnostische Überlegungen und therapeutische Möglichkeiten dargelegt.
Erwachsene mit einer ADHS leiden häufig weniger an einer sichtbaren Hyperaktivität, sondern eher an einer inneren Unruhe bei weiterhin verminderter Aufmerksamkeitsleistung und Beeinträchtigungen der Affektregulation und Impulskontrolle (14). Eine Metaanalyse unter Berücksichtigung der ehemaligen DSM-IV- Kriterien geht von einer weltweiten Prävalenz der adulten ADHS von etwa 2,5% aus (21). Anderen Studien zufolge wird in Deutschland sogar von einer Prävalenz von 4,7% ausgegangen (5).
Dabei stellt das Vorliegen einer ADHS einen Risikofaktor für weitere psychiatrische Erkrankungen dar. Zu den häufigsten psychiatrischen Komorbiditäten zählen Depressionen, Suchterkrankungen, Angst- und Persönlichkeitsstörungen (2, 9).
Diagnostik
Bei der Diagnostik einer ADHS spielt besonders die Eigen- und Fremdanamnese eine entscheidende Rolle. Es liegen zur Diagnosestellung mit
- ICD-10
- DSM-5
- Wender-Utah-Kriterien
drei verschiedene Diagnosesysteme vor, die in den deutschen Leitlinien gleichwertig bei der Diagnosestellung berücksichtigt werden (2). Dabei sind die Wender-Utah-Kriterien speziell für das Erwachsenenalter konzipiert worden (24).
Grundsätzlich setzt die Diagnosestellung voraus, dass die Symptomatik bereits im Kindes- oder zumindest im Jugendalter vorgelegen hat. Dabei fordert die ICD-10 insgesamt strengere Kriterien für die Diagnosestellung der F90.0 (Einfache Aktivitäts- und Aufmerksamkeitsstörung). So müssen in der ICD-10 alle Symptome − Unaufmerksamkeit, Hyperaktivität und Impulsivität − erfüllt sein und das Störungsbild muss bereits vor dem 7. Lebensjahr vorgelegen haben. Wenn, wie häufiger bei Mädchen der Fall, das Symptom der Unaufmerksamkeit deutlich überwiegt und keine Hyperaktivität auftritt, kann lediglich eine F98.8 (sonstige näher bezeichnete Verhaltens- und emotionale Störungen mit Beginn in der Kindheit und Jugend) kodiert werden. Auch muss ausgeschlossen werden, dass eine tiefgreifende Entwicklungsstörung (F84), eine manische (F30) oder depressive Episode (F32) oder eine Angststörung (F41) vorliegen (6).
Das DSM-5 hingegen unterscheidet zwischen verschiedenen Erscheinungsformen der Erkrankung. So lassen sich nach DSM-5 ein vorwiegend unaufmerksamer Typ, ein vorwiegend hyperaktiv-impulsiver Typ sowie ein kombinierter Typ der AD(H)S diagnostizieren. Im DSM-5 wurde im Vergleich zum DSM-IV das Alterskriterium modifiziert, indem die Altersgrenze der Erstmanifestation auf 12 Jahre heraufgesetzt wurde. Auch eine komorbid auftretende, tiefgreifende Entwicklungsstörung führt nicht zum Diagnoseausschluss (1). Beide Klassifikationssysteme setzten jedoch voraus, dass die Kernsymptomatik in verschiedenen Lebensbereichen auftritt.
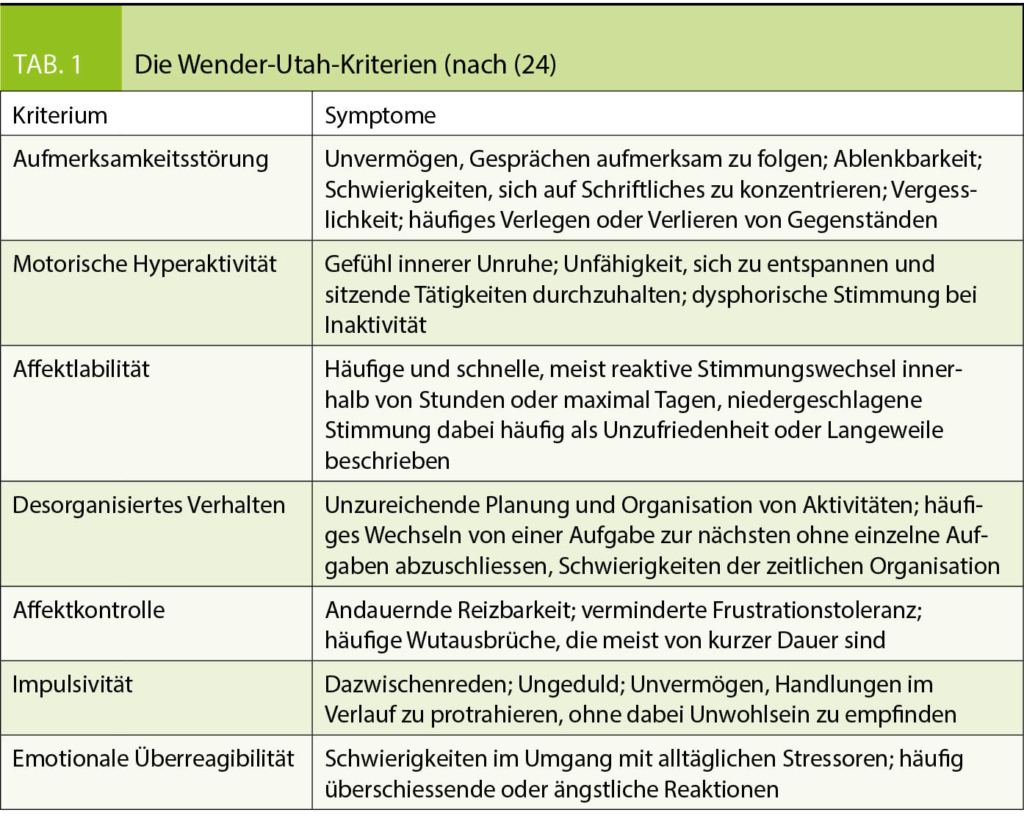
Die Wender-Utah-Kriterien wurden speziell für das Erwachsenenalter konzipiert und berücksichtigen den entwicklungsbedingten Symptomwandel der Betroffenen (24). Dabei werden zur Diagnosestellung neben Aufmerksamkeitsstörung und Hyperaktivität zwei weitere Charakteristika verlangt (Tab. 1).
Da die ADHS-Diagnose einen Symptombeginn im Kindes- bzw. Jugendalter voraussetzt, kommt neben der ausführlichen Eigenanamnese auch einer Fremdanamnese eine besondere Bedeutung zu. Zunächst sollten dabei mögliche Schwangerschafts- oder Geburtskomplikationen eruiert werden, da diese häufig mit einer im Verlauf auftretenden ADHS-Symptomatik assoziiert sind (14). Da bei den Betroffenen oft mit Beginn des Schulbesuchs u.a. durch die nun steigenden äusseren Anforderungen und Regeln die Symptomatik zunehmend zu Tage tritt, ist es auch häufig ratsam, (Grund-)schulzeugnisse zur Einschätzung hinzuzuziehen.
Zusätzlich zur klinischen Diagnostik in Form einer ausführlichen Anamnese gibt es noch verschiedene evaluierte Fragebögen und strukturierte Interviews. Ausserdem kann die Durchführung einer neuropsychologischen Testung sinnvoll sein (2).
Grundsätzlich stellt die ADHS allerdings nach wie vor eine klinische Diagnose dar und die genannten Fragebögen und strukturierten Interviews sowie die neuropsychologische Testung dienen lediglich als ergänzende Verfahren, die auf eine Diagnose hinweisen können. Eine alleine auf diesen Verfahren basierende Diagnosestellung ist nicht zulässig (7).
Differentialdiagnostik
Wie bei allen psychischen Erkrankungen ist auch bei der Diagnostik der ADHS die Durchführung einer ausführlichen somatischen und auch psychiatrischen Differentialdiagnostik obligat (2). So sollten u.a. besonders eine Hyper- oder Hypothyreose, Vigilanzstörungen oder andere neurologische und auch kardiovaskuläre Erkrankungen ausgeschlossen werden. Dazu kann eine Labordiagnostik sowie eine MRT-, EKG- und EEG-Untersuchung durchgeführt werden.
Auch kommt der Abgrenzung der Symptomatik von anderen psychiatrischen Erkrankungsbildern eine grosse Bedeutung zu. So können beispielsweise Konzentrationsstörungen auch im Rahmen affektiver Erkrankungen wie Depressionen auftreten. Dabei weisen diese jedoch typischerweise einen phasenhaften Verlauf auf, wohingegen die Symptomatik der ADHS chronisch persistiert. Auch die Abgrenzung von Borderline-Persönlichkeitsstörungen kann aufgrund teilweise überlappender Symptome schwierig sein. Nicht selten kommt es auch zu einem komorbiden Auftreten der genannten Erkrankungen (2, 9). In der Abb.1 ist ein differenzialtherapeutischer Entscheidungsbaum zur Behandlung von Erwachsenen mit ADHS vorgeschlagen.
Therapie
Die Diagnose einer ADHS impliziert nicht zwangsläufig eine Therapienotwendigkeit. Entscheidend dabei ist die jeweilige Symptomausprägung und die daraus resultierenden funktionellen Einschränkungen sowie die Präferenzen des Patienten und der Angehörigen (2, 12).
Dabei gelten Stimulanzien nach Ausschluss von Kontraindikationen als Mittel der ersten Wahl (7, 8). Vor Beginn einer medikamentösen Therapie sowie im Verlauf sollte eine ausführliche kardiovaskuläre Abklärung, eine neurologische sowie in regelmässigen Abständen eine Laboruntersuchung erfolgen.
Dabei gibt es in Deutschland und der Schweiz mittlerweile verschiedene Präparate, die für die Behandlung der ADHS im Erwachsenenalter zugelassen sind.
Methylphenidat
Die meisten Erfahrungswerte bezüglich der Behandlung einer adulten ADHS liegen innerhalb der Gruppe der Psychostimulanzien für Methylphenidat vor. Seine Wirkung entfaltet Methylphenidat über eine Wiederaufnahmehemmung von Dopamin (DA) und Noradrenalin (NA), die zu einer Erhöhung der intrasynaptischen DA- und NA-Konzentration führt (3, 23). In Deutschland sind für die Behandlung Erwachsener die retardierten Präparate Medikinet adult® und Ritalin adult® zugelassen (2). Die Präparate haben eine Wirkdauer von ca. 8-10 h. Vorteile der Retardpräparate sind eine gleichmässigere Wirkstofffreisetzung und dadurch verminderte Rebound-Phänomene sowie eine Förderung der Compliance durch eine üblicherweise nur ein- bis zweimal tägliche Einnahme. In der Regel wird mit einer Einnahme von 5-10 mg täglich begonnen und die Dosis wöchentlich bedarfsangemessen um 10 mg bis auf eine Maximaldosis von 1mg/kgKG bzw. 80 mg/d gesteigert (3). In der Schweiz sind Concerta®, Methylphenidat Mepha Depotabs® und Methylphenidat Sandoz® Ret Tabl für die Behandlung von einer seit dem Kindesalter fortbestehenden ADHS bei Patienten im Alter von 6 bis 65 Jahre zugelassen und Medikinet®, Methylphenidat-Mepha LA Depocaps® sowie Ritalin® für Patienten im Alter von 6 bis 18 Jahre.
Lisdexamfetamin
Lisdexamfetamin ist als Elvanse adult® seit Februar 2019 auch zur Behandlung Erwachsener zugelassen. Dabei stellt Lisdexamfetamin eine inaktive Vorstufe von D-Amphetamin dar, wodurch das Missbrauchs- und Abhängigkeitspotential verringert werden soll. Lisdexamfetamin wird nach Aufnahme über den Intestinaltrakt vorwiegend in Erythrozyten hydrolysiert und dabei unter Freisetzung von Amphetamin und Lysin aktiviert. Das Präparat entfaltet seine Wirkung über eine Blockade von NA- und DA-Transportern und eine zusätzliche Entleerung präsynaptischer Vesikel und bewirkt somit ebenfalls eine Erhöhung der intrasynaptischen NA- und DA-Konzentration.
Die Initialdosis beträgt in der Regel bei Erwachsenen 30 mg pro Tag und kann in wöchentlichen Abständen je nach individuellen Erfordernissen um 20 mg auf eine Höchstdosis von 70 mg gesteigert werden (3). In der Schweiz wird die Substanz unter dem Namen Elvanse® angeboten mit der Indikation einer Behandlung einer seit dem Kindesalter fortbestehenden ADHS bei Kindern ab 6 Jahren, Jugendlichen und Erwachsenen bis 55 Jahre im Rahmen einer therapeutischen Gesamtstrategie, wenn das Ansprechen auf eine zuvor erhaltene Behandlung mit Methylphenidat als klinisch unzureichend angesehen wird.
Metaanalysen gehen von einer weitgehend vergleichbaren Wirksamkeit von Methylphenidat und Lisdexamfetamin aus (15, 16).
Häufige Nebenwirkungen von Stimulanzien wie Methylphenidat und Lisdexamfetamin sind Kopfschmerzen, Schwindel, Schlafstörungen, Nervosität, Appetitverlust und Magenbeschwerden. Absolute Kontraindikationen stellen eine Schizophrenie, Hyperthyreoidismus, Angina pectoris oder kardiale Arrhythmien und ein Glaukom dar (2, 12).
Atomoxetin
Der Noradrenalinwiederaufnahmehemmer Atomoxetin gehört bei komorbiden Tic- oder Angststörungen zu den Mitteln der ersten Wahl und wird auch bei komorbiden Suchterkrankungen häufig bevorzugt eingesetzt (2, 3).
Laut Fachinformationen liegt die empfohlene Startdosis ab > 70 kgKG zwar bei 40 mg, aufgrund erhöhter Nebenwirkungen kann jedoch auch mit einer niedrigeren Dosierung (18 oder 25 mg) begonnen werden (9). Je nach individuellen Erfordernissen kann die Dosis dann im Verlauf auf bis zu maximal 100 mg am Tag gesteigert werden. Häufige Nebenwirkungen sind unter anderem Appetitminderung, Kopfschmerzen, abdominelle Schmerzen sowie Übelkeit. Ausserdem kann es zu einem Blutdruck- und Herzfrequenzanstieg kommen (2, 3). In der Schweiz wird die Substanz unter dem Handelsnamen Strattera® als Therapie zweiter Wahl angeboten, zur Behandlung einer seit dem Kindesalter fortbestehenden ADHS, bei Kindern ab 6 Jahren, Jugendlichen und Erwachsenen bis 50 Jahre im Rahmen einer therapeutischen Gesamtstrategie, wenn das Ansprechen auf eine zuvor erhaltene Behandlung mit Methylphenidat als klinisch unzureichend angesehen wird oder eine solche wegen Kontraindikationen nicht möglich ist.
Antidepressiva
Besonders bei komorbider, schwerer depressiver Episode gehören Antidepressiva mit einem dopaminergen und/oder noradrenergen Wirkprofil wie beispielsweise Bupropion (Wellbutrin® XR), Venlafaxin oder Duloxetin zu den Mitteln der ersten Wahl (3).
Psychotherapie
Die deutschen Leitlinien empfehlen eine multimodale Therapie aus psychopharmakologischer und psychotherapeutischer Behandlung, da besonders im Erwachsenenalter häufig sekundäre psychosoziale Folgen sowie komorbide Erkrankungen im Vordergrund stehen (2, 7). Dabei stellt eine ausführliche Psychoedukation die Grundlage jeder Behandlung dar.
Kognitiv-behaviorale Verfahren
Am besten untersucht und evaluiert sind psychotherapeutische Verfahren, die sich an kognitiv-behavioralen Konzepten orientieren (22, 25). Dabei stehen u.a. eine Bearbeitung dysfunktionaler Grundannahmen sowie die Erarbeitung von Strategien zur Verbesserung der Organisation und Aufmerksamkeitsfokussierung sowie der Emotionsregulation und Impulskontrolle im Vordergrund. Auch für eine achtsamkeitsbasierte Verhaltenstherapie liegen Wirksamkeitsnachweise vor (20).
Dialektisch-behaviorale Verfahren
Aufgrund der Überschneidungen der ADHS-Symptomatik mit emotional-instabilen Persönlichkeitszügen wurde mit dem «Freiburger Konzept» ein strukturiertes Verfahren zur Behandlung der ADHS entwickelt, das an das von Marsha Linehan konzipierte Dialektisch-Behaviorale-Therapieprogramm angelehnt ist (10). Dabei sollen die Patienten im Rahmen eines strukturierten Vorgehens u.a. eine verbesserte Emotionsregulation und Fertigkeiten zum besseren Umgang mit Anspannung sowie Achtsamkeitstechniken erlernen. Die Effektivität dieses Konzeptes konnte in verschiedenen Studien nachgewiesen werden (4, 11).
Zusammenfassung
Während früher davon ausgegangen wurde, dass die Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) eine Erkrankung des Kindesalters darstellt, konnte mittlerweile gezeigt werden, dass die Symptome bei etwa 50-80% der Betroffenen zumindest teilweise bis ins Erwachsenenalter persistieren (2, 4). Dabei kann es jedoch zu einem entwicklungsbedingten Symptomwandel kommen.
Bei der Diagnosestellung steht die klinische Diagnostik im Vordergrund. Es liegen jedoch zusätzlich auch verschiedene evaluierte und diagnoseweisende Fragebögen und strukturierte Interviews vor. Die Therapie fusst auf einer Kombination von Pharmakotherapie und Einzel- oder Gruppentherapiekonzepten, deren Wirksamkeit in verschiedenen Studien belegt werden konnte.
Psychiatrie und Psychotherapie
Universitätsklinikum Bonn
Venusberg-Campus 1
D-53127 Bonn
helena.rosen@ukbonn.de
Psychiatrie und Psychotherapie
Universitätsklinikum Bonn
Venusberg-Campus 1
D-53127 Bonn
Dr. H. Rosen hat keine Interessenskonflikte. Prof. A. Philipsen gibt im Zusammenhang mit diesem Artikel folgende mögliche Interessenskonflikte an: Beratertätigkeit, Vortragstätigkeit: Janssen-Cilag, Lilly, Medice, Novartis, Shire/Takeda; Prüfarzttätigkeit in Zulassungsstudien: Lilly, Medice, Novartis; Veranstaltungen der Klinik / Kongressreisen wurden unterstützt durch Lundbeck, Servier, Janssen-Cilag, Lilly, Medice, Novartis, Shire/Takeda. Buch- und Zeitschriftenartikel zum Thema ADHS.
1. American Psychiatric Association. Diagnostisches und Statistisches Manual Psychischer Störungen – DSM-5. 2014; Hogrefe, Göttingen
2. Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften. S3-Leitlinie: Aufmerksamkeitsdefizit- / Hyperaktivitätsstörung (ADHS) im Kindes-, Jugend- und Erwachsenenalter. 02.05.2017 URL: https://www.awmf.org/leitlinien/detail/ll/028-045.html. (Zugriff am 29.06.2019)
3. Benkert O, Hippius H. Kompendium der Psychiatrischen Pharmakotherapie. 2019; Springer, Berlin
4. Biederman J, Mick E, Faraone SV. Age-dependent decline of symptoms of attention deficit hyperactivity disorder: impact of remission definition and symptom type. Am J Psychiatry 2000; 157(5): 816-818
5. De Zwaan M, Gruss B, Müller A et al. The estimated prevalence and correlates of adult ADHD in a German community sample. Eur Arch Psychiatry Clin Neurosci 2012; 262: 79–86
6. Dilling H, Freyberger H. Taschenführer zur ICD-10-Klassifikation psychischer Störungen: nach dem Pocket Guide von J. E. Cooper. 2019; Huber, Bern
7. Ebert D, Krause J, Sackenheim C et al. ADHS im Erwachsenenalter – Leitlinien auf Basis eines Expertenkonsensus mit Unterstützung der DGPPN. Nervenarzt 2003; 74: 939–945
8. Faraone SV, Glatt SJ. A comparison of the efficacy of medications for adult attention- deficit/hyperactivity disorder using meta-analysis of effect sizes. J Clin Psychiatry 2010; 71(6): 754-763
9. Groß S, Figge C, Matthies S, Philipsen A. ADHS im Erwachsenenalter. Nervenarzt 2015; 9: 1171-1180
10. Hesslinger B, Philipsen A, Richter H. Psychotherapie der ADHS im Erwachsenenalter. 2004; Hogrefe, Göttingen
11. Hirvikoski T, Waaler E, Alfredson J et al. Reduced ADHD symptoms in adults with ADHD after structured skills training group: Results from a randomized controlled trial. Beh Res Ther 2011; 49:175–185
12. Jacob CP, Philipsen A, Ebert D, Deckert J. Multimodale Therapie der Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung im Erwachsenenalter. Nervenarzt 2008; 79: 801-808
13. Kessler RC, Adler LA, Barkeley R et al. Patterns and predictors of attention-deficit/hyperactivity disorder persistence into adulthood: results from the national comorbidity survey replication. Biol Psychiatry 2005; 57:1442–1451
14. Krause J, Krause KH. ADHS im Erwachsenenalter. 2014; Schattauer, Stuttgart
15. Linderkamp F, Lauth G. Zur Wirksamkeit pharmakologischer und psychotherapeutischer Therapien bei Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) im Erwachsenenalter: Eine empirische Metaanalyse. Verhaltenstherapie 2011; 21: 229-238.
16. Meszaros A et al. Pharmacotherapy of adult attention deficit hyperactivity disorder (ADHD): a metaanalysis. Int J Neuropsychopharmacol 2009; 12(8): 1137-1147
17. NICE, Attention Deficit Hyperactivity Disorder – Diagnosis and management of ADHD in children, young people and adults. National Clinical Practice Guideline Number 72. 2009; London: National Collaborating Centre for Mental Health commissioned by the National Institute for Health & Clinical Excellence
18. Philipsen A, Richter H, Peters J et al. Structured group psychotherapy in adults with attention deficit hyperactivity disorder: results of an open multicentre study. J Nerv Ment Dis 2007; 195:1013–1019
19. Retz-Junginger P, Sobanski E, Alm B, Retz W, Rösler M. Alters- und geschlechtsspezifische Besonderheiten der Aufmerksamkeitsdefizit-/ Hyperaktivitätsstörung. Nervenarzt 2008; 7: 809-819
20. Schoenberg PL et al. Effects of mindfulness-based cognitive therapy on neurophysiological correlates of performance monitoring in adult attention-deficit/hyperactivity disorder. Clin Neurophysiol 2014; 125(7): 1407-16
21. Simon V et al. Prevalence and correlates of adult attention-deficit hyperactivity disorder: meta-analysis. Br J Psychiatry 2009; 194: 204-211
22. Vidal-Estrada R, Bosch-Munso R, Nogueira-Morais M et al. Psychological treatment of attention deficit hyperactivity disorder in adults: a systematic review. Actas Esp Psiquiatr 2012; 40:147–154
23. Volkow ND et al. Role of dopamine in the therapeutic and reinforcing effects of methylphenidate in humans: results from imaging studies. Eur Neuropsychopharmacol 2002; 12(6): 557-566
24. Wender PH. Attention-deficit hyperactivity disorder in adults. Oxford Univ Press 1995; New York Oxford
25. Young S et al. Cognitive-behavioural therapy in medication-treated adults with attention- deficit/hyperactivity disorder and co-morbid psychopathology: a randomized controlled trial using multi-level analysis. Psychol Med 2015; 45(13): 2793-804.