Die intrauterine Wachstumsretardierung (intrauterine growth restriction, IUGR) ist eine häufige Schwangerschaftskomplikation, welche mit einer erhöhten fetalen Morbidität und Mortalität assoziiert ist. Eine Unterscheidung zwischen konstitutionell kleinen und wachstumsrestringierten Feten ist fundamental nicht nur für die Überwachung sondern auch für das Outcome der Schwangerschaft und die Definierung des Entbindungszeitpunktes. Ein wichtiges Tool dafür ist unter anderem die dopplersonographische Kontrolle des Feten.
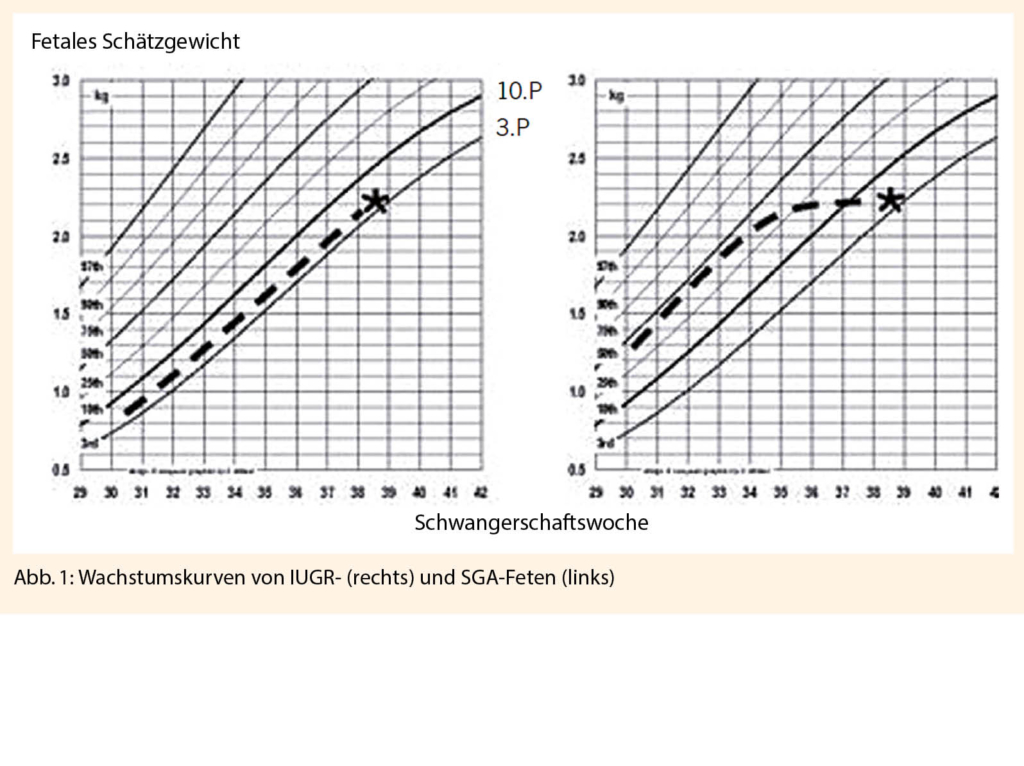
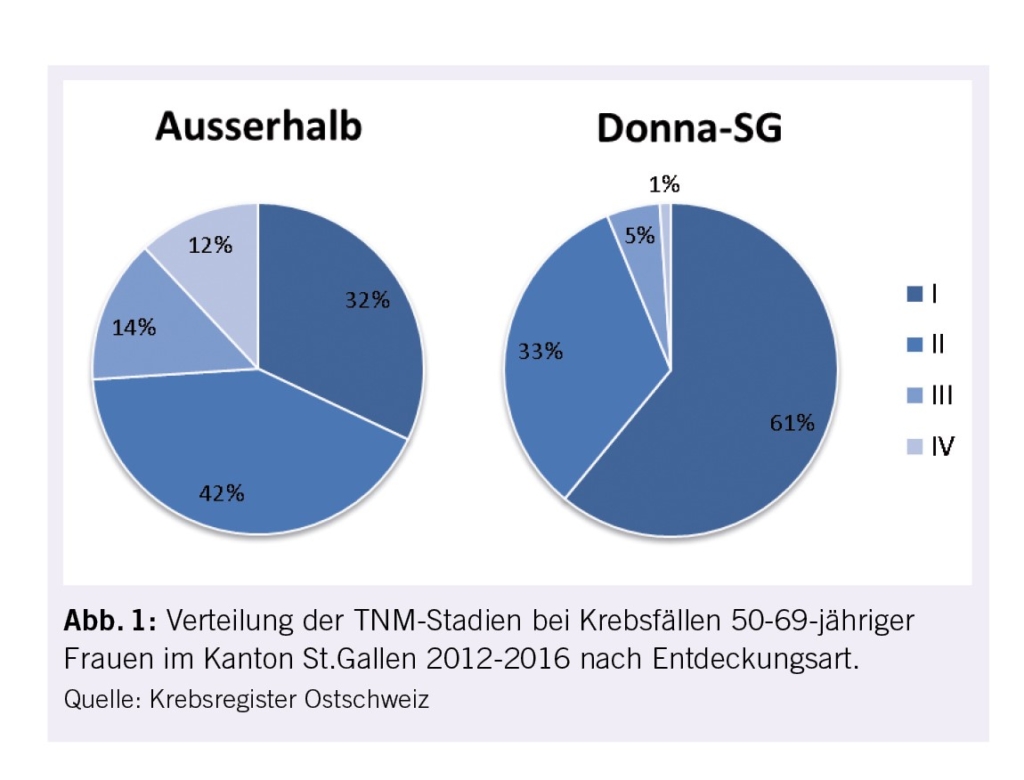
Als small for gestational age (SGA) gelten die Feten oder Neugeborenen, deren Schätz- oder Geburtsgewicht unterhalb der 10. Perzentile liegt. Es handelt sich um konstitutionell kleine Feten mit einem kontinuierlichen Wachstum auf perzentilengerechtem Niveau (Abb. 1. links). Obwohl nicht alle SGA Kinder zwangsläufig mit einem erhöhten Morbiditätsrisiko behaftet sind, ist die perinatale Morbidität und Mortalität bei einem fetalen Schätzgewicht unterhalb der 3. Perzentile deutlich erhöht (1).
Eine intrauterine Wachstumsretardierung (IUGR) besteht, wenn sich das fetale Schätzgewicht unter der 10. Perzentile befindet und/oder eines der folgenden Charakteristika vorliegt:
a) wenn kein perzentilengerechtes Wachstum vorhanden ist (die Wachstumskurve im Verlauf abflacht) oder
b) bei pathologischer Dopplersonographie der Arteria umbilicalis oder
c) bei pathologischer Dopplersonographie der Arteriae uterinae oder
d) bei Vorliegen eines Oligohydramnions
Diese Feten können ihr Wachstumspotential plazentar bedingt nicht ausschöpfen (Abb. 1 rechts).
Neben einer erhöhten Mortalität haben diese Neugeborenen ein erhöhtes Risiko für Zerebralparese, Kleinwuchs, Frühge-
burtlichkeit oder Herz-Kreislauf-Erkrankungen und Stoffwechselerkrankungen im späteren Leben (2).
Deswegen ist eine frühe Erkennung und diesbezüglich richtige Betreuung dieser Feten von grosser Bedeutung. Man unterscheidet zwischen einer frühen (early onset, < 34 SSW) IUGR und einer späten (late onset, ≥ 34 SSW) IUGR.
Ätiologie
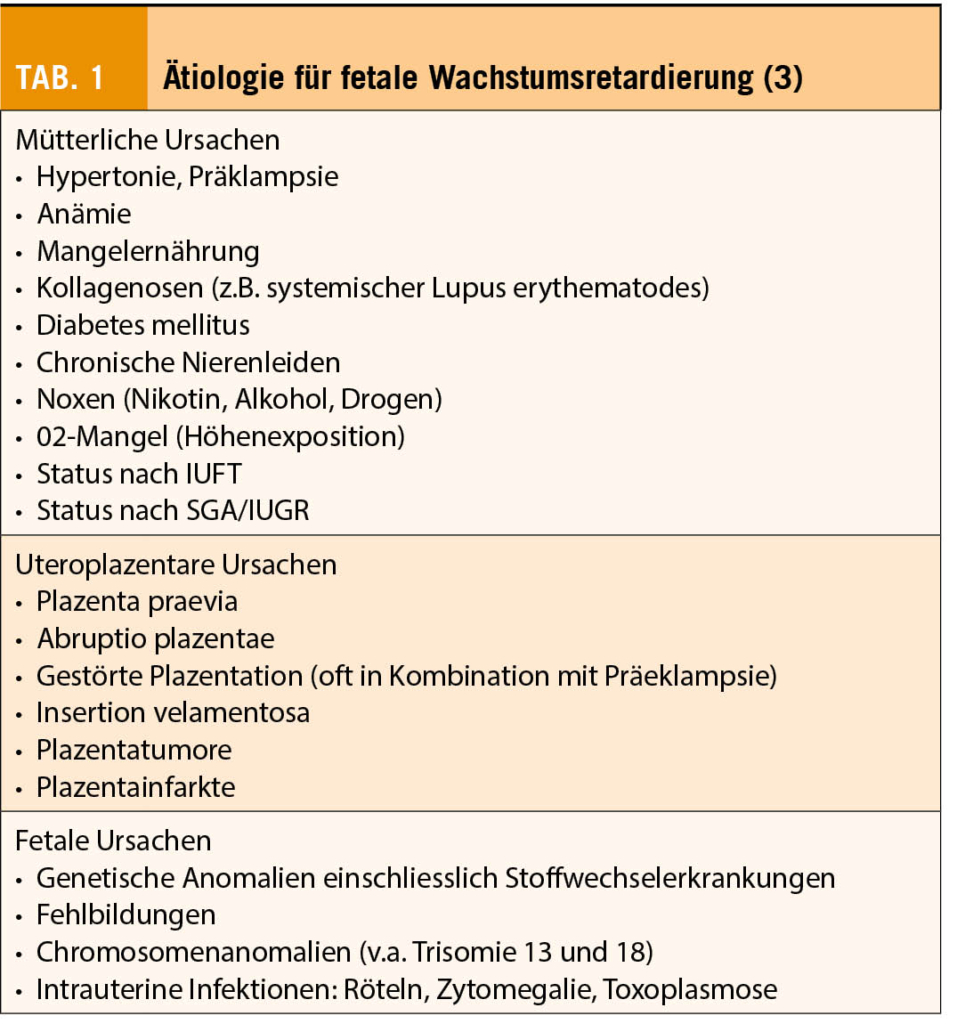
Die IUGR tritt in ca. 5-10% aller Schwangerschaften auf. Ihre Ätiologie ist multifaktoriell und kann in mütterliche (präplazentare), plazentare und fetale (endogene und exogene) Ursachen eingeteilt werden (Tab. 1).
Diagnostik
Bei Verdacht auf eine intrauterine Wachstumsretardierung ist zunächst die Überprüfung des Gestationsalters (mit evtl.Terminkorrektur) gemäss Scheitel-Steiss-Länge wichtig.
Es sollen sequentielle Messungen zur Gewichtsschätzung mit Überprüfung des Wachstumsverlaufs erfolgen.
Falls das fetale Schätzgewicht unter der 10. Perzentile liegt oder kein perzentilengerechtes Wachstum vorhanden ist, kann durch die Bestimmung der Fruchtwassermenge und der Dopplerparameter zwischen einem SGA- und einem IUGR- Feten unterschieden werden. Plazenta und Nabelschnurmorphologie sowie –insertion sollten ebenfalls überprüft werden.
Bei Verdacht auf frühe IUGR sollte zusätzlich noch eine infektiologische Abklärung oder eine Feindiagnostik mit Karyotypisierung zum Ausschluss chromosomaler oder struktureller Anomalien in Erwägung gezogen werden. Im Rahmen der Schwangerenvorsorge empfiehlt sich eine Kardiotokographie (CTG), wenn möglich mit Beurteilung der Mikrofluktuation.
Überwachung bei IUGR
Nach der Diagnosestellung einer IUGR soll durch regelmässige klinische und sonographische Verlaufskontrollen der fetale und maternale Zustand motorisiert werden. Bei Hinweiszeichen für eine Präeklampsie erfolgen zusätzlich klinische und laborchemische Kontrollen. Sonographische Verlaufskontrollen des fetalen Wachstums, der Fruchtwassermenge und der Dopplerparameter erlauben eine ganzheitliche Überwachung der feto- und uteroplazentaren Funktion. Die fetale Gewichtsbestimmung erfolgt in der Regel alle 2 Wochen. Bei Auffälligkeiten in den Dopplerparametern sollte eine Verlaufssonographie je nach Schweregrad der IUGR in kürzeren Intervallen stattfinden.
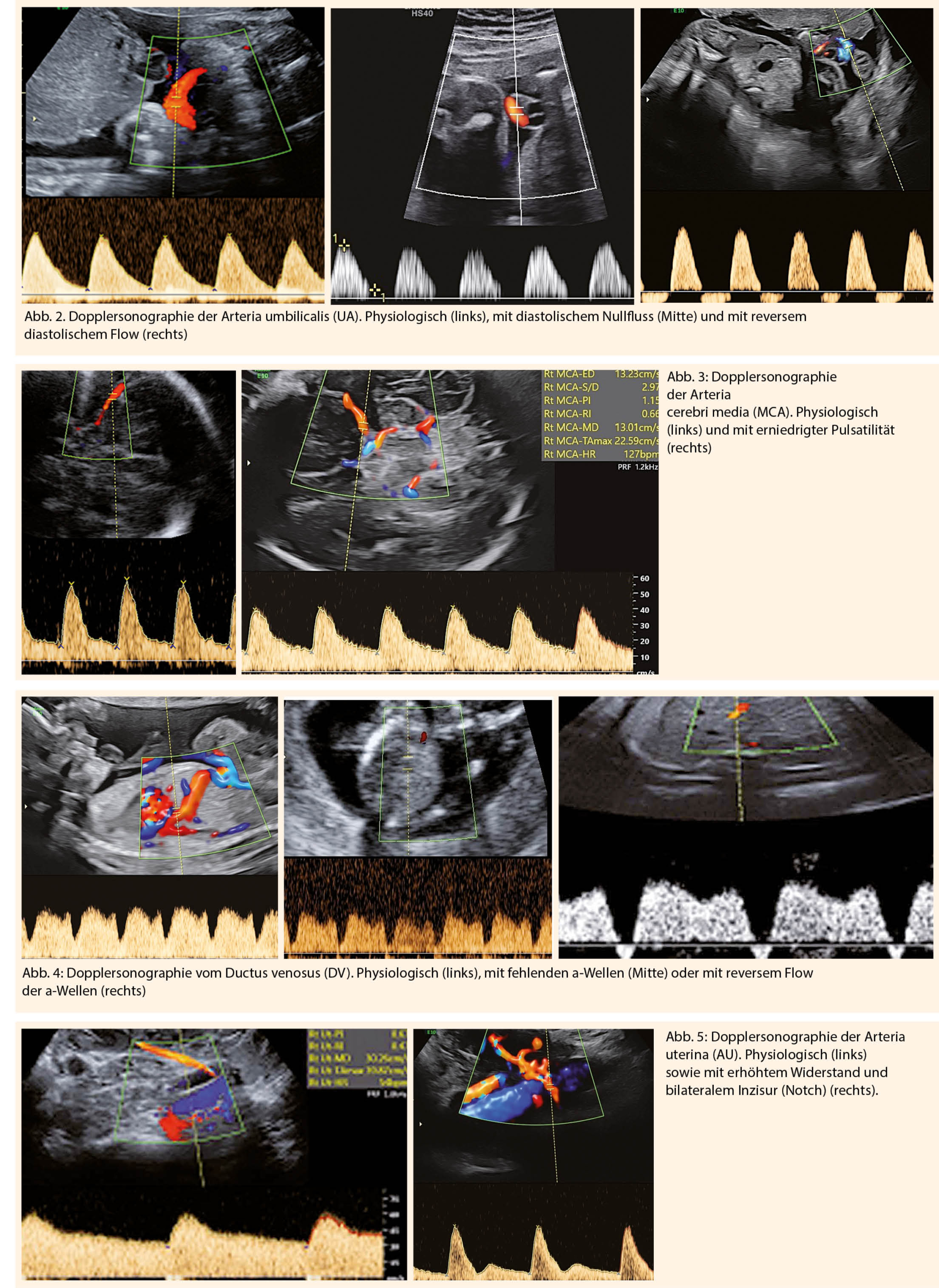
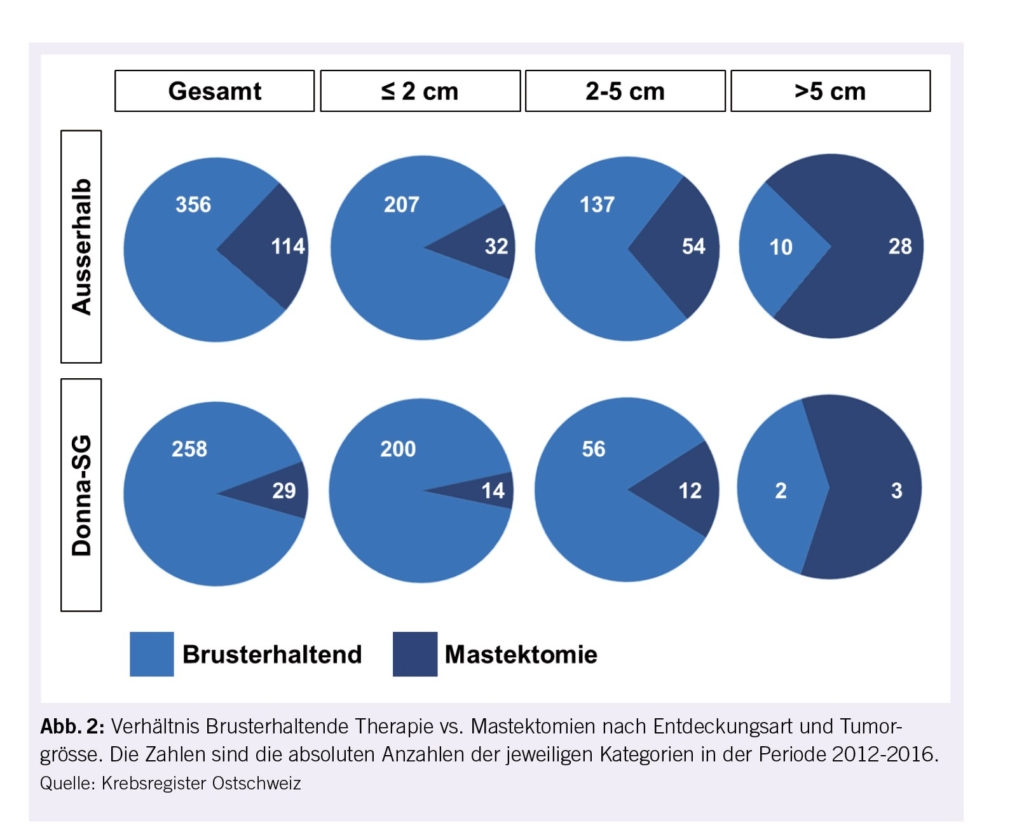
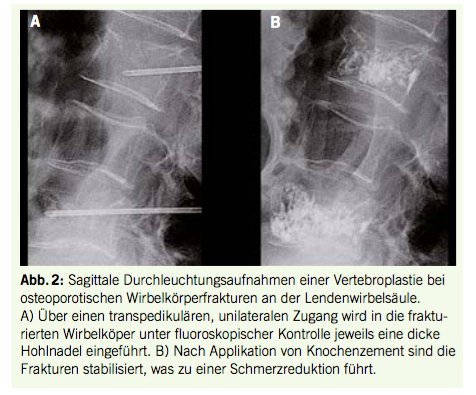
Die Dopplersonographie der Arteria umbilicalis (UA) trägt zur Reduktion der perinatalen Mortalität bei. Pathologische Zeichen sind ein erhöhter Resistence-Index (RI>95.P) oder Pulsatilitäts- Index (PI>95.P), ein diastolischer Nullfluss (AED-flow) oder ein reverser diastolischer Blutfluss (RED-flow) in der A. umbilicalis (Abb. 2). Diese Zeichen sind eher mit einer schlechteren Prognose assoziiert (4).
Bei auffälligen Befunden der Arteria umbilicalis sollten ebenfalls die Dopplerparameter der Arteria cerebri media (MCA) und der Arteria uterinae gegebenenfalls des Ductus venosus (DV) kontrolliert werden. Die Dopplersonographie der Arteria cerebri media ermöglicht die Überwachung vom hämodynamischen Status des Feten. Ein pathologischer Befund der MCA ist ein erniedrigter Resistence-Index (RI<5.P) oder Pulsatilitäts-Index (PI<5.P) aufgrund einer zerebralen Vasodilatation des Feten auch bezeichnet als brain-sparing effect (Abb. 3) (5).
Als weiterer wichtiger Parameter zur fetalen Überwachung bei IUGR gilt die cerebroplacentare Ratio (CPR), der Quotient aus dem PI der A. cerebri media und dem PI der A. umbilicalis. Pathologische CPR- Werte unter der 5. Perzentile gelten als aussagekräftiger Indikator einer fetalen Hypoxie (6).
Eine fehlende a-Welle im Ductus venosus (DV) oder ein reverse flow der a-Welle sind Zeichen für eine drohende oder auch bereits bestehende Azidämie (Abb. 4). Die Dopplersonographie der Arteria uterinae (AU) kann Hinweise auf eine potentiell gestörte Plazentation und Trophoblastinvasion bereits ab dem 1. Trimester geben. Zeichen der gestörten Blutströmung ist das Ausbleiben der Widerstandsabsenkung der uterinen Durchblutung, was sich oft mit einem doppelseitigen Inzisur (Notch) manifestiert (Abb. 5). Durch Bestimmung vom mittleren uterinen Widerstand im 3. Trimenon ist die Differenzierung zwischen konstitutionell kleinen und wachstumsretardierten Feten möglich. (7)
Management
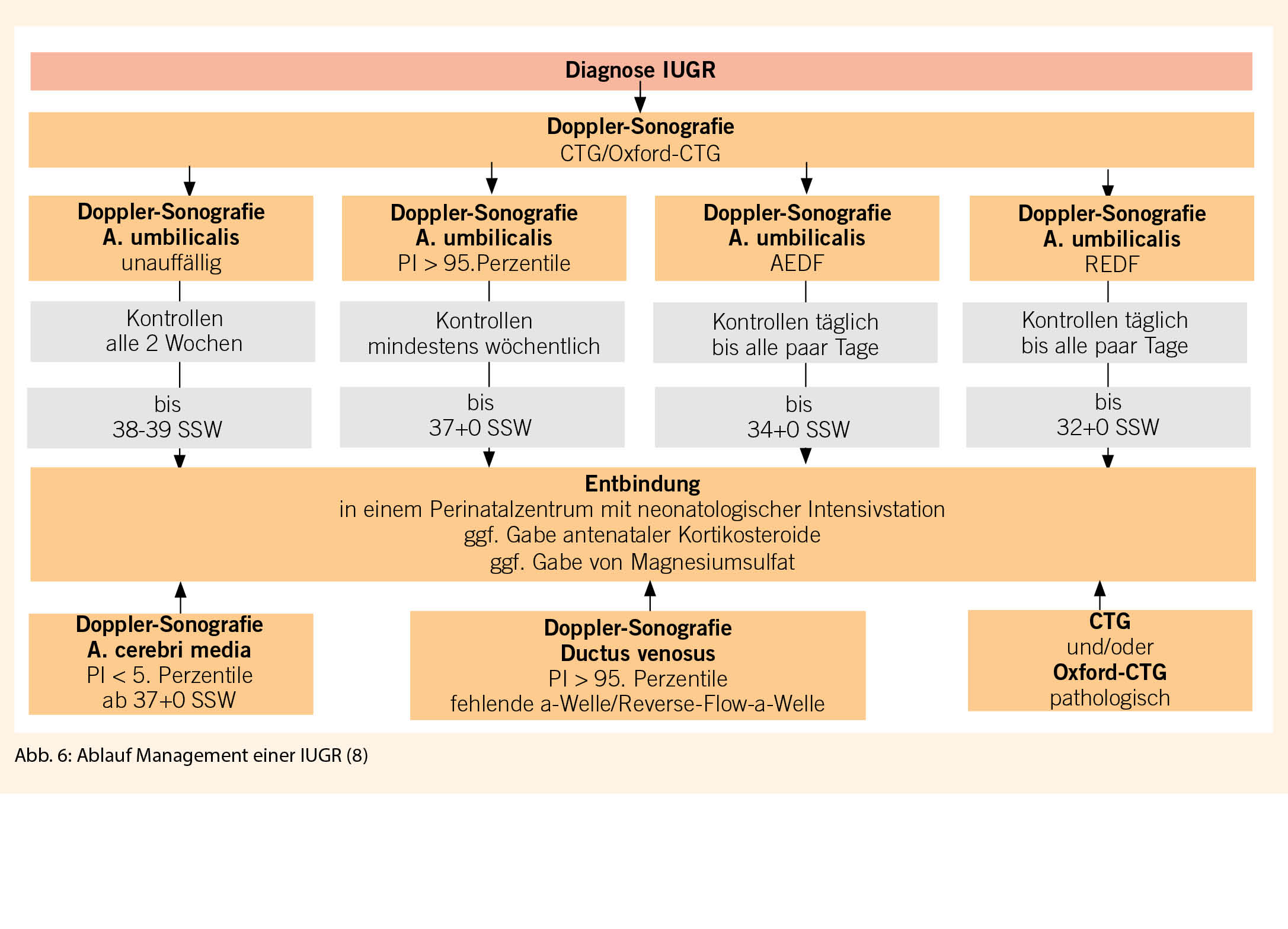
Das Management und das Festlegen des Entbindungszeitpunkts sollen individuell je nach Schweregrad der IUGR entschieden werden (Abb. 6). Im Falle einer geplanten Entbindung vor der abgeschlossenen 34. Schwangerschaftswoche sollte die Gabe von Kortikosteroiden antenatal im Sinne einer Lungenreifung erfolgen (9). Eine Entbindung im Perinatalzentrum für die bestmögliche Betreuung des Neugeborenen ist empfohlen. Der Entbindungsmodus soll individuell unter Berücksichtigung vom gesamten klinischen Bild je nach Schwangerschaftswoche und fetalen Reserven bestimmt werden.
Prävention
Falls es anamnestisch ein erhöhtes Risiko für die Entwicklung einer gestörten uteroplazentaren Perfusion bzw. einer intrauterinen Wachstumsretardierung gibt, soll die prophylaktische Gabe von niedrig-dosiertem Acetylsalizylsäure (ASS) 100-150 mg vor der 16. Schwangerschaftswoche empfohlen werden (10). Eine Abstinenz von Nikotin scheint ebenfalls das Risiko für eine IUGR zu reduzieren.
Copyright bei Aerzteverlag medinfo AG
Universitätsspital Zürich
Rämistr.100
8091 Zürich
Chefärztin Geburtshilfe Kantonsspital Graubünden
Frauenklinik Fontana
Departement Gynäkologie und Geburtshilfe
Lürlibadstrasse 118
7000 Chur
carolin.blume@ksgr.ch
Die Autoren haben keine Interessenkonflikte in Zusammenhang mit diesem Artikel
1. Uhl B. Intauterine Wachstumsretardierung. Gynäkologie und Geburtshilfe compact 2013 (5): 229
2. Kehl S et al. Intrauterine Growth Restriction. Deutsche Gesellschaft Gynäkologie und Geburtshilfe (S2k-Level, AWMF Registry No. 015/080, October 2016) Version 1: 26-27
3. Kehl S et al. Intrauterine Growth Restriction. Deutsche Gesellschaft Gynäkologie und Geburtshilfe (S2k-Level, AWMF Registry No. 015/080, October 2016) Version 1: 29
4. Aliferevic Z. et al. Fetal and umbilical Doppler ultrasound in high-risk pregnancies. The cohrane database of systematic reviews 2013; 11: CD007529
5. Suzanne L. Miller et al. The consequences of fetal growth restriction on brain structure and neurodevelopmental outcome. The Journal of Physiologie 594.4 (2016) pp 807–823