Das Blutbild ist eine zentrale Untersuchung und wichtige Hilfestellung in vielen Notfallsituationen. Natürlich werden Laborwerte stets im klinischen Kontext interpretiert und vom behandelnden Arzt kritisch hinterfragt. Veränderungen im Blutbild können auch eine unerwartete Notfall-Situation induzieren, die Fragen aufwerfen und gelegentlich akuten Handlungsbedarf zur Folge haben. Im Folgenden besprechen und illustrieren wir typische «Blutbildnotfälle», die im hämatologischen Konsiliardienst häufig sind und auch zum allgemein-internistischen «Rucksack» gehören.
Der Pseudo-Blutbildnotfall
Insbesondere bei asymptomatischen Patienten mit ungewöhnlichen Abweichungen von den Referenzbereichen muss an Artefakte gedacht werden.
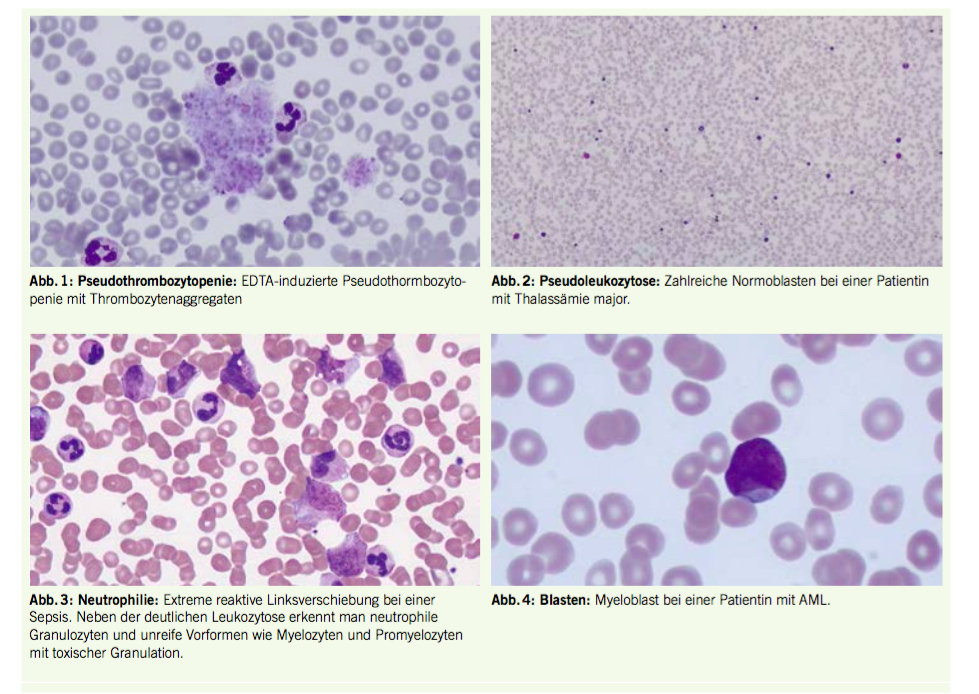
Pseudothrombozytopenie:
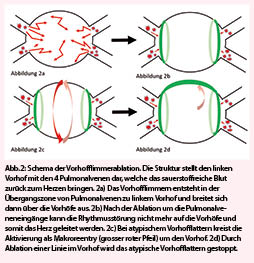
Erniedrigte Thrombozyten bei der Zählung im EDTA-Blut können durch Aggregation oder Anlagerung der Plättchen an Leukozyten auftreten (1) (Abb. 1). Gleichzeitig kann eine Pseudoleukozytose gemessen werden, wenn die Thrombozyten-Aggregate fälschlicherweise maschinell als Leukozyten gezählt werden. Die Aggregatbildung kann durch den Ersatz durch andere Antikoagulantien, z.B. Natriumcitrat, verhindert werden. Die Thrombozytenaggregate lassen sich durch mikroskopische Ausstrichuntersuchung erkennen. In der Regel wird ein medizinisch-analytisches Labor direkt bei der Erfassung einer Thrombozytopenie (<100 000/μl) einen Ausstrich durchführen und die Thrombozytenzahl mikroskopisch schätzen.
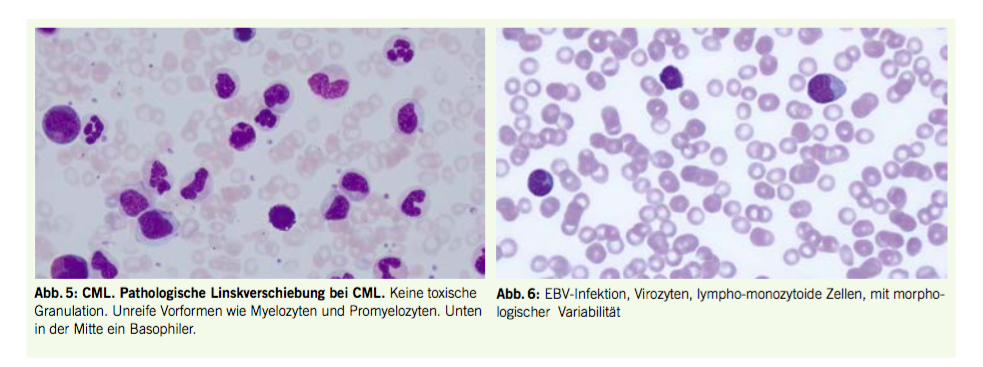
Pseudoleukozytose
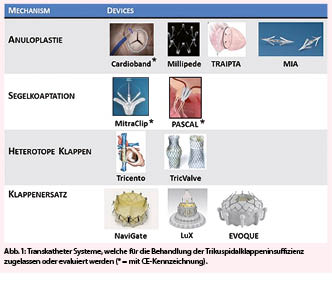
Eine Pseudoleukozytose oder Pseudohyperleukozytose (Abb. 2) kann bei Patienten mit Thalassämien (intermedia und major) irrtümlicherweise gemessen werden, wenn die Zellzahlen mit einem Hämatolologie-Analyser gemessen werden. Seit mehreren Jahren bieten aber die grösseren Hämatologie-Analysen die Möglichkeit einer Diskriminierung zwischen Erythroblasten und «echten» (d.h. myeloisch/monozytären oder lymphatischen) Leukozyten. Die korrigierten Leukozytenzahlen werden als NRBC-korrigierte Leukozyten bezeichnet. Es empfiehlt sich eine Kontrolle mittels Blut-Ausstrich, wo die Diskrepanz zwischen «echten» Leukozyten und Erythroblasten/Normoblasten deutlich erkennbar wird (1). Um die korrekte Leukozytenzahl zu erfassen, sollte bei Patienten mit Thalassämien das Blutbild in einer venösen Blutentnahme bestimmt werden.
Der «weisse» Blutbildnotfall
Neutropenie
Eine schwere Neutropenie (Neutrophile Granulozyten < 0,5 x 109/l) stellt immer einen Notfall dar, weil diese Patienten ein deutlich erhöhtes Risiko aufweisen, schwere Infektionen zu erleiden (2). Die Neutropenie kann auch bei einer normalen Gesamtleukozytenzahl vorliegen und wird erst anhand des Differentialblutbildes festgestellt.
Eine erwartete Neutropenie tritt am häufigsten bei Patienten nach einer Chemotherapie oder seltener unter einer Immunsuppression auf (z.B. Azathioprin, Methotrexat) und ist in der Regel nicht isoliert.
Bei einer unerwarteten isolierten Neutropenie muss vor allem an eine medikamentös-induzierte Agranulozytose gedacht werden. In diesem Fall ist die genaue Medikamentenanamnese elementar. Zu den Medikamenten, die eine Neutropenie induzieren können, gehören z.B. Nichtsteroidale Antirheumatika, Antiepileptika oder Neuroleptika. Eine schwere Neutropenie kann sehr selten auch bereits nach einmaliger Anwendung von Metamizol auftreten (immunologisch induzierte Agranulozytose) (2). Diese kann rasch nach Reexposition auftreten, weshalb das Medikament nie mehr bei diesen Patienten eingesetzt werden darf (Ausweis!).
Bei klinisch stabilen asymptomatischen afebrilen Patienten werden engmaschige Kontrollen empfohlen. Diese Patienten können vom Einsatz myeloischer Wachstumsfaktoren profitieren. Meist ist eine fachärztliche Beurteilung einschliesslich einer Knochenmarkpunktion indiziert.
Bei Patienten mit schwerer Neutropenie, Fieber und/ oder Anzeichen einer Infektion, ist eine notfallmässige Hospitalisation indiziert. Das Fieber (>38°C) kann das einzige Symptom sein, weil bei Agranulozytose die klinischen, bekannten Symptome der Infektion oft fehlen respektive fälschlicherweise als leicht erscheinen.
Eine unerwartete Neutropenie mit Thrombozytopenie oder/und mit Anämie weist auf eine schwere hämatologische Krankheit und erfordert umgehend fachärztliche Abklärungen einschliesslich Knochenmarkpunktion (2). Eine mikroskopische Ausstrichbeurteilung hilft, die Morphologie der Zellen im peripheren Blut unmittelbar zu beurteilen.
Leukozytose
Eine Leukozytose muss immer im Kontext mit anderen Symptomen und Befunden interpretiert werden. Die Leukozytosen sind überwiegend reaktiv und nur selten maligne.
Die maligne Form muss rasch erkannt und behandelt werden.
Die Höhe der Leukozytenzahl allein kann nicht sicher zwischen einer reaktiven oder malignen Ursache unterscheiden. Es bedarf einer mikroskopischen Beurteilung (Ausstrich), um die Morphologie der Zellen im peripheren Blut zu charakterisieren und die Dringlichkeit der Situation einzuschätzen (3).
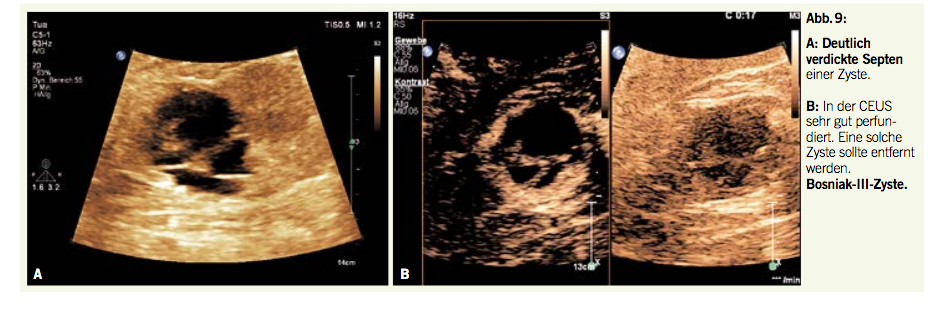
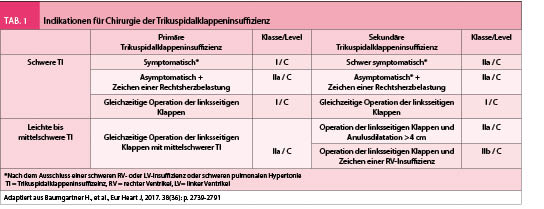
Als Linksverschiebung bezeichnet man unreife Vorformen der Granulozyten, oft mit basophilen Schlieren und toxischen Granulationen (Abb. 3).
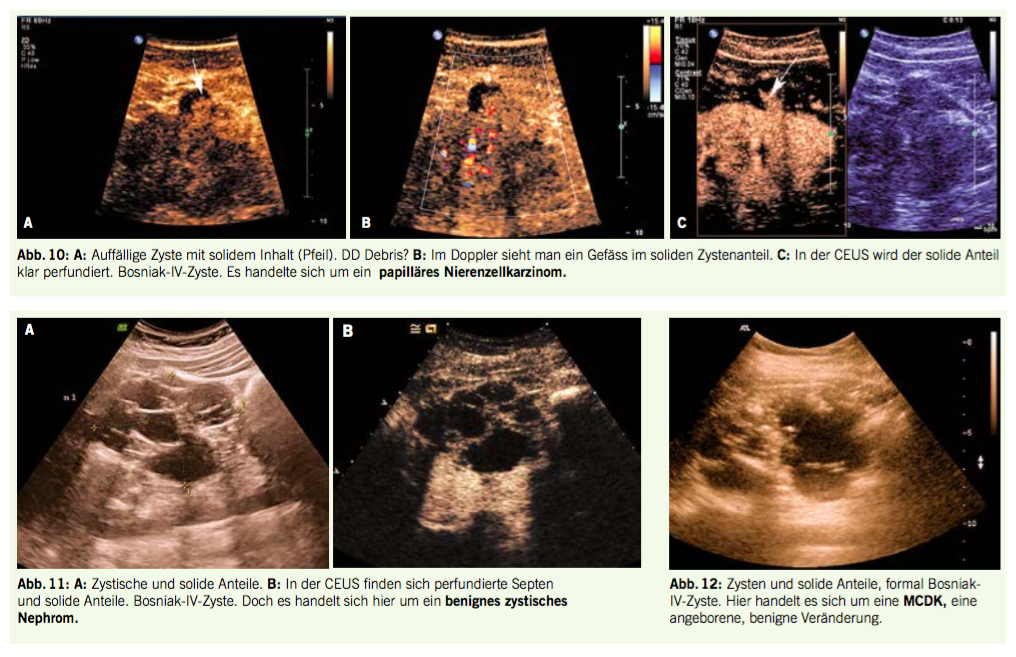
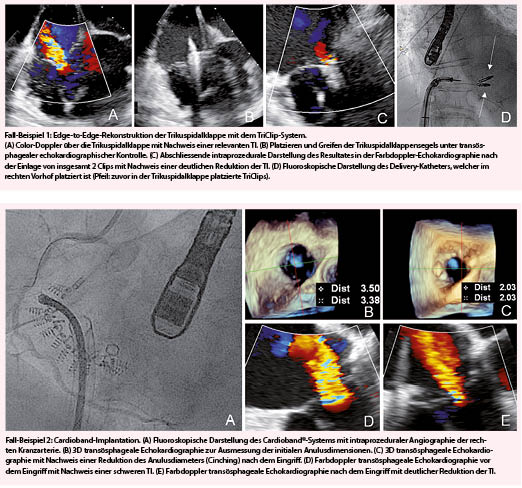
Bei einem Hiatus leukaemicus finden sich Blasten in Kombination mit reifen Granulozyten bei gleichzeitiger Abwesenheit der Zwischenformen wie Promyelozyten, Myelozyten und stabkernigen Neutrophilen; es besteht hier der dringende Verdacht auf eine akute Leukämie (Abb. 4).
Ein monomorphes Bild identisch aussehender Blutzellen im Ausstrich, z.B. Blasten oder Lymphozyten, suggeriert eine bösartige Erkrankung (3). Im Scattergramm des Differentialblutbildes erkennt man eine abnorme Verteilung der Lymphozyten- und der Monozyten-Population. Der Hämatologie-Analyser meldet dann allenfalls einen «Blasten»-Alarm.
Ein pleomorphes Bild, d.h. das Auftreten vieler morphologisch unterschiedlicher Zellen, kann hingegen sowohl bei reaktiven als auch bei malignen Leukozytosen vorliegen.
Bei einer Sepsis sehen wir im Rahmen der reaktiven Linksverschiebung eine pleomorphe Leukozytose (Abb. 3). In ähnlicher Form findet man diese ebenfalls bei der Chronischen Myeloischen Leukämie (CML, Abb. 5).
Infektiöse Mononukleose
Bei infektiöser Mononukleose findet sich ein typisches «buntes» Bild mit Lymphozytose und Vermehrung lympho-monozytoider Zellen («Virozyten», Abb. 6). Auffällig ist die morphologische Variabilität der Zellen. Obwohl einzelne Lymphozyten an leukämische Lymphozyten erinnern können, sind die Lymphozyten pleomorph, was bei Leukämien unwahrscheinlich ist (1). Eine vermehrte Anzahl von «aktivierten» Lymphozyten wird vom Hämatologieautomaten ebenfalls erkannt und mit den klassischen Warnhinweisen («Abn. Lymph/L-Blast» und/oder «Atyp. Lymph») quittiert.
Bei einer Leukozytose mit Polyglobulie und/oder Thrombozytose muss an eine myeloproliferative Erkrankung gedacht werden.
Hyperleukozytose
Eine Hyperleukozytose (Leukozytenzahlen ≥ 100*10³/µl) ist immer ein Notfall, da hier eine lebensbedrohliche Leukostase mit Hyperviskosität und verminderter Gewebeperfusion auftreten kann (3). Für das Auftreten einer Leukostase ist nicht allein die Leukozytenzahl, sondern auch das Zellvolumen wichtig. Deshalb sind Patienten mit einer akuten myeloischen Leukämie (AML) oder chronischen myeloischen Leukämie (CML) mit grossen myeloischen Vorläuferzellen im peripheren Blut eher gefährdet.
Warnzeichen bei einer Leukozytose sind in Tabelle 1 zusammengefasst:
- Blasten im peripheren Blutbild
- Leukozytenzahl > 50*10³/µl
- Hyperleukozytose (Lc ≥ 100*10³/µl) mit den Symptomen: Schwindel, Sehstörungen, Delir, Dyspnoe, Blutungen
- Leukozytose mit Anämie und/oder Thrombozytopenie
- Leukozytose mit Polyglobulie und/oder Thrombozytose
- Leukozytose mit B-Symptomatik, Lymphadenopathie und Verschlechterung des Allgemeinzustands
Der «rote» Blutbildnotfall
Anämie
Entscheidend für die Beurteilung einer Anämie als Notfall sind das Tempo der Entstehung, die Klinik und die weiteren Laborbefunde.
Eine schwere megaloblastäre Anämie oder eine Eisenmangelanämie bei chronischer Blutung, die sich jedoch sehr langsam entwickelte, wird oft überraschend gut vertragen.
Eine akute hämolytische Anämie stellt immer einen Notfall dar. Die Morphologie der Erythrozyten (Makrozytose, Polychromasie, Normoblasten, Retikulozytose), der Nachweis von Fragmentozyten und die Thrombozytenzahl spielen bei Abklärung einer Hämolyse eine wichtige Rolle.
Bei einer Coombs-positiven hämolytischen Anämie kann es zu einer raschen Dekompensation der Hämolyse mit relevantem Hämoglobinabfall und entsprechender Symptomatik kommen.
Der Nachweis zahlreicher Fragmentozyten bei einer Coombs-negativen, hämolytischen Anämie ist dringend verdächtig auf eine Erkrankung aus dem Formenkreis der mikroangiopatischhämolytischen Anämien, wie z.B. die thrombotisch-thrombozytopenische Purpura (TTP) und das hämolytisch-urämische Syndrom (HUS). Zudem weisen diese Patienten eine Thrombozytopenie, eine deutlich erhöhte LDH, ein erniedrigtes Haptoglobin, Fieber, neurologische Symptome und eine Niereninsuffizienz auf (4).
Polyglobulie und erhöhter Hämatokrit
Bei erhöhtem Hämatokrit sollten zuerst die häufigeren und naheliegende Ursachen wie Flüssigkeitsmangel bzw. -verlust sowie eine chronische obstruktive Pneumopathie ausgeschlossen werden. Bei deutlich erhöhte Hämatokrit muss an eine chronische myeloproliferative Erkrankung wie z.B. die Polycythaemia vera gedacht werden.
Klinisch stehen in der Regel Symptome im Vordergrund, welche durch die erhöhte Blutviskosität und Mikrozirkulationsstörungen bedingt sind (z.B. gerötete Gesichtshaut, Kopfdruck/Kopfschmerzen, Hypertonie, Sehstörungen, Parästhesien, Erythromeralgie) oder thromboembolische Komplikationen. Die Therapie besteht im Aderlass und dem Beginn mit niedrig dosierter Acetylsalizylsäure.
Der «Plättchen»-Blutbildnotfall
Eine akute Thrombozytopenie (Plättchen < 100 ’000/ µl) stellt immer eine Notfall-Situation dar. Es muss sichergestellt werden, dass die Labordiagnostik rasch und eindeutig berichtet, ob es um eine Pseudo-Thrombozytopenie oder eine echte Thrombozytopenie handelt. Eine Pseudothrombozytopenie ist wahrscheinlich, wenn sich entweder im EDTA-antikoagulierten Vollblut Gerinnsel zeigen oder wenn im Ausstrich Thrombozytenaggregate gefunden werden. Diese Thrombozytenaggregate müssen aktiv am Rande der Ausstrichfahne gesucht werden
Bei einer Thrombozytenzahl < 5-10 x 109/l besteht ein hohes Risiko für Spontanblutungen (5).
Alter, Therapie mit Aggregationshemmern, Antikoagulantien und Comorbiditäten können bereits bei höheren Thrombozytenzahlen spontane Blutungen begünstigen. Klinik (Fieber, neurologische Symptome, Durchfälle) und Labor (Hämolyse, Fragmentozyten, Niereninsuffizienz, Gerinungstörungen) bestimmen die weiteren Massnahmen und die Dringlichkeit (4). Die Messqualität der Hämatologie-Analyser hat sich in den letzten Jahren in allen Belangen erfreulich verbessert, womit die untere Messgrenze der Thrombozytenkonzentration im Bereich von 1000 Plättchen/μl definiert wird und auch Aussagen zum Reifegrad sowie zur Anisozytose validiert sind.
An eine immunthrombozytopenie (ITP) denken wir bei asymptomatischen Patienten mit isolierter Thrombozytopenie. Erhöhte Fraktion der unreifen Thrombozyten (auf Sysmex-Analyser als IPF, «immature platelet fraction», bezeichnet) deutet auf gesteigerte Thrombopoiese bei peripherem Verbrauch. Bei Patienten über 60 Jahren wird meist eine Knochenmarkpunktion gemacht, da mit dem Alter das Risiko für andere Ursachen steigt. Eine Therapieindikation besteht in der Regel bei Thrombozytenzahl < 30 x109/l(5).
Ein absoluter Notfall ist eine Heparin-induzierte Thrombozytopenie (HIT). Die HIT ist dosisunabhängig, tritt in der Regel 5-10 Tage nach Beginn der Heparinisierung (UFH > LMWH > Heparinoide) auf. Nach Heparin-Reexposition kann sie auch innerhalb weniger Stunden auftreten und zu thrombotischen Komplikationen führen (5). Heparin muss sofort abgesetzt werden.
Zusammenfassend ist die Kenntnis der wichtigsten Blutbildnotfälle sowohl für die Aerzteschaft als auch für das medizinische Personal zusammen mit der Klinik als Weichenstellung für die weiteren Massnahmen und die Erkennung der Dringlichkeit von grossem Nutzen.
Copyright bei Aerzteverlag medinfo AG
Departement für Innere Medizin Kantonsspital Baden Im Ergel 1, 5404 Baden
veronika.ballova@ksb.ch
Departement für Innere Medizin Kantonsspital Baden Im Ergel 1, 5404 Baden
Leiter Gerinnungssprechstunde Kantonsspital Baden, 5404 Baden
Labor für Molekulare Kardiologie, Leiter Plättchenforschung,
Universität Zürich
Wagistrasse 12
8952 Schlieren
hansjuerg.beer@ksb.ch
Die Autoren haben deklariert, in Zusammenhang mit diesem Artikel keine Interessenskonflikte zu haben.
1. H. Löffler, J. Rastetter, T. Haferlach. Atlas der klinischen Hämatologie. Springer
2004.
2. J.L. Frater. How I investigate Neutropenia. Int J Lab Hematol. 2020;42 (Suppl.
1):121-132.
3. N. Abramson, B. Melton. Leukocytosis: Basics of Clinical Assessment. Am Fam
Physician. 2000 Nov 1;62(9):2053-2060ent.
4. J.J. Shatzel, MDa, J.A. Taylor. Syndromes of thrombotic microangiopathy. Med
Clin N Am 101 (2017) 395-415.
5. R.L. Gauer, M.M. Braun. Thrombocytopenia. Am Fam Physician. 2012 Mar 15;
85(6):612-622