In jedem Lebensalter ist aus Gesundheitsgründen eine moderate Dauerleistungsaktivität im Umfange von 150 Minuten pro Woche empfohlen. Im Pensionsalter kommt es aufgrund einer subklinischen Entzündungslage im Körper zu einem Muskelmasseverlust (Sarkopenie). Bis zum 80sten Lebensjahr wird die körperliche Leistungsfähigkeit dadurch in etwa halbiert. Es ist deswegen im Alter zum Erhalt der Muskelmasse indiziert, 2 – 3 mal wöchentlich, ein gezieltes Krafttraining aller Muskelgruppen der oberen und der unteren Extremität sowie der Rumpfmuskulatur durchzuführen. Dies sollte mit jeweils 10 – 15 erschöpfenden Kontraktionen geschehen. Die Gesundheitswirksamkeit des aeroben Trainings ist der Freisetzung von Zytokinen (Myokine oder Exerkine) aus der belasteten Muskulatur zuzuschreiben. Zum Muskelaufbau bedarf es zusätzlich eines Krafttrainings, welches einen gezielten mechanischen Reiz setzt, der im Dauerleistungstraining nicht erreicht wird.
It is generally accepted that 150 Minutes per week of moderate to intensive endurance activity has multiple health relevant benefits. Starting at retirement age a systemic low-grade inflammation leads to progressive muscle mass loss such that by age of 80, the physical performance capacity is practically halved. To reduce muscle loss a 2 – 3 times weekly strength training program is recommended including all major muscle groups of the upper and lower extremity as well as the trunk. Individual training sets should lead to exhaustion of the targeted muscles in 10 – 15 contractions. The health benefit of aerobic training is mediated by the release of cytokines (myokines or exerkines) from the activated muscles. Additional strength training is needed for muscle build-up or maintenance as endurance type training does not induce sufficient mechanical stress in activated muscles.
Key Words: Sarcopenia, muscle loss, elderly patients, training, muscle build-up
Leistungsfähigkeit im Alter
Es ist die allgemeine Erfahrung, dass unsere körperliche Leistungsfähigkeit mit dem Alter abnimmt. Allerdings stellen wir fest, dass der Abfall der Dauerleistungsfähigkeit, gemessen als maximal erreichbare Leistung auf dem Ergometer, bis zu einem Alter von 60 Jahren bescheiden ausfällt (1, 2). Nach 60 ist der Abfall allerdings steil; zwischen dem 60. und dem 80. Lebensjahr halbiert sich die aerobe Leistungsfähigkeit in etwa.
Als Hauptursache der Abnahme der körperlichen Leistungsfähigkeit mit dem Älterwerden ist vor allem die lineare, altersbedingte Abnahme der maximalen Herzfrequenz zu nennen (3). Dazu kommt der in höherem Alter zunehmende Verlust an Muskelmasse (Sarkopenie), welcher die Abnahme der Leistungsfähigkeit stark beschleunigt (4). Der Erhalt dieser Muskelmasse und die Bekämpfung der Sarkopenie sind der Fokus dieser kurzen persönlichen Darstellung. Es wird dabei versucht, praktische Trainingsempfehlungen mit den Mechanismen der altersbedingten Leistungseinschränkungen zu begründen.
Bewegungsempfehlungen
Für gesunde Erwachsene fordert das ACSM (American College of Sports Medicine) 150 Minuten moderate bis intensive (vigorous) körperliche Tätigkeit pro Woche (5). Diese Empfehlung ist unbestritten und gilt grundsätzlich für alle Erwachsenen und alle Lebensalter. Die Vorgaben für ältere Erwachsene sind im Copenhagen Consensus Statement 2019 Physical Activity and Ageing, zusammengefasst und erscheinen etwas weniger strikt (6). Man geht davon aus, dass sich bei Älteren die günstigen Auswirkungen körperlicher Aktivität bei niedrigeren Volumina und Intensitäten einstellen. Dabei hält das Copenhagen Consensus Statement zusätzlich fest, dass körperliche Tätigkeit nicht nur gegen zivilisatorische Erkrankungen wirkt, sondern auch den altersbedingten kognitiven Abbau verzögert und einen günstigen Einfluss auf Parkinson und Alzheimer nimmt.
Praktisch bedeutet dies für Menschen im Pensionsalter (65+), dass sie idealerweise fünfmal in der Woche über mindestens 30 Minuten körperlich aktiv sein sollten. Aufgrund der niedrigeren geforderten Intensitäten ist es nicht mehr notwendig zu joggen; es genügt ein etwas akzentuierter Spaziergang z.B. mit dem Hund. Die Sportart, die man sich auswählt, spielt für den Erhalt der Gesundheit keine Rolle und sollte aufgrund der persönlichen Präferenz gewählt werden. Schwimmen, Rudern und Radfahren sind dabei ebenso geeignet wie Wanderungen oder Ausflüge mit dem E-Bike oder allenfalls Yoga und Pilates. Im Alter geht es nicht mehr um «schweisstreibendes Training», sondern um bewusst genussreiches Bewegen, wobei mehr das Volumen als die Intensität im Vordergrund stehen sollte. Im Alter braucht es keinen aufwändigen Trainingsplan, wie er notwendig ist, wenn man seine Leistungsfähigkeit gezielt verbessern will. Man trainiert nicht mehr für die Verbesserung der Leistung, sondern für den Erhalt der Gesundheit und der Lebensqualität.
Eine ideale Alterssportart ist das Golfspiel. Dabei ist man in jeder Golfrunde 3–4 Stunden intermittierend, aber nie maximal körperlich aktiv. Für das Golfspiel spricht zusätzlich der Umstand, dass für jeden Golfschlag höchste geistige Konzentration, Koordination und ein gutes Gleichgewicht gefordert sind. Es kommen damit eine ganze Reihe komplexer, kognitiver Fähigkeiten ins Spiel. Golf betreibt man idealerweise in einer Gruppe von zwei bis maximal 4 Personen. In diesem Sinne kann Golf zum Erhalt der sozialen Integration beitragen. Jeder Golfclub betreibt für weibliche (Ladies) und männliche Senioren spezielle Seniorengruppen und reserviert dafür auch Spielzeiten und Turniere. Leider ist Golf teuer und stellt psychomotorisch ausserordentlich hohe Anforderungen. Golf lässt sich aber auch noch im Pensionsalter erlernen, wenn man gewillt ist, die damit verbundenen Frustrationen zu ertragen.
Es gibt also beliebig viele Möglichkeiten, auch im Alter körperliche Dauerleistungstätigkeiten in genügendem Umfange und mit Spass zu betreiben, insbesondere da einem im Alter normalerweise genügend Zeit dazu zur Verfügung steht.
Sarkopenie
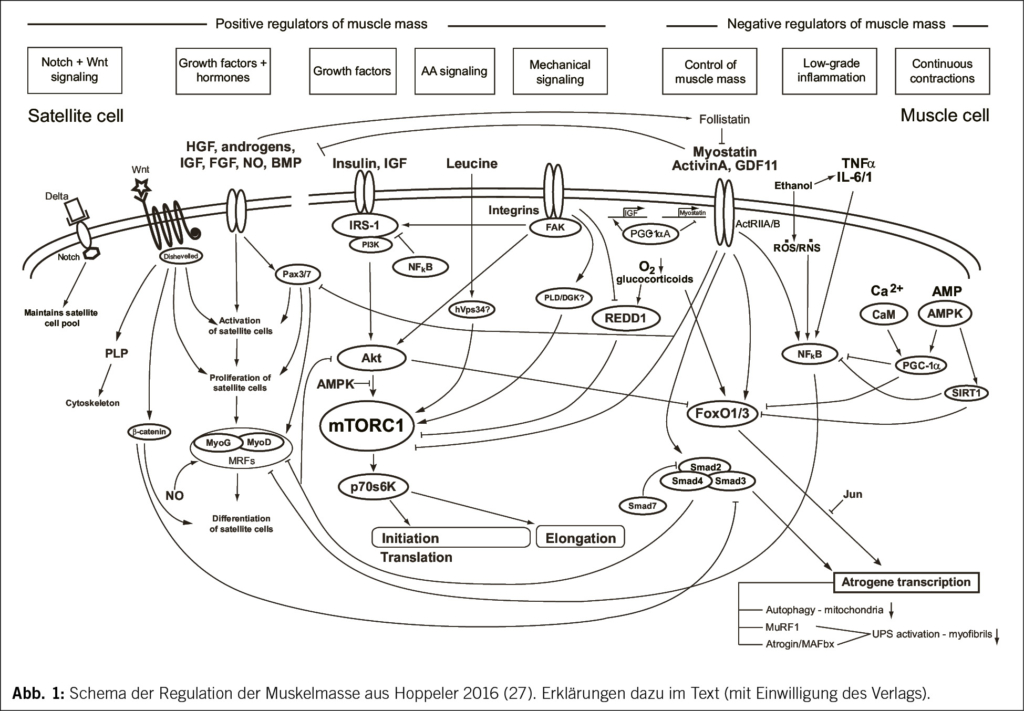
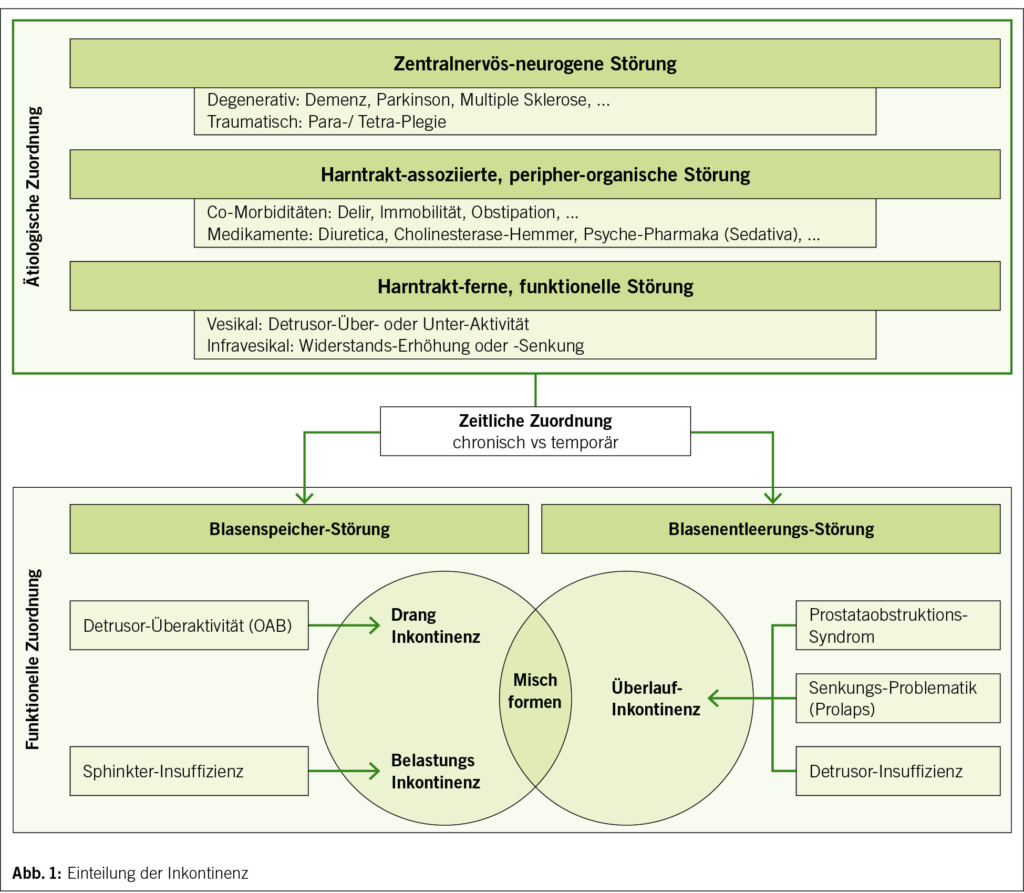
Mit den beschriebenen Tätigkeiten, auch wenn im erforderlichen Umfange betrieben, bleibt das Problem der Sarkopenie nur teilweise gelöst. Auch bei adäquater körperlicher Tätigkeit wird im Alter ein Verlust an Muskelmasse stattfinden und den Leistungszerfall beschleunigen. Der Begriff Sarkopenie wurde von Rosenberg (7) geprägt und bezeichnet im engeren Sinne den altersbedingten Verlust an Muskelmasse und Funktion. Rosenberg nennt als Ätiologie für Sarkopenie: Bewegungsarmut, vermehrtes Muskelfett, Insulin Resistenz, Verlust an Motoneuronen, verminderte Proteinaufnahme, erhöhtes Interleukin-6, Abnahme an Östrogen und Testosteron sowie verminderte Abgabe von Wachstumshormon (8). Die genannte Ätiologie benennt damit im Wesentlichen die bekannten positiven und negativen Regulatoren der Muskelmasse (Abb. 1).
Zentral wird die Muskelmasse durch den molekularen Effektor mTorc geregelt. Dabei ist mTorc für die translatorische Steuerung der Synthese der muskulären und anderer Proteine verantwortlich. Mechanischer Reiz und anabole Hormone scheinen einen dominanten Reiz auf das Wachstum der Muskelzelle zu haben. Wobei mechanischer Reiz kombiniert mit anabolen Hormonen besonders wirksam ist (9). Auch Insulin und Wachstumshormon gehören zu den wesentlichen positiven Regulatoren der Muskelmasse, dabei nimmt die Belastung der Muskulatur selbst einen wesentlichen Einfluss auf die Sekretion der genannten Hormone und Wachstumsfaktoren (10). Als weiterer kritischer Faktor für Muskelwachstum und Muskelerhalt ist die ausreichende Zufuhr von Proteinen über die Nahrung – dabei ist die Aminosäure Leucin der molekular relevante Effektor.
Der dominante negative Regulator der Muskelmasse ist das Myostatin, ein Mitglied der TGF-beta (transforming growth factor-beta) Superfamilie. Wird Myostatin in Mäusen ausgeschaltet, so entwickeln diese eine Muskelhypertrophie im Bereich einer zwei- bis dreifachen Zunahme der Masse individueller Muskeln (11). Der naheliegende klinische Einsatz von Myostatin-Antagonisten oder ähnlich wirkenden pharmakologischen Interventionen zur Bekämpfung der Sarkopenie scheint aber vorderhand noch ausser Reichweite (12). Als Therapien erster Wahl gelten deswegen körperliche Aktivität (vor allem Krafttraining) und die alimentäre Unterstützung (im Fokus steht die Protein Supplementierung).
Weitere wichtige negative Regulatoren der Muskelmasse sind Glucocorticoide und Hypoxie. Der Glucocorticoid induzierte Muskelmasseverlust muss als Kollateralschaden der Therapie mit Glucocorticoiden als Entzündungshemmer in rheumatischen Erkrankungen oder im Rahmen von Krebstherapien gesehen werden. Beim Muskelmasseverlust durch Hypoxie spielt es keine Rolle, ob die systemische Hypoxie aufgrund eines lange währenden Aufenthalts in grosser Höhe besteht oder durch COPD verursacht wird.
In den Vordergrund des klinischen Interesses ist in der letzten Zeit die durch eine chronische Entzündungslage im Organismus hervorgerufene Sarkopenie gerückt (13). Alterungsprozesse an der Mitochondrienpopulation, speziell in der Muskulatur, scheinen dabei besonders bedeutend. Verantwortlich sind Fehler im mitochondrialen Proteinmetabolismus, der mitochondrialen Biogenese und der Autophagie (14). Man geht davon aus, dass für die mitochondriale Dysfunktion vor allem für eine Anhäufung von Sauerstoffradikalen (ROS) verantwortlich ist. Dadurch kommt es zu einer Entzündungslage in der Muskulatur. Betroffen ist aber nicht nur die Muskulatur, das grösste Organ unseres Körpers, sondern alle Organsysteme. Diese altersbedingte Entzündungslage im Organismus wird mit dem Begriff «Inflammaging» belegt (15). Inflammaging wird als Hauptgrund für die altersbedingte Sarkopenie angesehen (16).
Myokine, Exosomen und Inflammaging
Über die letzten 20 Jahre konnte etabliert werden, dass der aktivierte Muskel als endokrines Organ funktioniert und eine Vielzahl von kleinen Peptiden (Zytokine) freisetzt, welche als Myokine bezeichnet werden. Die Myokine dienen primär der Kommunikation zwischen den Organen (organ crosstalk, (17)). Es ist ebenfalls etabliert, dass viele, der durch den aktiven Muskel freigesetzten Zytokine, eine anti-inflammatorische Aktivität besitzen (18). Der aktive Muskel setzt aber nicht nur Zytokine, sondern auch sogenannte Exosomen frei (19). Exosomen sind Mikrovesikel, welche die genannten Myokine enthalten, daneben aber auch verschiedene Nukleinsäuren wie, microRNA, messenger RNA und mitochondriale DNA. Der Inhalt dieser Exosomen soll für die multisysteme Wirkung von körperlicher Aktivität verantwortlich sein. Dies beinhaltet einerseits multiple, günstige metabole Anpassungen im Organismus, als auch die Verminderung des Risikos für Inaktivität assoziierte Erkrankungen wie Arteriosklerose, kardiovaskuläre Erkrankungen, einige Krebsarten, Osteoarthritis, Obesitas, metaboles Syndrom, Diabetes 2 und Depression. Safdar und Tarnopolski (19) schlagen deswegen den Begriff «Exerkine» für die Gesamtheit der durch Muskeltätigkeit freigesetzten Exosomen vor. Regelmässige körperliche Aktivität ist damit anerkanntermassen der wichtigste modifizierbare Faktor in der Ätiologie der genannten Erkrankungen. Einen wesentlichen Anteil der günstigen Wirkung der regulären, körperlichen Aktivität wird dabei deren anti-inflammatorischen Effekt zugeschrieben (20).
Tatsächlich kann man mit 150 Minuten moderater Aktivität pro Woche die wesentlichen positiven Effekte auf die multiplen «zivilisatorischen» Erkrankungen erreichen. Wir können davon ausgehen, dass die Muskelmasse bis circa ins Pensionsalter ohne zusätzliche Massnahmen erhalten bleibt. Es ist offensichtlich, dass der ab dem 60. –65. Lebensjahr beschleunigt, auftretende Verlust an Leistungsfähigkeit vor allem dem in den Vordergrund tretenden Muskelabbau zuzuschreiben ist. Wir müssen deswegen in dieser Altersgruppe spezifische Massnahmen zum Erhalt der Muskelmasse ins Auge fassen.
Krafttraining im Alter
Die von der ACSM und vom Copenhagen Consensus Statement vorgeschlagenen 150 Minuten körperlicher Tätigkeit kann als Dauerleistungsbelastungen charakterisiert werden. Dabei wird eine grössere Muskelmasse bei einem Bruchteil der maximal möglichen Leistung über längere Zeit belastet. Dies führt zu einem Anstieg der Atmung und Herzfrequenz, weil der Energiebedarf aerob gedeckt werden muss. Die Wirkung der Belastung ist damit systemisch. Die mechanische Belastung der einzelnen, an der Bewegung beteiligten Muskeln bleibt allerdings gering. Dauerleistungstraining führt also per se nicht zu einer Zunahme der Muskelmasse der belasteten Muskeln oder deren Kraft, sondern nur zu einer Verbesserung der Leistungsfähigkeit des Gesamtorganismus (21).
Ist das Ziel einer Belastung die Vergrösserung des Muskelquerschnitts oder der Kraft, muss dazu eine Form von Krafttraining gewählt werden. Beim Krafttraining werden Muskelgruppen mit wenigen, fast maximalen Belastungen bis zur Erschöpfung ausgelastet. Ein Satz (oder Set) beschreibt dabei eine Einheit aus mehreren nacheinander ausgeführten Wiederholungen derselben Bewegung. Steht der Gewinn an Muskelmasse im Vordergrund (Hypertrophie Training), wird die Belastung so gewählt, dass mit 8 –12 Wiederholungen eine vollständige Ausbelastung erfolgt. Das ACSM empfiehlt in seinen Guidelines für ältere und gebrechliche (frail) Personen 10 –15 Wiederholungen (22). Sind in einem Set 15 Wiederholungen möglich – kann das Gewicht bzw. die Belastung erhöht werden. Dabei wird die Einzelbelastung in einem Set auf die maximal mögliche Belastung in einer Einzelkontraktion bezogen. Diese Belastung wird als 1RM bezeichnet. Bei Hypertrophie Training wird typischerweise mit Belastungen von 65 bis 85 % von 1RM trainiert.
Im Krafttraining gibt es unendlich viele Varianten eines effektiven Trainings zum Gewinn oder Erhalt von Muskelmasse und Kraft (23). Man kann mit freien Gewichten trainieren oder an Kraftmaschinen, man kann das eigene Körpergewicht zum Training verwenden oder an elektronisch kontrollierten Maschinen, welche den Widerstand in beide Richtungen der Bewegung variieren können. Die Art und Weise des Krafttrainings spielt vermutlich eine geringe Rolle – Hauptsache man trainiert 2–3 mal in der Woche und vermeidet dabei häufig gemachte Fehler. In einer Metaanalyse von 47 Studien zeigt Peterson (23) an einer Population von 1047 über 50-Jährigen einen Kraftzuwachs in vier Muskelgruppen von 24 % bis 33 % bei zwei bis drei Trainings pro Woche, einer Trainingsdauer von 6 bis 24 Wochen und einer Belastung von 40 % bis 80 % von 1RM. Dieses erstaunliche Resultat zeigt, dass eigentlich jegliches Krafttraining, unabhängig von der gewählten Modalität, effektiv ist.
Hinweise zum effektiven Training im Älterwerden
Sinnvollerweise kombiniert man ab einem Alter von 60–65 Jahren Dauerleistungstraining nach Vorgaben des Copenhagen Consensus Statements mit zwei Krafttrainingseinheiten. Letztere sollten an nicht konsekutiven Tagen stattfinden. Es liegen zurzeit noch keine gesicherten Daten dazu da, inwieweit dabei die Krafttrainingseinheiten die Dauerleistungseinheiten in Bezug auf die Exerkin Produktion ersetzen können. Wir dürfen aber davon ausgehen, dass auch im Krafttraining Exerkine in ähnlichem Umfange freigesetzt werden wie im Dauerleistungstraining (24).
Beim Krafttraining sollte auf ein vernünftiges Aufwärmen der zu trainierenden Muskulatur geachtet werden. Dazu eignen sich für die untere Extremität mindestens 10 Minuten auf dem Fahrradergometer bei leichter Belastung (50 –100 Watt). Für die obere Extremität wäre ein Oberkörperergometer ideal. Man kann die Oberkörpermuskulatur aber auch mit einem Cross-Trainer oder mit einer Rudermaschine für mindestens 10 Minuten aufwärmen.
Bei älteren Erwachsenen empfiehlt sich die Verwendung von Krafttrainingsgeräten. Training mit freien Gewichten ist koordinatorisch wesentlich anspruchsvoller und sinnvollerweise nur dann zu wählen, wenn schon Erfahrung im Training mit freien Gewichten besteht. Koordinatorische Aspekte sollten im Alter eher mit separaten Koordinationsübungen geübt werden. Zur Festlegung der Belastungen in den einzelnen Übungen sollte man die Hilfe des Personals des Trainingszentrums in Anspruch nehmen. Damit wird auch sichergestellt, dass die Ausführung der einzelnen Übungen korrekt erfolgt und auf richtiges Atmen geachtet wird.
Eine Trainingseinheit sollte alle grösseren Muskelgruppen der oberen und der unteren Extremität umfassen. Es ist darauf zu achten, dass auch die Rumpfmuskulatur, besonders die Rumpfrotation, in den gewählten Übungen zum Zuge kommt. Insgesamt ergeben sich dadurch etwa 10 –12 Übungen. Bei der Auswahl der Übungen ist darauf zu achten, dass mono artikuläre Übungen (z.B. reine Knieextension oder Knieflexion) ungünstig sind, weil bei diesen Übungen die Gelenkbelastungen höher sind als bei Übungen in einer sogenannten «geschlossenen» Muskelkette (z.B. der Beinpresse). Mono artikulare Übungen sind vor allem dann abzulehnen, wenn degenerative Gelenkerkrankungen vorliegen.
Im Gegensatz zu der häufig propagierten Ansicht, zwei bis drei Sets (also Wiederholungen einer Übung) zu machen, genügt gerade im Alter ein einzelnes Set vollständig (25, 26). Wenn nicht maximaler Muskelmasse- oder Kraftgewinn im Vordergrund steht, scheint es sinnvoller zu sein, die Trainingszeit auf eine grössere Anzahl verschiedener Übungen zu verteilen.
Die Datenlage für die gesundheitlichen Vorteile vermehrter körperlicher Aktivität in allen Lebensaltern ist erdrückend. Es besteht ein weitestgehender Konsens, dass dazu 150 Minuten körperliche Dauerleistungstätigkeit von moderater Intensität genügt. Aufgrund der im Alter zunehmend wichtiger werdenden Sarkopenie und dem damit assoziierten Muskelmasseverlust ist es dringend geraten, ab 60–65 Jahren mindestens zwei Trainingseinheiten Krafttraining an nicht konsekutiven Wochentagen in den individuellen Lebensplan einzubauen.
Copyright
Aerzteverlag medinfo AG
Universität Bern, Institut für Anatomie
Baltzerstrasse 2
3012 Bern
Physiotherapie und Osteopathie
Hühnerbühlrain 40
3065 Bolligen
Die Autoren haben keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Farazdaghi GR. and Wohlfart B. Reference values for the physical work capacity on a bicycle ergometer for women between 20 and 80 years of age. Clin Physiol. 2001 Nov;21(6):682-7.
2. Wohlfart B. and Farazdaghi GR. Reference values for the physical work capacity on a bicycle ergometer for men – a comparison with a previous study on women. Clin Physiol Funct Imaging. 2003 May;23(3):166-70.
3. Birnbaumer P., Traninger H., Borenich A., Falgenhauer M., Modre-Osprian R., Harpf H. and Hofmann P. Heart Rate Performance Curve Is Dependent on Age, Sex, and Performance. Front Public Health. 2020 Apr 2;8:98.
4. Keller K. Sarcopenia. Wien Med Wochenschr. 2019 May;169(7-8):157-172.
5. Garber CE., Blissmer B., Deschenes MR., Franklin BA., Lamonte MJ., Lee IM., Nieman DC. and Swain DP. American College of Sports Medicine position stand. Quantity and quality of exercise for developing and maintaining cardiorespiratory, musculoskeletal, and neuromotor fitness in apparently healthy adults: guidance for prescribing exercise.
American College of Sports Medicine. Med Sci Sports Exerc. 2011 Jul;43(7):1334-59
6. Bangsbo J., Blackwell J., Boraxbekk CJ., Caserotti P., Dela F., Evans AB., Jespersen AP., Gliemann L., Kramer AF., Lundbye-Jensen J., Mortensen EL., Lassen AJ., Gow AJ., Harridge SDR., Hellsten Y., Kjaer M., Kujala UM., Rhodes RE., Pike ECJ., Skinner T, Skovgaard T., Troelsen J., Tulle E., Tully MA., van Uffelen JGZ. and Viña J. Copenhagen Consensus statement 2019: physical activity and ageing. Br J Sports Med. 2019 Jul;53(14):856-858.
7. Rosenberg IH. Epidemiologic and methodologic problems in determining nutritional status of older persons. Proceedings of a conference. Albuquerque, New Mexico, October 19-21, 1988, Am J Clin Nutr, 1989 Nov;50(5 Suppl):1121-235.
8. Rosenberg IH. Sarcopenia: origins and clinical relevance. Clin Geriatr Med. 2011 Aug;27(3):337-9.
9. Bhasin S., Storer TW., Berman N., Callegari C., Clevenger B., Phillips J., Bunnell TJ., Tricker R., Shirazi A andCasaburi R. The effects of supraphysiologic doses of testosterone on muscle size and strength in normal men. N Engl J Med. 1996 Jul 4;335(1):1-7.
10. Hackney AC and Lane AR. Exercise and the Regulation of Endocrine Hormones.
Prog Mol Biol Transl Sci. 2015;135:293-311.
11. McPherron AC., Lawler AM and Lee SJ. Regulation of skeletal muscle mass in mice by a new TGF-beta superfamily member.Nature. 1997 May 1;387(6628):83-90.
12. Rolland Y., Dray C., Vellas B. and Barreto PS. Current and investigational medications for the treatment of sarcopenia. Metabolism. 2023 Dec;149:155597.
13. Daussin FN., Boulanger E. and Lancel S. From mitochondria to sarcopenia: Role of inflammaging and RAGE-ligand axis implication. Exp Gerontol. 2021 Apr;146:111247.
14. Picca A., Calvani R., Leeuwenburgh C., Coelho-Junior HJ., Bernabei R., Landi F. and Marzetti E. Targeting mitochondrial quality control for treating sarcopenia: lessons from physical exercise. Expert Opin Ther Targets. 2019 Feb;23(2):153-160.
15. Franceschi C., Garagnani P., Parini P., Giuliani C and Santoro A. Inflammaging: a new immune-metabolic viewpoint for age-related diseases. Nat Rev Endocrinol. 2018 Oct;14(10):576-590.
16. Liang Z., Zhang T., Liu H., Li Z., Peng L., Wang C and Wang T. Inflammaging: The ground for sarcopenia? Exp Gerontol. 2022 Oct 15;168:111931.
17. Severinsen MCK and Pedersen BK. Muscle-Organ Crosstalk: The Emerging Roles of Myokines. Endocr Rev. 2020 Aug 1;41(4):594-609.
18. Pinto A., Di Raimondo D., Tuttolomondo A., Buttà C., Milio G and Licata G. Effects of physical exercise on inflammatory markers of atherosclerosis. Curr Pharm Des. 2012;18(28):4326-49.
19. Safdar A and Tarnopolsky MA. Exosomes as Mediators of the Systemic Adaptations to Endurance Exercise. Cold Spring Harb Perspect Med. 2018 Mar 1;8(3):a029827.
20. Malandish A and Gulati M. The impacts of exercise interventions on inflammaging markers in overweight/obesity patients with heart failure: A systematic review and meta-analysis of randomized controlled trials. Int J Cardiol Heart Vasc. 2023 Jun 27;47:101234.
21. Steiner R., Meyer K., Lippuner K., Schmid JP., Saner H and Hoppeler H. Eccentric endurance training in subjects with coronary artery disease: a novel exercise paradigm in cardiac rehabilitation? Eur J Appl Physiol. 2004 May;91(5-6):572-8.
22. Liguori G. ACSM‘s Guidelines for Exercise Testing and Prescription. AMERICAN COLLEGE OF SPORTS MEDICINE (ACSM), Walters Kluwer, 11the edition, 2023, ISBN/ISSN: 9781975226480.
23. Peterson MD., Rhea MR., Sen A and Gordon PM. Resistance exercise for muscular strength in older adults: a meta-analysis. Ageing Res Rev. 2010 Jul;9(3):226-37.
24. Zunner BEM., Wachsmuth NB., Eckstein ML., Scherl L., Schierbauer JR., Haupt S., Stumpf C., Reusch L and Moser O. Myokines and Resistance Training: A Narrative Review. Int J Mol Sci. 2022 Mar 23;23(7):3501.
25. Radaelli R., Wilhelm EN., Botton CE., Rech A., Bottaro M., Brown LE and Pinto RS. Effects of single vs. multiple-set short-term strength training in elderly women. Age (Dordr). 2014;36(6):9720.
26. Polito MD., Papst R and Goessler K. Twelve weeks of resistance training performed with different number of sets: Effects on maximal strength and resting blood pressure of individuals with hypertension. Clin Exp Hypertens. 2021 Feb 17;43(2):164-168.
27. Hoppeler H. Molecular networks in skeletal muscle plasticity. J Exp Biol. 2016 Jan;219(Pt 2):205-13.