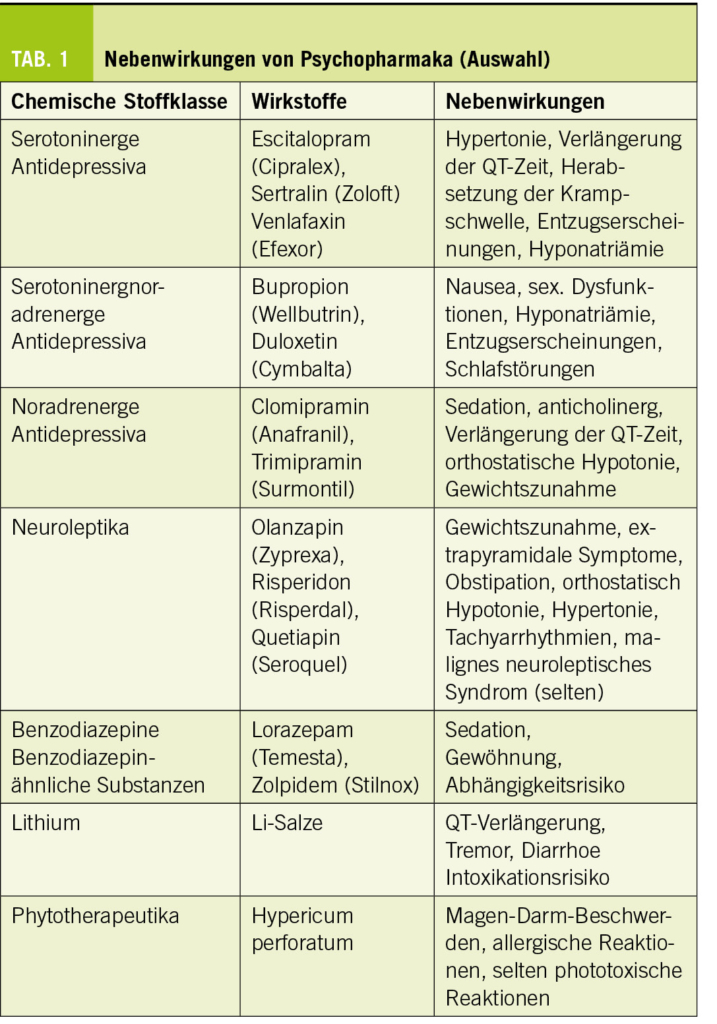
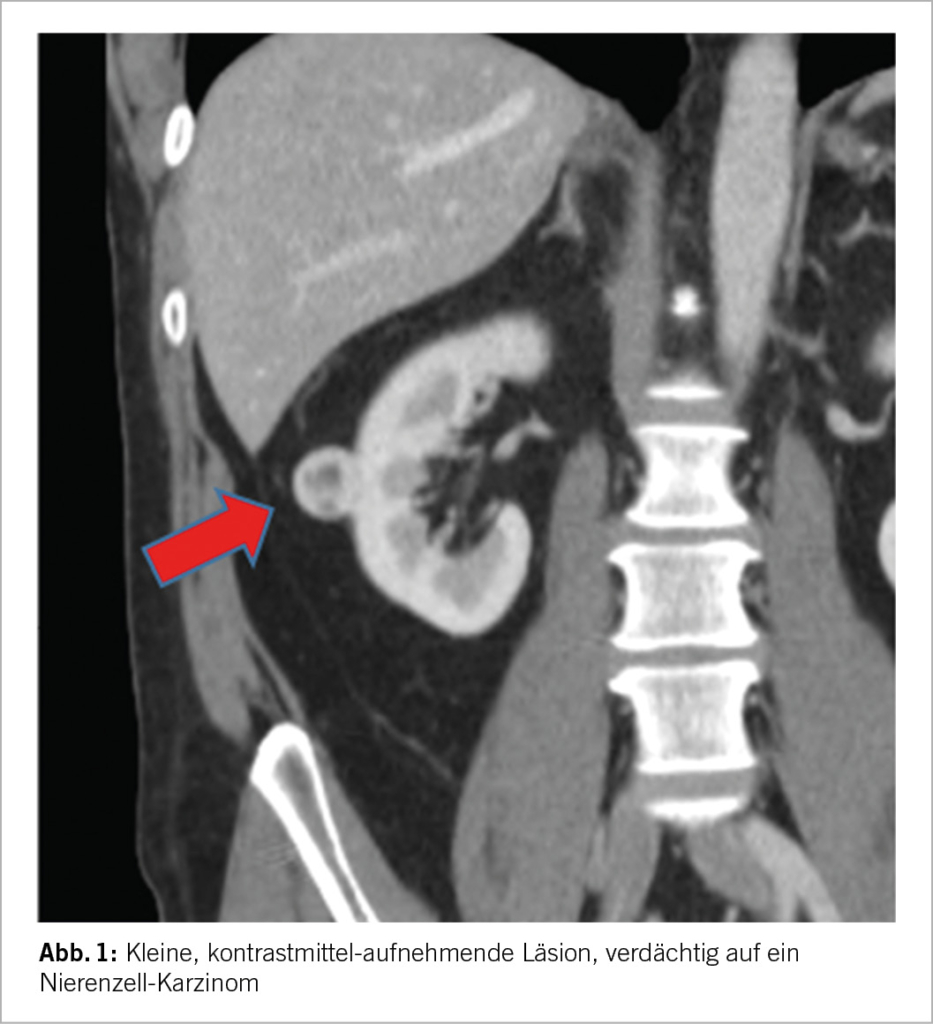
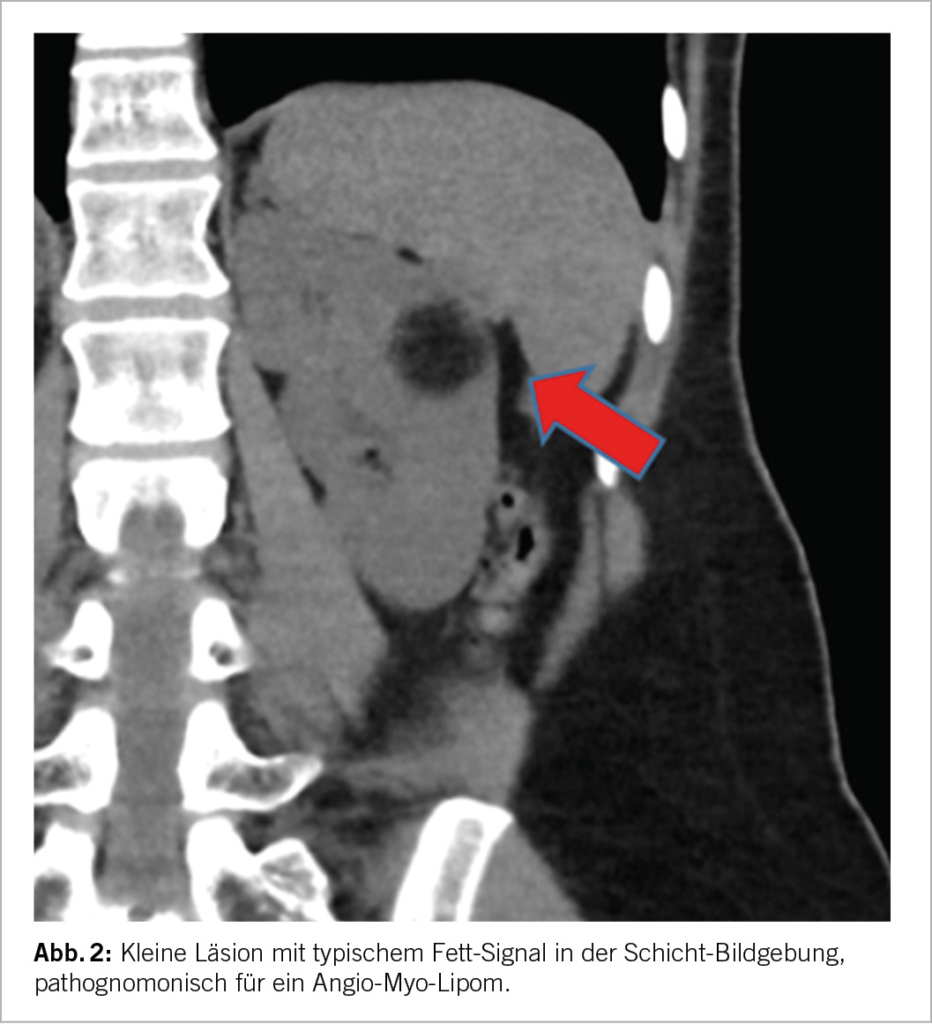
Eine erhebliche Anzahl von Menschen leiden an depressiven Erkrankungen, an pathologischen Ängsten, zeigen psychosomatische Symptome, haben chronische Schlafprobleme oder sind psycho-physisch erschöpft. Sie suchen oft zuerst in der hausärztlichen Praxis medizinische Hilfe. Hausärzte sind also jeden Tag mit psychisch beeinträchtigten Patienten konfrontiert und müssen dann handeln. Umso wesentlicher ist eine Grundkompetenz betreffend die unterschiedlichen Psychopharmaka und deren gezielten Einsatz, aber auch das Wissen über deren therapeutische Limitationen. Psychopharmaka können in Zeiten des vermeintlichen Neurobiologie-Hype jedoch eine gute, vertrauensvolle Beziehung zwischen Arzt und Patient nie ersetzen. Sie sind in der anspruchsvollen Behandlung von psychisch erkrankten Patienten als Ergänzung zu bewerten.
A considerable number of people suffer from depressive disorders, pathological anxiety, show psychosomatic symptoms, have chronic sleep problems or are psycho-physically exhausted and often first seek medical help in the GP’s practice. GPs are therefore confronted with psychologically impaired patients every day and must then act. This makes it all the more important for them to have a basic knowledge of the various psychotropic drugs and their targeted use, but also to know about their therapeutic limitations. Even in times of supposed neurobiology hype, psychopharmaceuticals can never replace a good, trusting relationship between doctor and patient. They are to be seen as a supplement in the demanding treatment of mentally ill patients.
Allgemeine Aspekte der Behandlung mit Psychopharmaka
Psychiatrische Erkrankungen schwererer Ausprägung führen im Vergleich zu vielen somatischen Krankheiten in höherem Masse zu dauerhaften Beeinträchtigungen und zu einer verkürzten Lebenserwartung. Sie stellen daher hohe Anforderungen an den Behandler. Viele Patienten mit psychischen Leiden finden sich zuerst beim Hausarzt ein. Meistens sind es Menschen mit depressiven Symptomen oder sie klagen über pathologische Ängste, da diese beiden psychischen Erkrankungen unverändert die Rangliste der psychischen Erkrankungen anführen. Vor allem bei depressiven Störungen ist die Diagnostik zuweilen schwierig, da Patienten ihre beeinträchtigte Psyche nicht unmittelbar thematisieren. Oder sie können die Beschwerden nicht in Verbindung mit psychischen Prozessen bringen und berichten allein über körperliche Probleme. Der Hausarzt hat nicht selten den Vorteil, den Patienten schon länger zu kennen, kann Veränderungen in dessen Verhalten und Reaktionen ansprechen und die Symptomatik erklärbar machen. Wenn keine Zuweisung an den Psychiater erfolgt, kommt die Therapieverantwortung alleine bei ihm zu liegen. Er spielt somit eine wichtige Rolle bei der Ersterkennung, der Triage und der Behandlung von psychischen Störungen und ebenso bei der Verschreibung und Verwaltung von Psychopharmaka.
In Deutschland verschreiben die Hausärzte ein Drittel der Psychopharmaka, in den USA sind es Dreiviertel der Antidepressiva, die nicht von Psychiatern, sondern von Allgemeinärzten, Pädiatern oder Gynäkologen verordnet werden. Und die Zahlen des Psychopharmaka-Absatzes nehmen stetig zu, v.a. die der Antidepressiva, der Tranquilizer, der Neuroleptika und auch die von Methylphenidat. In der Schweiz nehmen laut Daten der Krankenkassen ca. 20 Prozent aller Versicherten eine Form von Psychopharmaka ein, die zur Hälfte von Hausärzten und zu 30 Prozent von Psychiatern verordnet werden. Die zunehmende Verschreibungspraxis von Psychopharmaka wird von der Ärzteschaft, den Krankenkassen, den Patienten und Patientenorganisationen zwar immer wieder kritisch bewertet, ohne dass sich hierdurch bis heute positive Veränderungen ergeben hätten. Psychopharmaka sollten immer sehr präzise und zeitlich begrenzt zur Anwendung kommen und der Patient muss während der Behandlung durch den verschreibenden Arzt regelmässig begleitet werden. Die alleinige medikamentöse Therapie von psychischen Erkrankungen ist einer Kombination mit medizinischer Psychotherapie unterlegen und ist grundsätzlich weder sinnvoll noch als zielführend zu betrachten. Psychopharmaka sind in der Psychiatrie und Psychotherapie therapeutisch bedeutsam, jedoch ist deren alleiniges Wirkungsspektrum begrenzt. Die Vorstellung, dass durch ihren Einsatz die einer psychischen Störung zugrundeliegenden Probleme gelöst werden können, greift zu kurz. Ohne eine vertiefte und kompetente Abklärung mit Analyse der hoch relevanten psycho-sozialen inkl. beruflichen Situation, bleibt der Einsatz von Psychopharmaka problematisch. Darüber hinaus sind deren Wirkung und Nebenwirkungen gegeneinander abzuwägen und Alternativbehandlungen und Selbsthilfemassnahmen in der Therapiestrategie zu berücksichtigen.
Die biologische Ausrichtung der Psychiatrie und die Neurowissenschaft versuchen ein Bild von psychischen Störungen zu etablieren, dass wenn die Psyche leidet, einfach das Gehirn krank sein soll. Es stellen sich somit in Verbindung mit dem heutigen generellen Anspruch des „Quick-fix“ für den Hausarzt wichtige Fragen der adäquaten bzw. kritischen Anwendungspraxis von Psychopharmaka: Wann also sollen Psychopharmaka zum Einsatz kommen? Welche Qualität von psychischen Störungen rechtfertigen eine medikamentöse Behandlung? Welcher Patient profitiert und was sind mögliche negativen Auswirkungen der zur Anwendung gelangenden Medikamente?
Antidepressiva
Die Datenlage hinsichtlich des Nutzens von Antidepressiva ist widersprüchlich. Antidepressive Medikamente mit neuem Wirkmechanismus, rascher Wirksamkeit und weniger Nebenwirkungen sind keine in Sicht. Neue Studien zeigen, dass sich die Mehrheit der untersuchten Antidepressiva zwar überzufällig von Placebo unterscheiden, also eine Wirkung aufweisen, jedoch in der Effektstärke sehr schwach bleiben. Die Effekte sind so gering, dass davon ausgegangen wird, dass 90 Prozent der Wirkung von Antidepressiva auf PIaceboeffekten beruhen. Trotzdem können Patienten von Antidepressiva profitieren, auch wenn wir bis heute nicht wissen wie und weshalb. Die Monoamin-Hypothese, also, dass allein eine erniedrigte Serotonin- oder Noradrenalin-Konzentration für die Auslenkung der Grundstimmung verantwortlich sein soll, lässt sich
auch aufgrund neuester Untersuchung nicht halten. Eine lineare neurobiologische Kausalität zwischen Antidepressiva und der Verbesserung des psychischen Gesundheitszustandes bestand wohl noch nie, deren teilweise erzielter thymoleptische Effekt bleibt ungeklärt.
Für leichte und mittelschwere depressive Zustände gelten Antidepressiva heute denn auch nicht mehr als dringend indiziert. Sie sind durch medizinische Psychotherapie erfolgreich behandelbar. Antidepressiva kommen jedoch bei ausgeprägter depressiver Symptomatik als aktivierende (SSRI bzw. SNRI) oder sedierende Antidepressiva (z.B. Trazodon (Trittico), Mirtazapin (Remeron) oder Trizyklika) zum Einsatz. SSRI sind darüber hinaus bei Angststörungen indiziert und mit sedierenden Antidepressiva, die stärker auf die Histamin-Rezeptoren einwirken, können auch oft lange vorbestehende Schlafprobleme angegangen werden. Hierbei sind die konsekutive eingeschränkte Fahrtauglichkeit und Sturzgefahr zu beachten. SSRI werden zudem auch bei Zwangsstörungen und chronischen Schmerzsyndromen angewendet. Das Serotonin-Syndrom unter SSRI ist selten und kann bei Kombination mit Triptan, Opioiden oder bei gleichzeitiger Gabe von anderen Antidepressiva auftreten. Es existiert aufgrund der oben dargestellten Unsicherheiten betreffend dem Wirkmechanismus von Antidepressiva keine massgeschneiderte Medikationsoption für einen bestimmten Patiententypus. Deren Einsatz bleibt von der individuellen Verträglichkeit, dem Vorliegen von Komorbiditäten und den eigenen Erfahrungen des Behandlers abhängig. In der hausärztlichen Praxis reichen wenige Präparate aus, die man jedoch gut kennen sollte. Antidepressiva sollen immer aufdosiert (Probesdosis) und nach anhaltender Stabillisierung des psychischen Gesundheitszustandes aufgrund möglicher Entzugserscheinungen immer langsam abgesetzt werden. Phytotherapeutika (Hypericum perforatum) sind bei mittelschwerer Ausprägung synthetischen Antidepressiva ebenbürtig und können dem Patienten als erste Wahl angeboten werden, da ihre Nebenwirkungen und das Interaktionsrisiko geringer sind. Ketamin ist seit 2020 als Antidepressivum in der Schweiz nur für therapieresistente Depressionen zugelassen und wird als Nasenspray und i.v. angewendet. In den letzten Jahren werden Neuroleptika auch bei depressiven Störungen ohne psychotische Symptome als Augmentationstherapie sowie bei Schlafstörungen eingesetzt. Die Indikation erscheint aufgrund des oft ungenügenden Benefits für die Patienten und v.a. wegen der Nebenwirkungen fraglich.
Bei rezidivierenden depressiven Erkrankungen ist Lithium unverändert der Moodstabilizer der Wahl, sein Wirkmechanismus ist nicht bekannt. Das Aufdosierungsschema ist genau zu befolgen und die regelmässigen Blutkontrollen gemäss Hersteller einzuhalten. Der therapeutische Bereich ist eng (Kardiotoxizität) und der Pat. muss hierzu wie auch über die übrigen möglichen Nebenwirkungen und das Zeitintervall (12 Stunden) zwischen der letzten Li-Einnahme und der Blutentnahme informiert werden.
Neuroleptika
Es existiert eine Vielzahl von Neuroleptika und deren Auswahl fällt ebenfalls nicht leicht. Sie sind antipsychotisch, sedierend und lindern die psychomotorische Unruhe. Sie kommen p.o. oder i.m. Depot bei psychotischen Symptomen im Rahmen einer Schizophrenie oder einer major depression, als Phasenprophylaxe bei bipolaren Störungen, bei akuten manischen Episoden und bei Erregungszuständen von schizophrenen und manischen Patienten i.m. akut zur Anwendung. Sie wirken auf unterschiedliche Dopamin-, Serotonin- und Histamin-Rezeptoren und sollen v.a. über ihren D2-Antagonismus zu einer Normalisierung der Hirnaktivität führen. Bei Latuda ist der Wirkmechanismus unbekannt, bei Reagila soll die Wirkung über einen partiellen D3- bzw. D2-Rezeptor-Agonismus erzielt werden. Eine deutlich bessere Wirksamkeit der neuen Präparate im Vergleich zu den klassischen Neuroleptika wurde in Studien bis heute nicht nachgewiesen. Antipsychotika der neuen Generation (z.B. Risperidon, Olanzapin, Quetiapin) werden aber als besonders wirksam gegen die Negativsymptomatik bei Schizophrenie propagiert. So besteht eine ähnliche Situation wie bei den Antidepressiva: Der Vorteil neuerer Präparate zeigt sich vorwiegend in deren teilweise günstigerem Nebenwirkungsprofil z.B. hinsichtlich Gewichtszunahme, Spätdyskinesien, Akathisie, Obstipation, orthostatische Hypotonie, Hypertonie und Tachyarrhythmien. Auch bei den Neuroleptika gilt es, wenige Präparate, deren Nebenwirkungen und mögliche Interaktionen gut zu kennen und auf die adäquate Dosierung zu achten. Untersuchungen haben gezeigt, dass durch eine Besetzung der Dopamin-Rezeptoren von 60-65 Prozent eine gute antipsychotische Wirkung erzielt wird und ab 80 Prozent v.a. die extrapyramidalen Nebenwirkungen stark zunehmen. Somit kann die Dosierung von Neuroleptika entsprechend niedrig gehalten werden (z.B. 2-6mg Risperdal, 5-20mg Zyprexa). Beim Einsatz von Neuroleptika aufgrund starker Unruhe und vorbestehendem kognitiven Defizit ist bei älteren Menschen Vorsicht geboten. Bei nächtlicher Unruhe älterer Patienten widerspiegeln Neuroleptikaverordnungen leider nur allzu oft den zu beklagenden Personalmangel in den Institutionen. Externe Sitzwachen sind hier als Alternative oft sinnvoller und zu diskutieren. Auch nur kurzfristig eingesetzte Neuroleptika können zudem eine dementielle Entwicklung beschleunigen.
Benzodiazepine
Nach den Antidepressiva gelten Benzodiazepine als die am zweithäufigsten verordneten Psychopharmaka. Sie kommen bei psychiatrischen Erkrankungen als Anxiloytika/Sedativa und Hypnotika zum Einsatz. Aufgrund ihres raschen Wirkungseintritts über die allosterische (nicht kompetitive) Bindung an den GABA-A-Rezeptor und der guten therapeutischen Breite werden sie oft zu lange, nicht selten über Jahre verordnet, was zu kognitiven Defiziten und zu low-dose-Abhängigkeiten führt. Da Benzodiazepine neben ihrem anxiolytischen, beruhigend-sedierenden, schlafanstossenden und krampflösenden Effekt auch muskelrelaxierend sind, steigt v.a. bei älteren Patienten das Sturzrisiko. Benzodiazepine sind mit Antidepressiva und Neuroleptika kombinierbar. Jedoch ist auf die Potenzierung der sedativen Wirkung hinzuweisen, insbesondere, wenn gleichzeitig Alkohol oder anderweitige psychotrope Substanzen konsumiert werden. Auch besteht bei einigen Präparaten die Möglichkeit der Wirkstoffkumulation, wobei bei Xanax und Temesta keine entsprechenden Effekte, hingegen bei Valium und Rivotril solche nachweisbar sind. Das Absetzen von Benzodiazepinen bei körperlicher Abhängigkeit führt zu Entzugssymptomen (cave Entzugsanfall) und sollte immer sehr langsam und unter strenger ärztlicher Aufsicht erfolgen.
Bei Unruhezuständen und verstärkten Angstgefühlen, z.B. im Rahmen einer depressiven Störung sowie für die Behandlung von Schlafproblemen stehen Alternativen zu den Benzodiazepinen zur Verfügung. Den Patienten sollten solche Präparate v.a. im Hinblick auf ihr geringeres bzw. fehlendes Abhängigkeitspotential angeboten werden. Lavendelöl (Laitea), Kombination von Hopfen und Baldrian (Hova), Melatonin (Circadin) wirken nachweislich bei vielen Patienten und auch Mirtazapin (Remeron), Mianserin (Tolvon) und Tradozon (Trittico) sind als schlafanstossende Antidepressiva den Benzodiazepinen gegenüber zu bevorzugen.
Copyright bei Aerzteverlag medinfo AG
Zentrum für Psychiatrie und
Psychotherapie rechter Zürichsee Küsnacht
Dorfstrasse 5
8700 Küsnacht
Der Autor hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
beim Verfasser