Was die Kategorisierung von chronischem Schmerz anbelangt, gibt es mit ICD-11 eine erfreuliche Entwicklung: Chronischer Schmerz wird erstmalig als eigenständige Erkrankung eingestuft. Auch vermeidet es ICD-11 Schmerz ohne läsionale Ursache auf eine psychiatrische oder psychogene Sache zu reduzieren, sondern spricht deutungsneutral von «primären chronischen Schmerzen». Bei allen Formen chronischer Schmerzkrankheiten frägt das neue Diagnoseraster sowohl die Phänomenologie des subjektiven Schmerzempfindens wie auch psychosoziale Begleiterscheinungen ab. Implizit nähert sich das Schmerzverständnis in ICD-11 einem non-dualen Menschenbild und schafft eine gute Verständnisgrundlage für den multimodalen Behandlungsansatz.
As far as the categorization of chronic pain is concerned, there is a welcome development with ICD-11: for the first time, chronic pain is classified as a disease in its own right. ICD-11 also avoids reducing pain without a lesional cause to a psychiatric or psychogenic cause, but speaks of „primary chronic pain“ in a neutral way. For all forms of chronic pain disorders, the new diagnostic grid queries both the phenomenology of the subjective pain sensation and psychosocial concomitant symptoms. Implicitly, the understanding of pain in ICD-11 approaches a non-dual view of man and creates a good basis of understanding for the multimodal treatment approach.
Key Words: ICD-11, chronic pain, primary chronic pain, pain disorder, classification
Von einem dualistischen zu einem non-dualen Schmerzverständnis
ICD-11 (International Classification of Diseases, 11th Revision) ist weltweit seit Anfangs 2022 eingeführt worden und soll ICD-10 nach einer Übergangsfrist vollumfänglich ablösen (1). ICD ist kein Lehrbuch, sondern ein epidemiologisches Diagnose-Erfassungsinstrument der WHO. Die Klassifizierungs-Entwicklung chronischer Schmerzen in ICD ist ein interessanter Spiegel unseres kollektiven medizinischen Denkens, das sich stetig weiterentwickelt.
ICD-10 war bei seiner Einführung insofern fortschrittlich, als eine Diagnose-Kategorie für Schmerzerkrankungen ohne läsionale Ursache geschaffen worden ist. Im damaligen kollektiven medizinischen Bewusstsein war das ein Novum, denn Schmerz ohne läsionale Ursache war für viele bis anhin undenkbar: Wo kein Feuer ist, hat es auch keinen Rauch zu geben. Generationen von Fachleuten der Medizin und des medizinischen Versicherungswesens bewegten sich in diesem materialistisch-reduktionistischen Paradigma.
Aus heutiger Sicht war die Schmerzklassifikation des ICD-10s einer stark dualistischen Sichtweise verhaftet: Entweder hatte die betroffene Person eine plausible Läsion als Erklärung der chronischen Schmerzen vorzuweisen oder sie stand unter dem Verdacht an einer Psychopathologie zu leiden. Entsprechend wurde der nicht-läsionale Schmerz in ICD-10 im Kapitel der psychischen Störungen (Kapitel F) unter dem Begriff «somatoform» abgehandelt und de facto «psychiatrisiert».
Diese «Entweder-oder-Logik» wurde im deutschsprachigen Raum 2009 durchbrochen, indem der hiesigen ICD-10-Version zusätzlich eine «Sowohl-als-auch»-Schmerzdiagnose beigefügt worden ist: Die chronische Schmerzstörung mit somatischen und psychischen Faktoren (ICD-10, F 45.41). Diese Diagnose bildete die klinische Realität bereits viel umfassender ab, denn bei den allermeisten chronischen Schmerzen spielen sowohl organische wie psychische Faktoren eine Rolle.
Schmerzkrankheiten
Der Begriff der Schmerzerkrankung (engl. pain disease) ist in der heutigen medizinischen Literatur etabliert (2). Entsprechend versteht ICD-11 chronischer Schmerz als eine selbständige Krankheitsentität mit eigener Symptomatik und eigenen Vulnerabilitätskriterien. Chronische Schmerzerkrankungen lassen sich weder auf eine organische Läsion noch auf ihre psychische Modulierbarkeit reduzieren.
Dass Schmerz primär ein perzeptiver Vorgang ist und dass diese Perzeption sich krankhaft verändern kann, schien lange ausgeblendet. Das komplexe regionale Schmerzsyndrom (Abk. engl. CRPS) illustriert beispielhaft, dass das Schmerzperzeptions-System per se erkranken kann. Die peripheren und zentralen neurologischen Veränderungen beim CRPS stehen dabei weder in einem direkten kausalen Zusammenhang mit der auslösenden Läsion noch mit einer Psychopathologie. Die Forschungen zu «chronic widespread pain» zeigen ebenfalls für überregionale (z.B. halbseitige) (3) sowie generalisierte Schmerzerkrankungen (4) eine vergleichbar komplexe Pathophysiologie. Heute wissen wir, auf welch vielfältige Weise chronischer Schmerz mit neuroplastischen, neurovegetativen und neuroimmunologischen Veränderungen einhergeht. Ein zentraler pathophysiologischer Mechanismus ist hierbei das Phänomen der peripheren und zentralen Sensibilisierung durch neurogene Inflammation (4, 5).
Zunehmend erhärtet sich auch das Wissen hinsichtlich der Disposition für Schmerzerkrankungen. Eine kürzliche Studie anhand Pa-tientendaten von 500’000 Personen zeigt, welche gesundheitlichen Risikofaktoren statistisch typischerweise Schmerzausweitung und Schmerzchronifizierung voraussagen (6). Bei den genannten Faktoren (belastende Lebensereignisse, Ein- und Durschlafstörungen, Reizbarkeit, Erschöpfung, Anspannung, gesteigertes Essverhalten/Adipositas) ist unschwer die gemeinsame Basis der Stress-Physiologie festzustellen. Gleichsam mit den geläufigen Vulnerabilitätskonzepten der «pain proneness» (Kindheitsbelastungen) (7) und der «action proneness» (Verausgabung als Erwachsene) (8) lassen sich die genannten Faktoren der Stress-Schmerz-Vulnerabilitätshypothese zuordnen, die besagt, dass anhaltende oder heftige Stressbelastung das Schmerzperzeptionssystem auf verschiedenen Niveaus verändert (9-12).
Schmerzkategorien in ICD-11
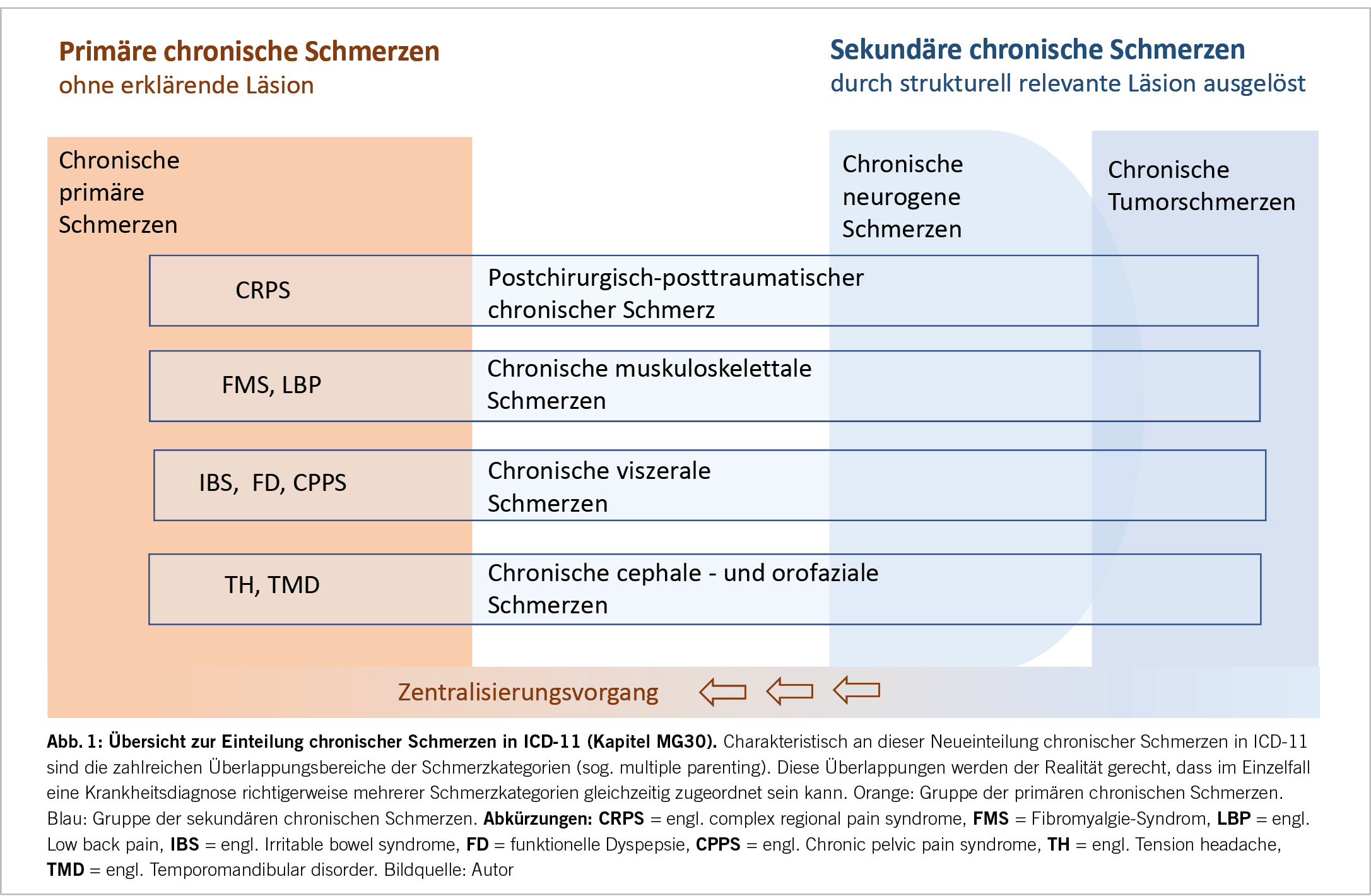
ICD-11 führt im Kapitel MG30 chronischen Schmerz als eine eigenständige Krankheits-Gruppe auf. Wert- und wortneutral unterteilt ICD-11 zwischen den beiden Hauptkategorien der sog. primären und sog. sekundären chronischen Schmerzen. Der Unterschied ist, naler Auslöser fassbar ist, auf dessen Grundlage sekundär eine chronische Schmerzerkrankung entsteht. Bei den primären chronischen Schmerzen ist diese Bedingung nicht nötig.
Einzelne Beispiele primärer Schmerzerkrankungen sind das erwähnte komplexe regionale Schmerzsyndrom, das Fibromyalgie-Syndrom, die chronische Migraine oder das chronische Beckenschmerz-Syndrom.
Beispiele für Unterkategorien sekundärer chronischer Schmerzen sind der tumorassoziierte chronische Schmerz, der neuropathische chronische Schmerz, der postoperative oder posttraumatische chronische Schmerz.
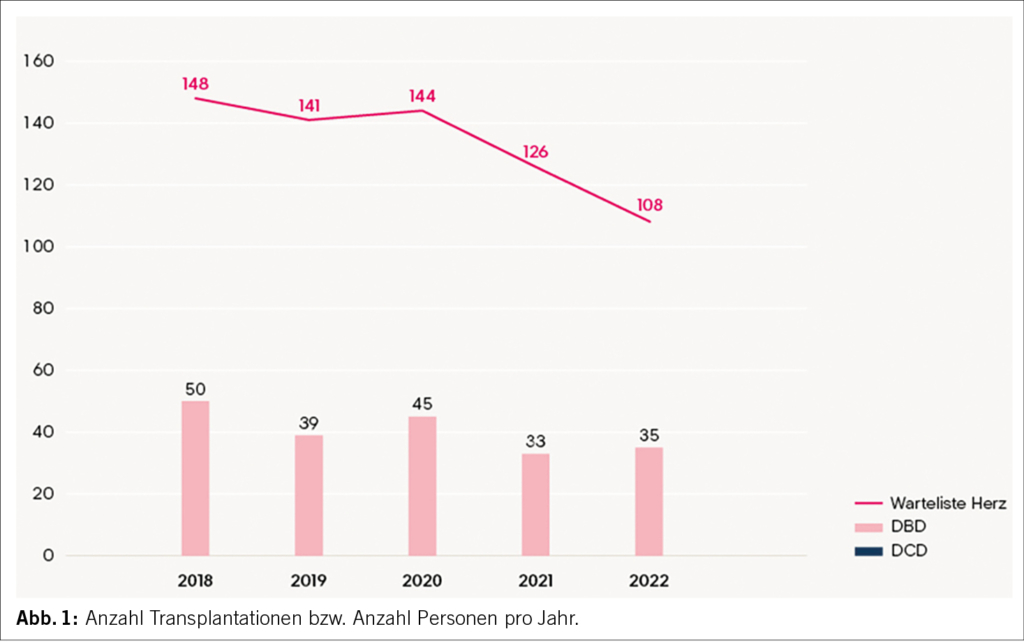
Realitätsentsprechend berücksichtigt ICD-11 die Tatsache, dass diese Schmerz-Unterkategorien einander nicht ausschliessen, sondern stets auch Überlappungsbereiche aufweisen. Das bedeutet, dass der Einzelfall richtigerweise gleichzeitig auch mehreren Kategorien zugeordnet werden kann (Abb. 1).
ICD-11 fordert die Integration des Subjektiven in die Schmerzdiagnostik
Chronischer Schmerz wird heute als anhaltender unangenehmer neuroperzeptiver Vorgang verstanden, der psychosoziale Implikationen mit sich führen kann. Der Tatsache, dass chronischer Schmerz immer auch psychischer Modulation unterworfen ist und regelhaft mit psychosozialen Faktoren verbunden ist, trägt ICD-11 Rechnung, indem bei allen Formen chronischer Schmerzkrankheiten eine sogenannte «Postkoordination» eingefordert wird. Hier geht es darum, die individuelle Erlebensdimension mittels spezifischer Items auszuloten und psychosoziale Aspekte einzubinden. Dieses mehrdimensionale Schmerz-Assessment ist eine gute Basis für eine individualisierte multimodale Schmerztherapie und auch Voraussetzung für eine ergebnisoffene und individualisierte Schmerzbegutachtung, wie sie in Schweizer Leitlinien gefordert wird (13).
Multimodale Schmerztherapie im ambulanten Bereich
Prinzipien, Inhalte und Wegleitungen zur multimodalen Schmerztherapie wurden bereits an anderer Stelle detailliert vorgestellt (14). Die multimodale Therapie geht über pharmakologische und interventionelle Massnahmen hinaus und fokussiert beim primären chronischen Schmerz vorab auf behaviorale Ressourcen und die physische Rekonditionierung. In der ambulanten Praxis bewährt sich hierfür eine interprofessionelle «therapeutische Triade» aufzubauen, in der Regel mit einer ärztlichen, einer physiotherapeutischen und einer psychologischen Fachperson. Der ärztlichen Fachperson obliegt die Verantwortung der klinischen Fallführung, das diagnostische Schmerzassessment, die Informationstherapie sowie fallentsprechend des Erstellens von Behandlungsvorschlägen für die beiden andern involvierten Fachpersonen. In der Physiotherapie geht es oft um die Überwindung schmerzassoziierter Myogelosen, um die Vermittlung körperlicher Entspannungsverfahren und die Anleitung zu einer dosierten Aktivierung zu Gunsten einer physischen Rekonditionierung (Pacing). Die psychologischen Interventionen fokussieren regelhaft auf Stressabbau, der Exploration von Entlastungsfaktoren, der Mobilisierung von Ressourcen, dem Ausbau von Copingstrategien, alles mit dem übergeordneten Ziel des Erlangens von mehr Selbstwirksamkeit im Schmerzerleben.
Regelmässige gemeinsame Fallbesprechungen (z.B. per Zoom) zur Zielüberprüfung verbessern die Therapie-Effizienz. Diese Team-arbeit ist oftmals für alle involvierten Personen entlastend und bereichernd zugleich. Die therapeutische Absprache ist per Tarmed abrechenbar (z.B. Tarmedposition 00.0144). Angesichts der grossen Häufigkeit chronischer Schmerzerkrankungen ist es lohnend, sich in der Behandlung dieser Erkrankungen gut aufzustellen.
Copyright bei Aerzteverlag medinfo AG
Akademie für Psychosomatische und
Psychosoziale Medizin (SAPPM)
Postfach 521
6062 Reiden
Der Autor hat keine Interessenskonflikte im Zusammenghang mit diesem Artikel deklariert.