Die Psoriasisarthritis (PsA) ist eine chronische inflammatorische Systemerkrankung, die mit der Immundermatose Psoriasis (Pso) assoziiert ist. Die Erkrankung birgt neben Schmerzen das Risiko eines Funktionsverlustes am Bewegungsapparat sowie einer Einschränkung der Lebensqualität. Insbesondere im Falle einer ungenügenden Krankheitskontrolle bestehen ein erhöhtes kardiovaskuläres Risiko und zahlreiche Komorbiditäten. In diesem Artikel stellen wir die Charakteristika der Psoriasisarthritis in Abgrenzung zu anderen entzündlich-rheumatischen Erkrankungen dar und beschreiben Risikofaktoren, die ein fachärztlich rheumatologisches Management erfordern. Das therapeutische Management wird in seinen Grundzügen erläutert.
Psoriatic arthritis (PsA) is a chronic inflammatory disease associated with psoriasis (Pso). Besides pain, PsA bears the risks of functional impairment of the musculoskeletal system and an overall reduction in the quality of life. Especially under insufficient disease control, PsA is associated with an increased risk of cardiovascular disease and numerous comorbidities. In this article, we present the characteristics of psoriatic arthritis distinguishing it from other inflammatory rheumatic diseases and describe risk factors that should encourage its management by a rheumatologist. The therapeutic management will be briefly sketched.
Key words: psoriatic arthritis, psoriasis, screening, treatment
Die Psoriasisarthritis (PsA) entwickelt sich bei ca. 30 % der Psoriasis-Patienten im Krankheitsverlauf. Bei gut 2/3 der Patienten geht die Hauterkrankung den anderen Symptomen voraus. Bei einem Teil der Betroffenen können aber erst Beschwerden am Bewegungsapparat manifest werden, die Hautveränderungen kommen dann im Verlauf dazu. Auch eine PsA ohne Hautbeteiligung ist möglich («Psoriasisarthritis sine Psoriasis»). Insbesondere bei diesen Patienten ist eine genaue Familienanamnese wichtig, denn in der Entstehung der Pso und der PsA spielen genetische Faktoren eine entscheidende Rolle. Die Erkrankung wird ausserdem durch metabolische und mikrobielle Faktoren beeinflusst.
Klinische Präsentation der Psoriasisarthritis
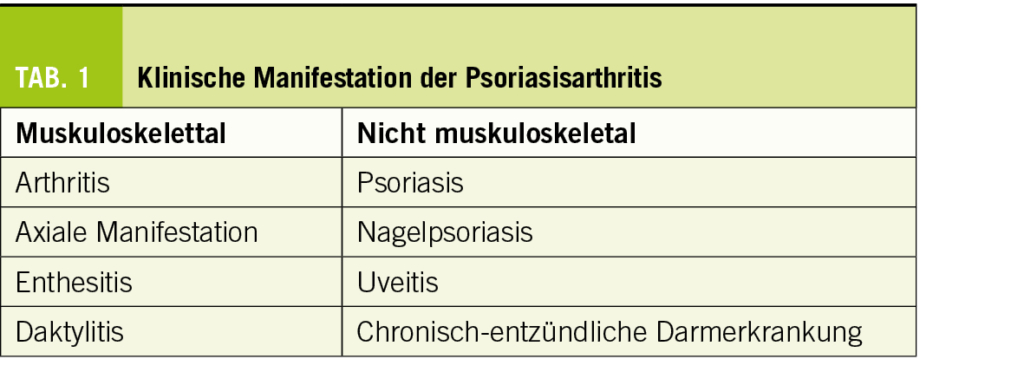
Die klinische Manifestation ist heterogen und umfasst muskulo-skelettale und nicht muskuloskelettale Aspekte (Tab.1). Typisch für die Psoriasis und für die Psoriasisarthritis ist die Assoziation der Entzündung zu mechanischem Stress (auch als «Mechanoinflammation» bezeichnet), was die Prädominanz der Entzündung an mechanisch exponierten Stellen wie der Haut an den Streckseiten über den Gelenken oder den Sehnenansätzen erklären kann.
Haut und Nägel
Neben der Psoriasis vulgaris treten weitere Formen der Psoriasis im Rahmen einer Psoriasisarthritis auf, u.a. die Psoriasis pustulosa, die Psoriasis guttata und die Psoriasis inversa. Die Nagelpsoriasis ist mit einem bis zu dreifach erhöhten Risiko für das Auftreten einer PsA assoziiert.
Periphere Arthritis, Enthesitis und Daktylitis
In 70 % der Fälle präsentiert sich die PsA, insbesondere zu Beginn, als Oligoarthritis. Hierbei kann prinzipiell jedes Gelenk betroffen sein, einschliesslich der DIP (distalen Interphalangeal)-Gelenke. Das Verteilungsmuster ist häufig asymmetrisch, typischerweise können Phalangen im Strahl betroffen sein. Zum Teil zeigt sich eine diffuse Schwellung eines gesamten Fingers oder Zehs mit Beteiligung der Weichteilstrukturen und der Gelenke, welche als Daktylitis oder «Wurstfinger/-zeh» bezeichnet wird. Polyartikuläre Verläufe können bei Fehlen typischer Hautläsion initial schwierig von einer rheumatoiden Arthritis unterschieden werden. Bei ausgeprägten destruktiven Veränderungen entwickeln sich mutilierende Veränderungen, welche dann eine Differenzierung anhand typischer Röntgenbefunde erlauben.
Axiale Manifestation
In bis zu 50 % der Patienten wird eine axiale Manifestation beschrieben. Diese manifestiert sich analog zur axialen Spondylarthritis häufig mit Rückenschmerzen mit entzündlichem Charakter. Der entzündliche Schmerzcharakter zeigt im Gegensatz zu mechanisch assoziierten Schmerzen eine Zunahme in Ruhe und eine Besserung durch Aktivität, eine verlängerte Morgensteifigkeit der Wirbelsäule, sowie ein sehr gutes Ansprechen auf NSAR.
Uveitis und Chronisch-entzündliche Darmerkrankungen
Diese nicht muskuloskelletalen Manifestationen treten bei einigen Patienten auf und spielen eine entscheidende Rolle in der Auswahl der Medikation (s. Management).
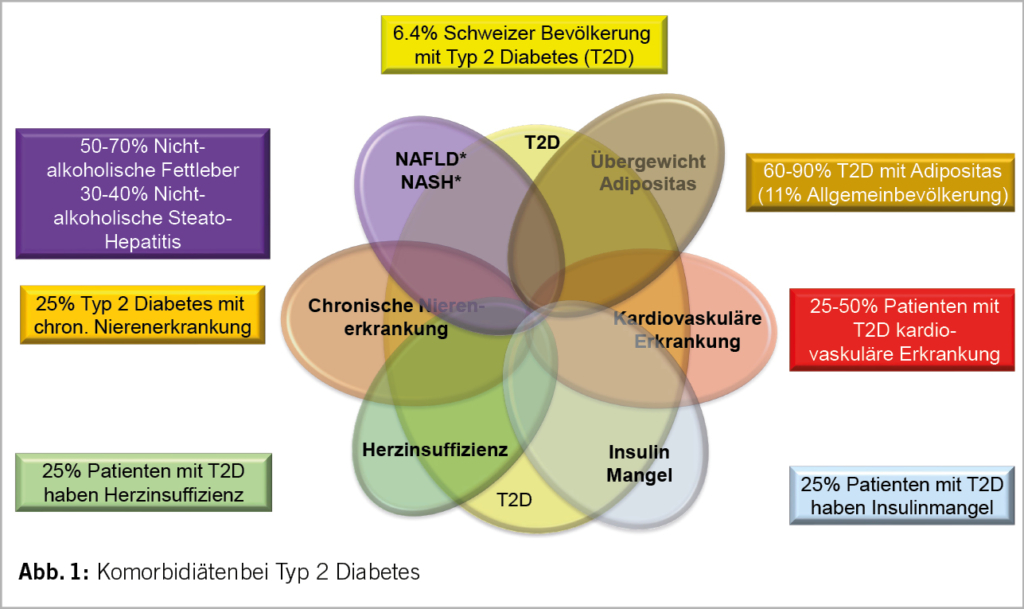
Komorbiditäten
Die PsA ist mit einer Reihe von Komorbiditäten assoziiert, insbesondere einem erhöhten kardiovaskulären Risiko multifaktorieller Genese. Neben der Inflammation und der Medikation (z.B. NSAR) finden sich bei PsA-Patientin auch häufiger traditionelle kardiovaskuläre Risikofaktoren wie eine arterielle Hypertonie, ein Diabetes mellitus, Atherosklerose und ein metabolisches Syndrom. Zudem ist die PsA mit Depression und Angststörungen assoziiert.
Labordiagnostik bei Psoriasisarthritis
Die Labordiagnostik in der PsA ist unspezifisch. Im Vergleich zu anderen entzündlich-rheumatischen Erkrankungen gibt es keine charakteristischen Laborparameter, insbesondere keine Auto-Antikörper. Laboruntersuchungen dienen somit primär dem Ausschluss von Differenzialdiagnosen und dem Screening von Komorbiditäten. Es empfiehlt sich insbesondere die einmalige Bestimmung von Rheumafaktoren und anti-CCP-Antikörpern zur Abgrenzung gegenüber einer rheumatoiden Arthritis. Akut-Phase-Proteine wie das C-reaktive Protein (CRP) sind bei der PsA häufig normwertig, was in der Differenzialdiagnostik ebenfalls hilfreich sein kann. Sind sie erhöht, zeigen sie eine schlechtere Prognose an und können im Verlauf gut mit dem Therapieansprechen korrelieren.
Bildgebung
Charakteristisch für die PsA sind die Coexistenz von erosiven und osteoproliferativen Veränderungen sowie weitere destruktive Veränderungen wie Lysen im Bereich der terminalen Phalangen und das sog. Pencil-in-cup-Phänomen. In axialen Aufnahmen finden sich Veränderungen analog zu axialen Spondylarthritiden, insbesondere können eine Sakroiliitis und Syndesmophyten nachgewiesen werden. MR-tomographisch und sonographisch kann eine entzündliche Aktivität abgebildet werden.
Identifikation von Patienten mit möglicher Psoriasisarthritis
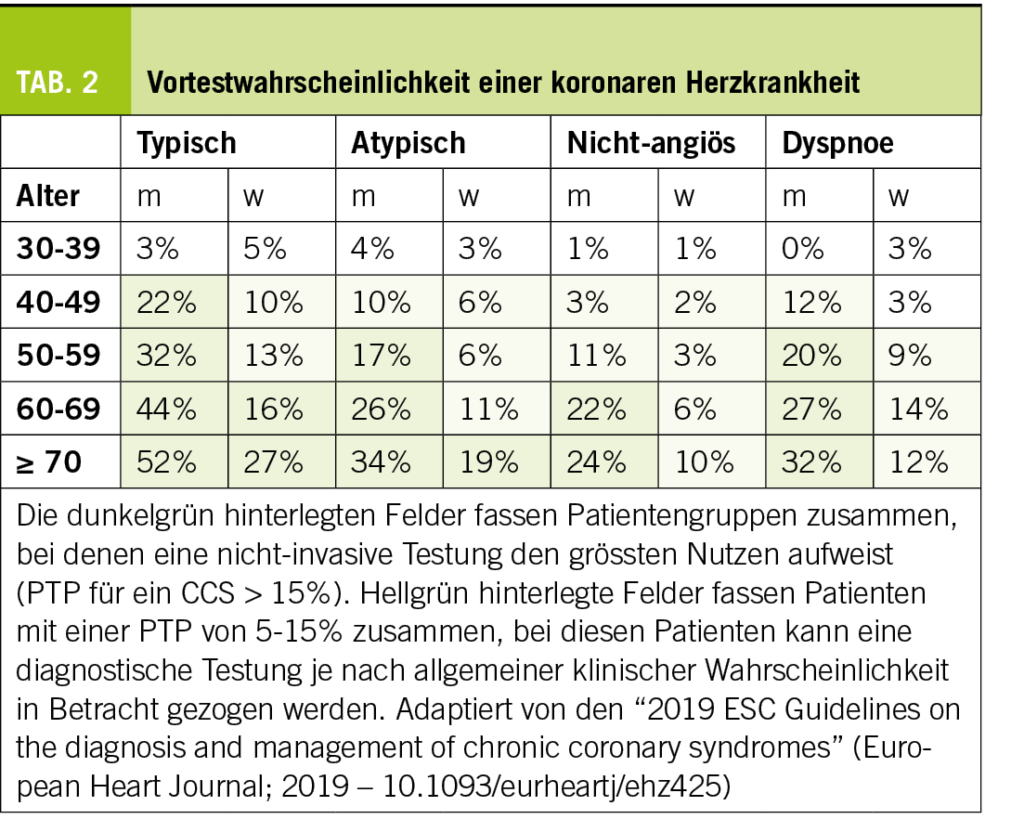
Zur Identifikation von Patienten mit einer möglichen Psoriasisarthritis bei bekannter Psoriasis stehen verschiedene Screening-Tools zur Verfügung, beispielsweise der Fragebogen der Rheumaliga Schweiz (1), der GEPARD (GErman Psoriasis ARthritis Diagnostic questionnaire) Fragebogen (2) oder der Psoriasis Epidemiology Screening Tool (PEST) Fragebogen (3). Anhand von einfachen Fragen kann hiermit die Entscheidung zur rheumatologischen Zuweisung des Patienten erleichtert werden. Relevante Fragen umfassen schmerzhafte Gelenkschwellungen und eine bereits nachgewiesene Arthritis, eine Nagelpsoriasis, eine Daktylitis und eine Achillodynie als möglichen Hinweis für eine Enthesitis (Tab. 2).
Management der Psoriasisarthritis
Das therapeutische Management orientiert sich an dem individuellen klinischen Manifestationsmuster und den Komorbiditäten. Optimalerweise erfolgt die Behandlung im interdisziplinären Team aus Rheumatologen, Dermatologen und Allgemeinmedizinern, sowie ggf. auch Ophthalmologen und Gastroenterologen. Die Patientenedukation, sowie das Screening und Management kardiovaskulärer Risikofaktoren sind immer fester Bestandteil der Behandlung.
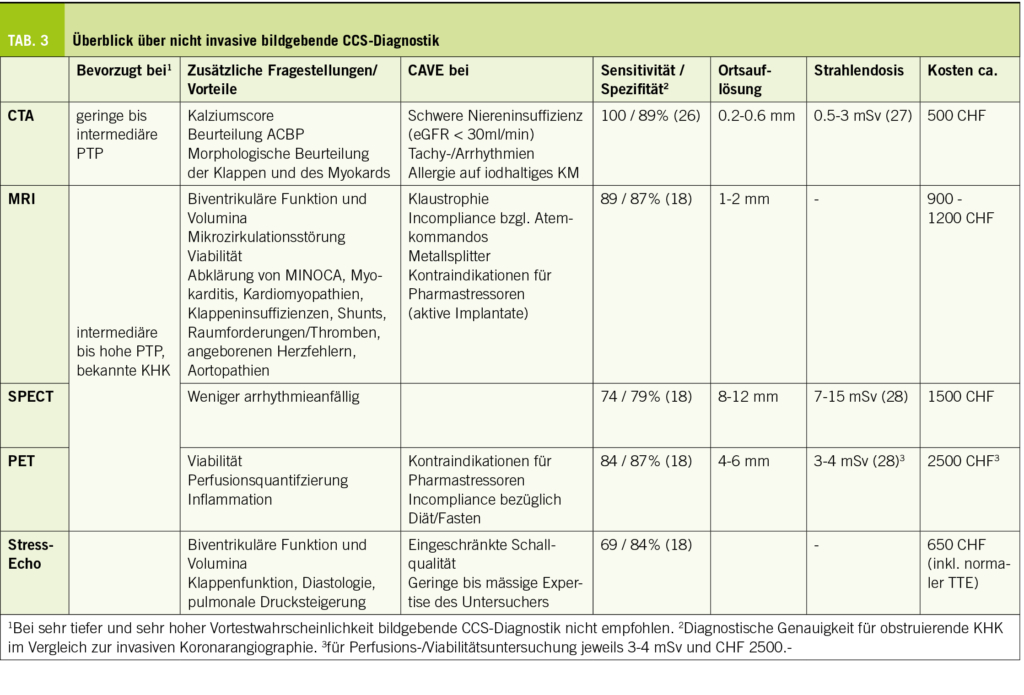
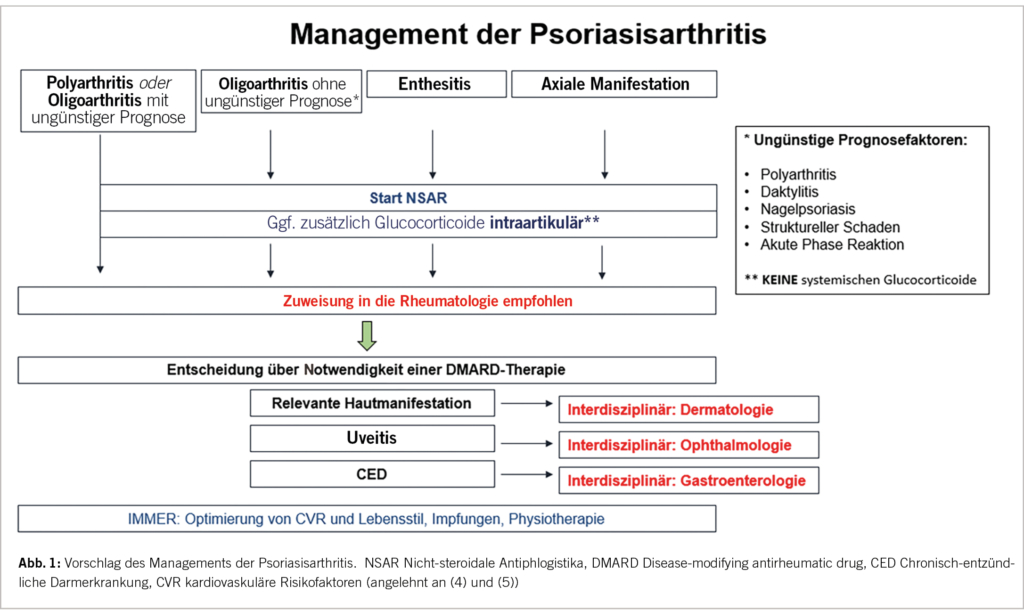
Der im Folgenden dargestellte Therapiealgorithmus basiert auf den Empfehlungen der GRAPPA [4] und der EULAR [5; Neue Empfehlungen aus 2023, präsentiert auf dem EULAR Kongress 2023]. Die Erstlinientherapie der muskuloskelettalen Manifestation sind Nicht-steroidale Antiphlogistika (NSAR). Bei der Gabe von NSAR müssen gastrointestinale, kardiovaskuläre und renale Risiken beachtet werden. Alternativ oder ergänzend können bei einer Oligoarthritis intraartikuläre Glukokortikoid-Infiltrationen erwogen werden. Systemische Glukokortikoide haben in der Therapie der PsA in aller Regel keinen Stellenwert und sollten vor dem Hintergrund einer möglichen Zunahme psoriatischer Hautläsionen und der Komorbiditäten vermieden werden. Im Falle einer persistierenden Symptomatik unter NSAR nach maximal 4 Wochen oder Vorliegen von negativen prognostischen Faktoren wird eine DMARD (Disease-modifying antirheumatic drug)-Therapie empfohlen (Abb. 1).
Zur Verfügung stehen eine Vielzahl von DMARDs mit unterschiedlichen Wirkmechanismen und Limitationen. Neben den konventionellen, synthetischen (cs)DMARDs wie Methotrexat (MTX) finden sich inzwischen fünf verschiedene zugelassene biologische Wirkprinzipien (TNF-Inhibitoren, IL-17A-Inhibitoren, IL-12/23-Inhibitoren, IL-23-In-hibitoren und ein CTLA4-Inhibitor) und ein weiterer (IL17A/F-Inhibitor mit in Kürze erwarteter Zulassung, sowie Januskinase (JAK)-Inhibitoren und der Phosphodiesterase(PDE)4-Hemmer Apremilast.
Die Auswahl der Medikation erfolgt individuell anhand des Verteilungsmusters und der Komborbiditäten unter Berücksichtigung der Patientenpräferenzen. Bei axi aler Manifestation, Uveitis oder chronisch-entzündlicher Darmerkrankung sind konventionelle DMARDs i.d.R. nicht ausreichend effektiv.
Copyright bei Aerzteverlag medinfo AG
Stadtspital Zürich
Abteilung für Rheumatologie,
Birmensdorferstrasse 497
8055 Zürich
Stadtspital Zürich
Abteilung für Rheumatologie,
Birmensdorferstrasse 497
8055 Zürich
Die Autorin und der Autor haben keine Interessesnkonflikte im Zusammenhang mit diesem Artikel deklariert.
1 https://www.rheumaliga.ch/fragebogen-psoriasis-arthritis
2 https://www.psoriasis-bund.de/fileadmin/images/download/formulare/GEPARD Fragebogen.pdf
3 Ibrahim GH, Buch MH, Lawson C et al. Evaluation of an existing screening tool for psoriatic arthritis in people with psoriasis and the development of a new instrument: the Psoriasis Epidemiology Screening Tool (PEST) questionnaire. Clin Exp Rheumatol. 2009; 27(3):469-74.
4 Coates LC, Soriano ER, Corp N. et al. GRAPPA Treatment Recommendations domain subcommittees. Group for Research and Assessment of Psoriasis and Psoriatic Arthritis (GRAPPA): updated treatment recommendations for psoriatic arthritis 2021. Nat Rev Rheumatol. 2022;18(8):465-479.
5 Gossec L et al. (2023) EULAR recommendations 2023