Der Klimawandel stellt eine zunehmende Bedrohung für die öffentliche Gesundheit dar. Insbesondere Herz-Kreislauf-Erkrankungen werden für eine übermässige Sterblichkeitsrate bei extremen Temperaturen verantwortlich gemacht. Dabei tragen sowohl niedrige als auch hohe Umgebungstemperaturen zu einer Vielzahl negativer Gesundheitsfolgen bei. Obwohl die kältebedingte Sterblichkeit derzeit höher ist als die durch hohe Temperaturen bedingte, ist die kältebedingte Sterblichkeitsrate in den letzten Jahrzehnten zurückgegangen, während die hitzebedingte Übersterblichkeit gestiegen ist. Ältere Erwachsene sind besonders gefährdet, vor allem solche mit häufigen altersbedingten chronischen Erkrankungen. Beeinträchtigungen der physiologischen Reaktionen auf die Regulierung der Körpertemperatur, der hämodynamischen Stabilität und der Flüssigkeitszufuhr tragen zu einem erhöhten Risiko von Gesundheitsstörungen bei älteren Menschen bei, die nicht optimalen Umgebungstemperaturen ausgesetzt sind. Die Entwicklung von Strategien, die darauf abzielen, hitzegefährdete Personen sowohl vor übermässiger Hitze- als auch vor Kältesterblichkeit zu schützen, ist daher dringend notwendig, wobei unterschiedliche regionale Bedürfnisse berücksichtigt werden müssen.
Climate change constitutes an increasing threat to public health. Particularly cardiovascular disease is made responsible for an excess death burden during extreme temperatures. Thereby both, low and high ambient temperatures contribute to a high range of adverse health outcomes. Although current mortality linked to cold temperatures is higher than the one linked to high temperatures, over the last decades cold-related death rate has decreased, whereas heat-related excess death ratio has increased. Older adults are particularly vulnerable, especially those with common age related chronic health conditions. Impairments in the physiological responses to the regulation of body temperature, hemodynamic stability and hydration contribute to an increased risk of health disorders in older individuals exposed to non-optimal ambient temperatures. The development of strategies aiming at protecting heat vulnerable individuals against both excess heat and cold mortality burden are therefore required, taking into account the variations in regional needs.
Key Words: climate change, ambient temperatures, cold, heatwave, cardiovascular disease
Gesundheitliche Belastung durch extreme Temperaturen
Das Interesse an den Auswirkungen der Klimaerwärmung auf die Gesundheit nimmt aufgrund der spürbaren klimatischen Veränderungen und besorgniserregenden Prognosen stetig zu. Es wird befürchtet, dass zukünftig sowohl vermehrte Hitzewellen als auch Kälteperioden zu einer globalen Bedrohung der Gesundheit werden.
Seit 1880 hat die durchschnittliche Oberflächentemperatur der Erde um 0.07 C° pro Dekade zugenommen. Seit den 1990er Jahren hat sich diese Zunahme um das Dreifache beschleunigt. Dies hat seit dem Jahr 2000 zu 19 der 20 heissesten Jahren mit einer Kumulierung von Hitzewellen geführt, wie sie betreffend Häufigkeit, Intensität und Dauer bislang unbekannt waren (1). Das saisonale Muster einer Übermortalität während heissen Sommertagen, aber auch während Kälteperioden ist seit längerem bekannt (2). Dabei tritt die Gefährdung durch Hitze typischerweise innerhalb weniger Tage auf, während sich der Effekt von Kälteperioden erst 3 oder 4 Wochen später manifestiert (3, 4).
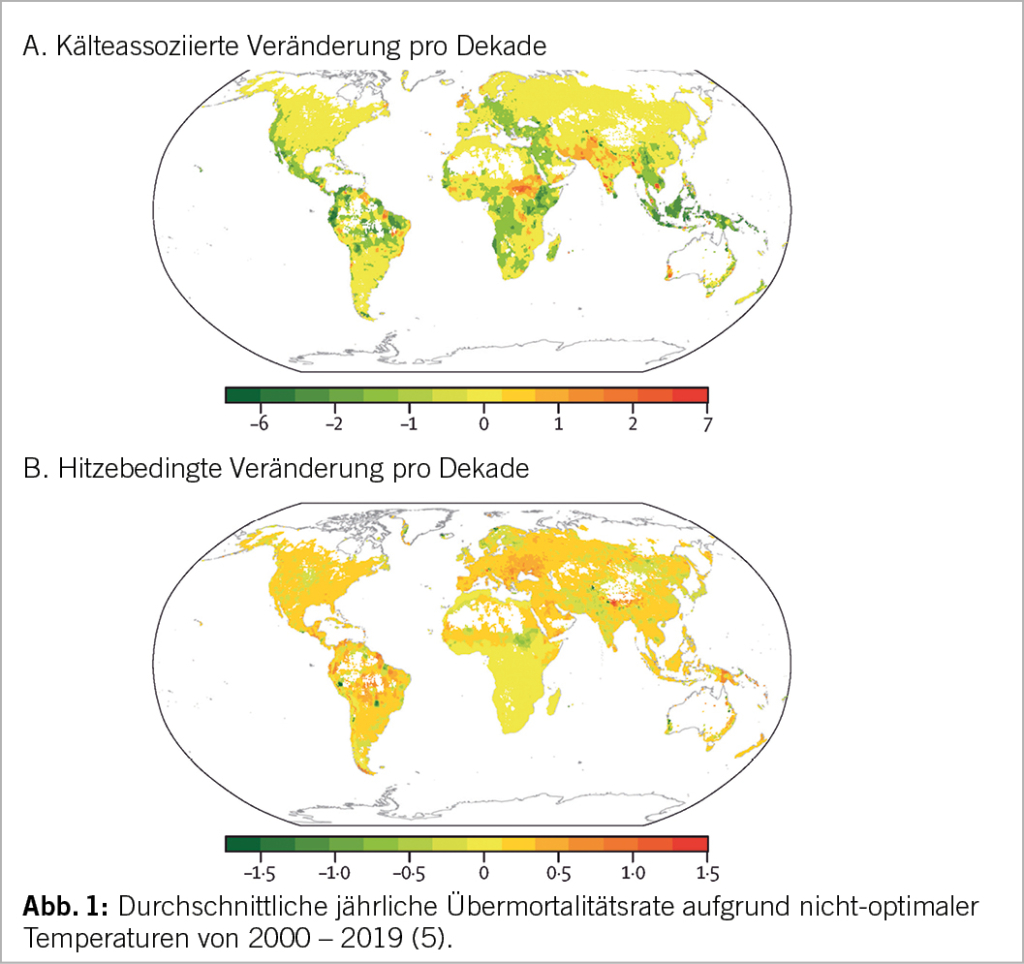
Das «Multi-Country Multi-City» (MCC) Collaborative Research Network sammelt seit 2014 überregional Daten zur temperatur-assoziierten Mortalität und deckt an 750 repräsentativen Orten aktuell 46.3% der weltweiten Fläche ab. In einer von ihren kürzlich publizierten Studien führten Zhao Q. et al. 9.4% der globalen Mortalität oder einen Sterblichkeitsüberschuss von 74 auf 100‘000 Einwohner auf extreme Umgebungstemperaturen zurück (5). Die Übermortalität war dabei in Kälteperioden höher (8.52%) als während Hitzeperioden (0.91%). Insgesamt nahmen aber die kälteassoziierten Todesfälle seit dem Jahr 2000 um 0.51% ab, währendem die hitzebezogene Todesrate um 0.21% zunahm.
Dabei wurden starke regionale Unterschiede verzeichnet (Abb. 1). Mehr als die Hälfte der Übermortalität wurde in Asien beobachtet, speziell in tief gelegenen und stark bevölkerten Küstenstädten Ost- und Süd-Asiens. Osteuropa hatte die höchste hitzebezogene, Subsahara-Afrika die höchste kältebezogene Übermortalitätsrate. Die tiefsten Übermortalitätsraten wurden in Lateinamerika, der Karibik und Südostasien beobachtet. Allerdings war eine hohe hitzebedingte Mortalitätsrate entlang der Westküste Lateinamerikas zu beobachten.
Diese geographischen Unterschiede zeigen, dass die Gefährdung der Gesundheit durch Extremtemperaturen zwar eine globale Erscheinung ist, aber je nach Region spezifische Anpassungen zum Schutz der Gesundheit nötig sind. So wurde z.B. in Südostasien eine Abnahme der kältebedingten Übermortalität verzeichnet. Auch in Ozeanien sind die kälteassoziierten Todesfälle substantiell zurückgegangen, allerdings haben die hitzebedingten Todesfälle überdurchschnittlich zugenommen, letzteres auch in Europa. Südasien war die einzige Region, wo die Durchschnittstemperatur abnahm, einhergehend mit einer Zunahme der kältebezogenen und der Gesamtmortalität.
Insgesamt führte die Zunahme der globalen Durchschnittstemperatur um 0.26° pro Dekade zwischen 2000 und 2019 zu einer deutlichen Abnahme der kältebezogenen und einer moderaten Erhöhung der hitzebezogenen Todesfälle, sodass Netto eine Reduktion der temperaturbezogenen Todesfälle verzeichnet wurde. Langfristig wird allerdings erwartet, dass die Mortalitätslast steigt.
Temperaturextreme und kardiovaskuläre Mortalität
Für die meisten klimaassoziierten Todesfälle werden kardiovaskuläre Erkrankungen verantwortlich gemacht. In ihrer multinationalen Studie in verschiedenen Klimazonen mit unterschiedlichen sozioökonomischen und demographischen Charakteristika zeigten Ahlamad et al., dass bei ischämischer Kardiopathie extreme Temperaturschwankungen für ca. 1% aller Todesfälle verantwortlich sind. Betreffend Hirnschlag wurde geschätzt, dass für 1000 Todesfälle 1.6, respektive 9 Todesfälle auf extreme Hitze- oder Kältetage zurückzuführen waren. Länder mit niedrigem Bruttosozialprodukt scheinen ein bis zu 3-fach erhöhtes Hirnschlagrisiko aufzuweisen (6). Dies könnte sowohl auf bessere Möglichkeiten reicher Länder einer Hitzeexposition auszuweichen als auch auf seltener im Freien durchgeführte Arbeiten zurückzuführen sein. Auch im Augsburger Register zeigte sich, dass zwischen 2001 und 2014, im Vergleich zum Zeitraum zwischen 1987 und 2000, das Risiko von hitzebedingten Myokardinfarkten signifikant anstieg, insbesondere in ländlichen Gegenden und bei Patienten mit Diabetes mellitus (7). Betreffend Mortalitätsrisiko der Herzinsuffizienz infolge extremer Temperaturen gibt es bislang wenig Evidenz, allerdings zeigten einzelne Studien höhere Hospitalisationsraten im Winter oder an heissen Tagen.
Adaptation an Temperaturschwankungen bei extremen Temperaturen (7)
Verschiedene Mechanismen werden für das erhöhte kardiovaskuläre Risiko bei extremen Temperaturen verantwortlich gemacht. Sowohl Kälte- wie auch Hitzeexposition stimulieren das sympathische Nervensystem mit entsprechender Auswirkung auf den Kreislauf. In der Hitze führt die Volumendepletion, in der Kälte die Vasokonstriktion und gesteigerte periphere Muskeldurchblutung zur Wärmeproduktion zur vermehrten Kreislaufbelastung. Aufgrund von Volumenverschiebungen gehen sowohl Hitze als auch Kälte mit einem gerinnungsaktivierenden Zustand einher. Die zunehmende Kreislaufbelastung, sowohl für die Wärmeabgabe als auch zur Wärmekonservierung, führt zu steigendem Sauerstoffbedarf, was bei Personen mit bekannter Arteriosklerose zu einer Bedarfsischämie oder einem erhöhten Risiko einer Plaqueruptur führen kann. Elektrolytstörungen, insbesondere bei Hitze, können das Arrhythmierisiko erhöhen (8-10).
Thermoregulation
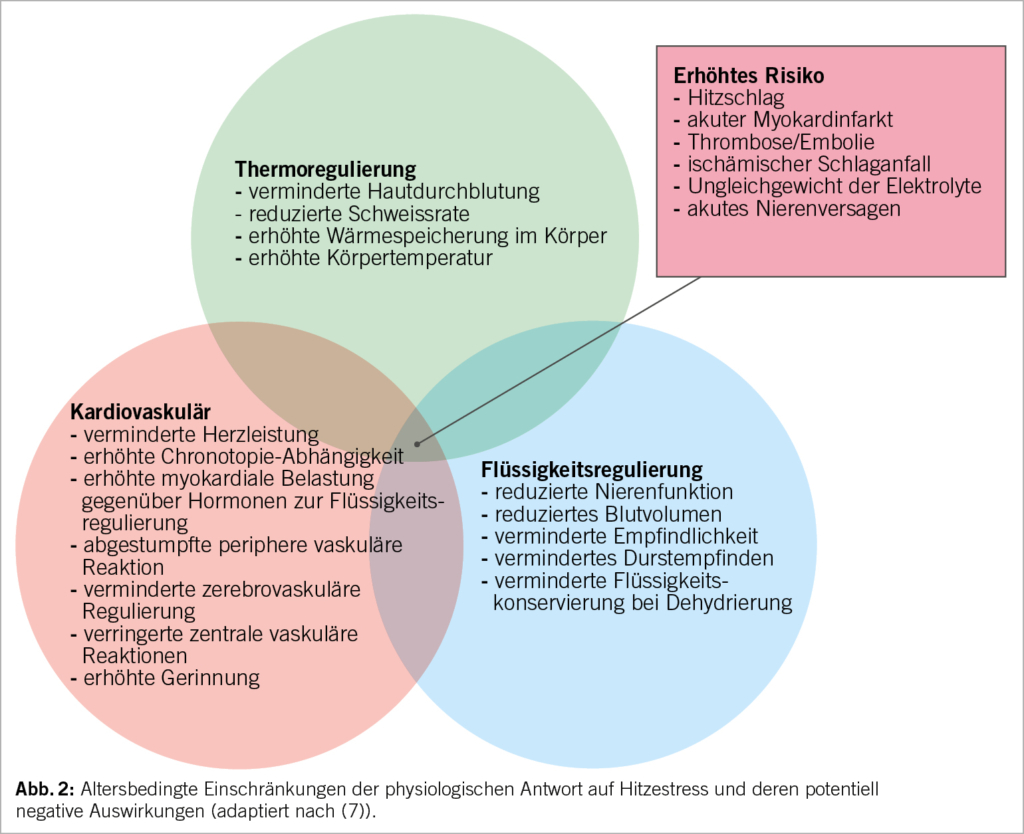
Die grösste Hitze-Vulnerabilität besteht bei älteren Personen mit altersassoziierten chronischen Erkrankungen (kardiovaskuläre Erkrankungen, Diabetes Typ 2) (Abb. 2). Die beeinträchtigte Regulation der Körpertemperatur und die verminderte hämodynamische Stabilität (Aufrechterhaltung des Blutdrucks und der Endorganperfusion) im höheren Alter fördern die Anfälligkeit gegenüber Hitzewellen (11).
Der Mensch kontrolliert seine Körpertemperatur in einem engen Bereich zwischen 36.5 und 37.0° C. Dies bedarf eines fein adjustierten Gleichgewichtes zwischen endogen produzierter Wärme und sowohl trockenem (Konvektion, Radiation, Konduktion) wie auch über Verdunstung erfolgendem Wärmeaustausch mit der Umgebung. Dieser Wärmeaustausch erfolgt sowohl über einen Temperatur- als auch einen Wasserdruckgradienten und wird durch Verhaltensmassnahmen und autonome Thermoeffektor-Antworten beeinflusst.
Der effektivste Thermoeffektor ist das individuelle Verhalten (12). Der Hitze an einem kühlen Ort auszuweichen oder der Einsatz von Air-Conditioning während Hitzewellen sind mit einer deutlich geringeren Morbidität und Mortalität vergesellschaftet. Allerdings können ältere Leute aufgrund von funktionellen oder kognitiven Einschränkungen ihr Verhalten häufig nicht mehr adäquat anpassen, resp. die eigene Körpertemperatur nicht mehr richtig einschätzen.
Bei Hitzeexposition übersteigt die Zunahme der Körpertemperatur initial die Kapazität der Wärmeabgabe und führt so zu einer vermehrten Wärmespeicherung, welche durch körperliche Aktivität noch verstärkt wird. Der daraus resultierende Anstieg der Körpertemperatur wird primär durch zentralnervöse und kutane Thermorezeptoren erfasst. Als primäre Reaktion erfolgt die durch das sympathische Nervensystem gesteuerte Vasodilatation auf der Haut und die ekkrine Schweissproduktion, was die Wärmeabgabe durch Konvektion erleichtert. Der daraus resultierende Anstieg der Hauttemperatur erhöht durch die Zunahme des Wärmegradienten zwischen Haut und Umgebung den trockenen Wärmeverlust. Gleichzeitig wird Wärme über 2-3‘000‘000 Schweissdrüsen abgegeben, was der effizientesten Methode der Thermoregulation in heisser, trockener Umgebung entspricht, insbesondere weil die Wärmeabgabe über Verdunstung unabhängig von der Umgebungstemperatur entlang einem Haut-Umgebungs-Wasserdampfgradienten erfolgt. Dies bedeutet aber, dass diese Art der Wärmeabgabe in feuchter Umgebung weniger effizient ist.
Solange die Wärmeabgabe den Wärmezuwachs auszugleichen vermag (kompensierbarer Zustand), wird sich die Körpertemperatur stabilisieren, wenn auch auf einem höheren Level. Im Gegensatz dazu können heissere oder feuchtere Bedingungen dazu führen, dass die Kapazität der Wärmeabgabe durch die Umgebungsbedingungen überfordert wird. In solchen Situationen des nicht kompensierbaren Zustandes wird die anhaltende Exposition zu einem progressiven Anstieg der Körpertemperatur führen und die Gesundheit gefährden (9). Dabei nimmt die thermoregulatorische Funktion mit zunehmendem Alter ab. Die Ursache ist multifaktoriell und beinhaltet die Abnahme der Bio-Verfügbarkeit von Stickstoff-Monoxid, eine Verminderung der autonomen Kontrolle der Autozirkulation und der kardialen Reserven sowie ein geringeres Ansprechen der Schweissdrüsen auf Veränderungen der Körpertemperatur (13).
Hämodynamische Regulation
Hitzestress löst eine ausgeprägte kardiovaskuläre Antwort zur Regulation der Körpertemperatur und Erhaltung der Hämodynamik aus. Bei jungen Individuen kann bei extremer Hitze die Hautdurchblutung durch kutane Vasodilatation von ca. 0.3 L/min in Ruhe auf 6–7 L/min ansteigen. Die entsprechende Steigerung des Herzminutenvolumens erfolgt vor allem durch Steigerung der Herzfrequenz. Das Schlagvolumen bleibt unverändert oder nimmt durch Steigerung der myokardialen Kontraktilität nur unwesentlich zu, trotz Abnahme des zentralvenösen Druckes und der kardialen Vorlast. Die gleichzeitige Vasokonstriktion im splanchnischen und renalen Gefässbett erleichtert dabei die Blutverteilung zu den zentralen Organen und zur Haut.
Diese Anpassungen erfolgen durch die sympathische Aktivierung des autonomen Nervensystems. Je älter ein Individuum, umso eingeschränkter ist allerdings die kardiovaskuläre Antwort und entsprechend geringer die Erhöhung der Hautdurchblutung. Verantwortlich dafür sind hauptsächlich eine Zunahme der endothelialen Dysfunktion und der arteriellen Steifigkeit, eine Reduktion der kardialen Reserven und eine verminderte autonome Antwort.
Eine allfällige altersbedingte kardiale Dysfunktion verstärkt dabei die inadäquate kardiovaskuläre Antwort gegenüber der Hitzeexposition weiter. Vor allem die verminderte Antwort auf die beta-adrenerge Stimulation und veränderte kardiale Mechanik limitieren das Herzminutenvolumen. Zudem ist das Schlagvolumen bei Hitzestress für eine vorgegebene linksventrikuläre Füllung im Vergleich zu normaler Temperatur vermindert. Schliesslich nimmt mit zunehmendem Alter auch die autonome Regulation des Blutdrucks ab (verminderte Baroreflexsensitivität).
Regulation des Flüssigkeitshaushaltes
Die Regulation des Flüssigkeitshaushaltes ist für die Erhaltung des intravaskulären Volumens und zur Unterstützung der hämodynamischen Stabilität bei Hitzestress essentiell. Weil Natrium und andere Elektrolyte bei der Flüssigkeitsabsonderung reabsorbiert werden, führt die hitzeinduzierte Dehydratation zu einem Zustand der Hämokonzentration mit reduziertem zirkulierendem Volumen (Hypovolämie) und erhöhter Serumosmolalität (hyperosmotische Hyponaträmie). Diese Veränderungen reduzieren die kutane Vasodilatation und Schweissproduktion für eine gegebene Körpertemperatur, was zu einer Zunahme des Kern-zu-Haut Temperaturgradienten führt. Damit vermindert sich die kutane Durchblutung und das Schwitzen. Diese Reaktion fördert die hämodynamische Stabilität und beugt bei niedrigeren Temperaturen einem weiteren Flüssigkeitsverlust vor. Bei höheren Temperaturen allerdings reduziert die Dehydratation die Wärmeabgabe und die Schwelle zur Nicht-Kompensierbarkeit des Temperaturanstiegs.
Die Dehydratation triggert regulatorische Anpassungen zur Wiedererlangung der Euhydratation. Änderungen in der Plasma Osmolalität werden von zentralen Osmorezeptoren der Arteria carotis interna an den Hypothalamus weitergeleitet. Bereits kleine Veränderungen von 1-2 % fördern das Durstgefühl und via Sekretion von Vasopressin die Reduktion der Ausscheidung von freiem Wasser über die Nieren. Die hormonelle Kontrolle des Flüssigkeitsgleichgewichts wird wegen der sekundären renalen Hypo-Perfusion durch die Aktivierung des Renin-Angiotensin-Aldosteron-Systems unterstützt. Dies führt zu einer Vielzahl von Effekten entlang der kardio-renalen Achse, wie die Reduktion des renalen Blutflusses, die Zunahme des Durstgefühls, der Vasopressin-Ausschüttung und der renalen Natriumretention. Auch die hämodynamischen Veränderungen, welche über Barorezeptoren in den Venen und in der Herzwand wahrgenommen werden, stimulieren die vermehrte Ausschüttung von Vasopressin- und das Durstgefühl.
Zweitabdruck aus «info@herz+gefäss» 03-2023
Copyright bei Aerzteverlag medinfo AG
Klinik Gais AG
Gäbrisstrasse 1172
9056 Gais
Der Autor hat keine Interessenkonflikte im Zusammenhang mit diesem Artikel deklariert.
1. climate. Global climate report—annual 2019. 2020. https://www.ncdc.noaa.gov/sotc/global/201913 (accessed Oct 11, 2020).
2. Kalkstein LS, Greene JS. An evaluation of climate/mortality relationships in large U.S. cities and the possible impacts of a climate change. Environ Health Perspect. 1997;105(1):84-93.
3. Analitis A, Katsouyanni K, Biggeri A, Baccini M, Forsberg B, Bisanti L, et al. Effects of cold weather on mortality: results from 15 European cities within the PHEWE project. Am J Epidemiol. 2008;168(12):1397-408.
4. Anderson BG, Bell ML. Weather-related mortality: how heat, cold, and heat waves affect mortality in the United States. Epidemiology. 2009;20(2):205-13.
5. Zhao Q, Guo Y, Ye T, Gasparrini A, Tong S, Overcenco A, et al. Global, regional, and national burden of mortality associated with non-optimal ambient temperatures from 2000 to 2019: a three-stage modelling study. Lancet Planet Health. 2021;5(7):e415-e25.
6. Alahmad B, Khraishah H, Roye D, Vicedo-Cabrera AM, Guo Y, Papatheodorou SI, et al. Associations Between Extreme Temperatures and Cardiovascular Cause-Specific Mortality: Results From 27 Countries. Circulation. 2023;147(1):35-46.
7. Meade RD, Akerman AP, Notley SR, McGinn R, Poirier P, Gosselin P, et al. Physiological factors characterizing heat-vulnerable older adults: A narrative review. Environ Int. 2020;144:105909.
8. Claeys MJ, Rajagopalan S, Nawrot TS, Brook RD. Climate and environmental triggers of acute myocardial infarction. Eur Heart J. 2017;38(13):955-60.
9. Kenny GP, Yardley J, Brown C, Sigal RJ, Jay O. Heat stress in older individuals and patients with common chronic diseases. CMAJ. 2010;182(10):1053-60.
10. Schauble CL, Hampel R, Breitner S, Ruckerl R, Phipps R, Diaz-Sanchez D, et al. Short-term effects of air temperature on blood markers of coagulation and inflammation in potentially susceptible individuals. Occup Environ Med. 2012;69(9):670-8.
11. Schneider A, Ruckerl R, Breitner S, Wolf K, Peters A. Thermal Control, Weather, and Aging. Curr Environ Health Rep. 2017;4(1):21-9.
12. Flouris AD, Schlader ZJ. Human behavioral thermoregulation during exercise in the heat. Scand J Med Sci Sports. 2015;25 Suppl 1:52-64.
13. Kenney WL, Munce TA. Invited review: aging and human temperature regulation. J Appl Physiol (1985). 2003;95(6):2598-603.