Die unsachgemässe Verschreibung von Antibiotika ist bei Atemwegsinfektionen weit verbreitet. Dies ist insbesondere in Pflegeheimen der Fall, was zur Antibiotikaresistenz beiträgt und die Bewohner vermeidbaren Nebenwirkungen aussetzt. In diesem Artikel werden verschiedene Möglichkeiten zur Optimierung der Verschreibungspraxis untersucht. Dabei werden sowohl bewährte Strategien aus Antibiotika-Stewardship-Programmen als auch innovative Ansätze, wie z. B. Entscheidungsalgorithmen, die Point-of-Care-Tests integrieren, oder die Verwendung von Lungenultraschall als Diagnosehilfe, berücksichtigt.
The inappropriate prescription of antibiotics is common for respiratory infections. This is particularly the case in nursing homes, contributing to antibiotic resistance and exposing residents to preventable adverse effects. This article explores various ways to optimise prescribing practices, drawing on both validated antibiotic stewardship programme strategies and innovative approaches, such as decision-making algorithms incorporating point-of-care tests or the use of lung ultrasound as a diagnostic aid.
Keywords: Antibiotic prescription, Nursing homes, Antibiotic stewardship, Respiratory infections, Rapid diagnostic tests
Der Verbrauch von Antibiotika
Antibiotikaresistenzen stellen eine Gefahr für die globale öffentliche Gesundheit dar, und der unsachgemässe Einsatz von Antibiotika trägt wesentlich dazu bei (1). Bewohner von Pflegeheimen erhalten doppelt so häufig Antibiotika wie ältere Personen, die zu Hause leben (2). Dabei ist die Hälfte dieser Verschreibungen nicht indiziert (3). Eine aktuelle Studie zur Prävalenz von Verschreibungen hat gezeigt, dass in der Schweiz 2.9 % der Bewohner am Tag der Erhebung eine Antibiotikabehandlung erhielten, wobei es Unterschiede zwischen den Einrichtungen in den Kantonen Waadt und St. Gallen gab (3.9 % gegenüber 1.8 %; p = 0.05) (4). Die häufigsten Fälle unzweckmässiger Verschreibungen in Pflegeheimen sind asymptomatische Bakteriurie und Atemwegsinfektionen. Zusätzlich zu den Resistenzen können Antibiotika den Bewohnern durch Nebenwirkungen wie Magen-Darm-Beschwerden und Hautausschläge sowie Veränderungen der Mikrobiota direkt schaden (5, 6). Bewohner von Pflegeheimen mit hohem Antibiotikaverbrauch haben ein erhöhtes Risiko für Magen-Darm-Beschwerden, selbst wenn sie nicht direkt Antibiotika ausgesetzt sind, im Vergleich zu Bewohnern von Einrichtungen mit geringerem Verbrauch (7).
Atemwegsinfektionen
Die Verschreibungsrate für Atemwegsinfektionen in europäischen Einrichtungen schwankt zwischen 53 und 80 % (2), wobei es zu einer erheblichen Überverschreibung bei akuten Bronchitiserkrankungen kommt, die meist viralen Ursprungs sind und daher spontan abklingen (8). Dieser hohe Einsatz lässt sich durch mehrere Faktoren erklären: (i) eine erhöhte Inzidenz von Atemwegsinfektionen aufgrund von Immunoseneszenz und Schluckstörungen, die das Verschlucken begünstigen, und (ii) die Schwierigkeit, Bewohner mit einer Lungenentzündung zu identifizieren. Dies ist auf unspezifische klinische Symptome (7), die begrenzte Verfügbarkeit diagnostischer Tests, insbesondere Blut- und Röntgenuntersuchungen, sowie die Tatsache, dass in den meisten Einrichtungen keine Ärzte vor Ort sind, zurückzuführen (3).
Antibiotika-Stewardship-Programme
Antibiotika-Stewardship-Programme sind Programme, die einen verantwortungsvollen Umgang mit Antibiotika aufzeigen. Sie umfassen Strategien, die sicherstellen sollen, dass Patientinnen und Patienten mit einer behandlungsbedürftigen Infektion das am besten geeignete Antibiotikum in der richtigen Dosierung und über die optimale Dauer erhalten (10). Die Einführung von Antibiotika-Stewardship-Programme in Pflegeheimen ist eine schwierige Aufgabe. Im Gegensatz zur Akutversorgung sind diese Programme in der Regel weniger gut organisiert und verfügen über weniger Ressourcen (3). Weitere Hindernisse für die Umsetzung sind: (i) der eingeschränkte Zugang zu bestimmten diagnostischen Tests vor Ort (Laboruntersuchungen und Radiologie) in Verbindung mit einer unsachgemässen Verwendung anderer Tests (Urinstix), (ii) die erste klinische Beurteilung durch das Pflegepersonal mit zahlreichen telefonischen Verschreibungen, (iii) das Fehlen von Daten zur Resistenz in diesem Umfeld und (iv) die hohe Kolonisationsrate, insbesondere der Harnwege und der Haut (3). Auch wenn nur wenige Studien die Wirksamkeit und Sicherheit von Antibiotika-Stewardship-Programmen in Pflegeheimen bewerten, deuten einige Literaturübersichten darauf hin, dass diese Programme tendenziell den Einsatz von Antibiotika verbessern, ohne die Zahl der Krankenhausaufenthalte oder die Sterblichkeit zu erhöhen (11–14).
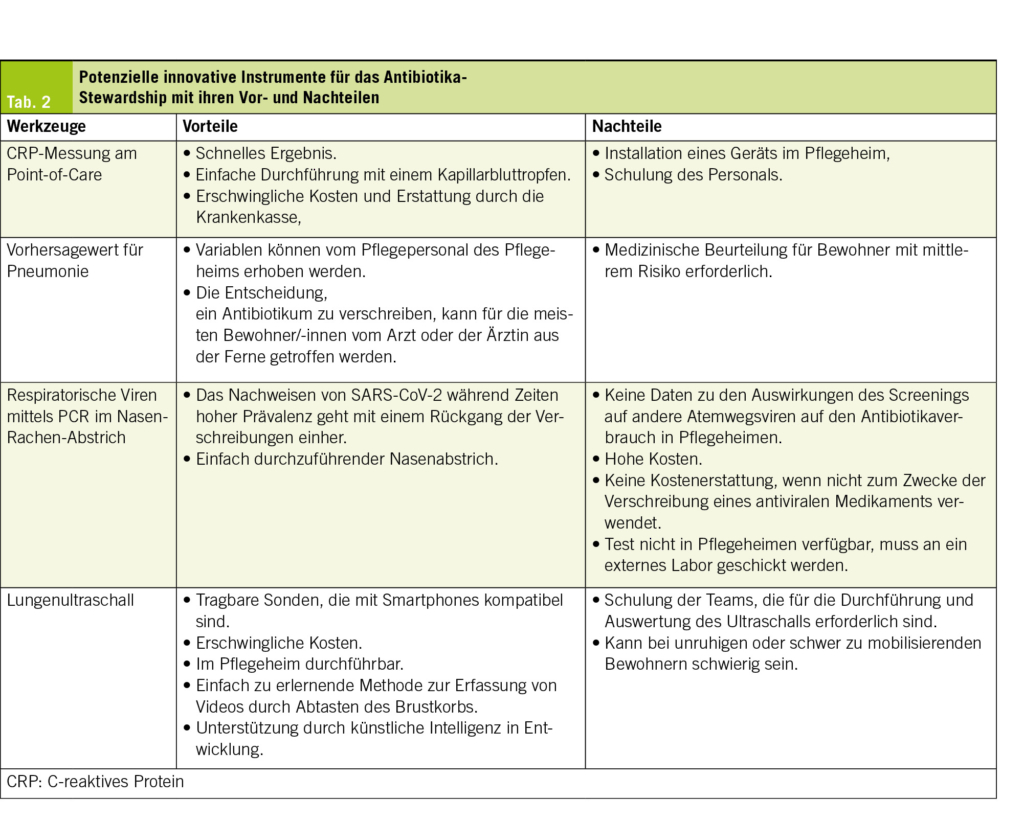
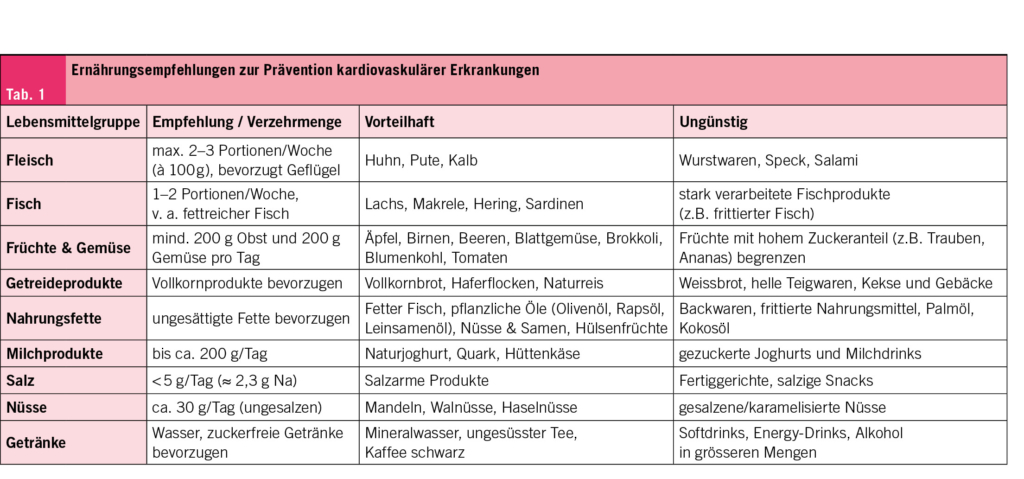
Angesichts der hohen Überverschreibungsrate und der negativen Auswirkungen auf die Bewohner ist es dringend erforderlich, Antibiotika-Stewardship-Programme einzuführen, die an den Kontext von Pflegeheimen angepasst sind, um den Selektionsdruck durch Antibiotika zu verringern und die Qualität der Pflege zu verbessern (11). Es gibt zahlreiche mögliche Massnahmen (Tab. 1), wie z. B. die Förderung lokaler Empfehlungen für die Diagnose und Behandlung häufiger Infektionen, die Reduzierung unnötiger mikrobiologischer Tests sowie die Förderung von Point-of-Care-Schnelltests (POC), die vor Ort durchgeführt werden können und deren Ergebnisse schnell verfügbar sind (3).
Antibiotika-Stewardship-Instrumente für Atemwegsinfektionen
Lokale Empfehlungen
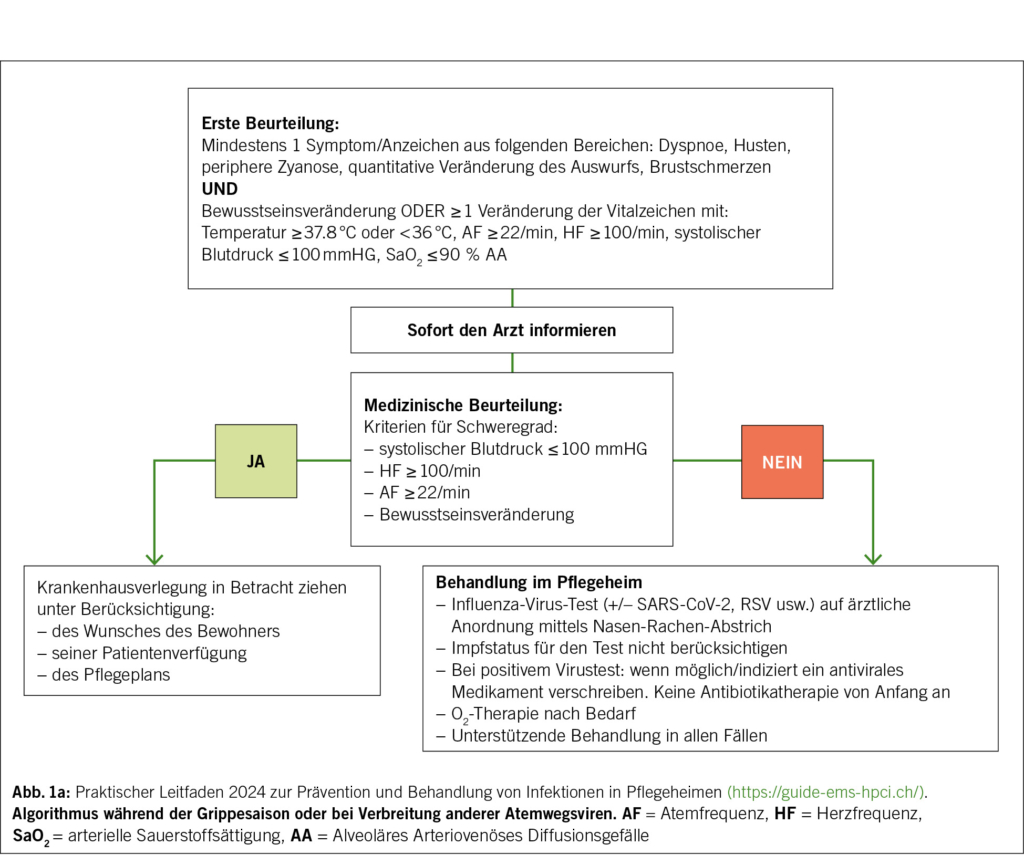
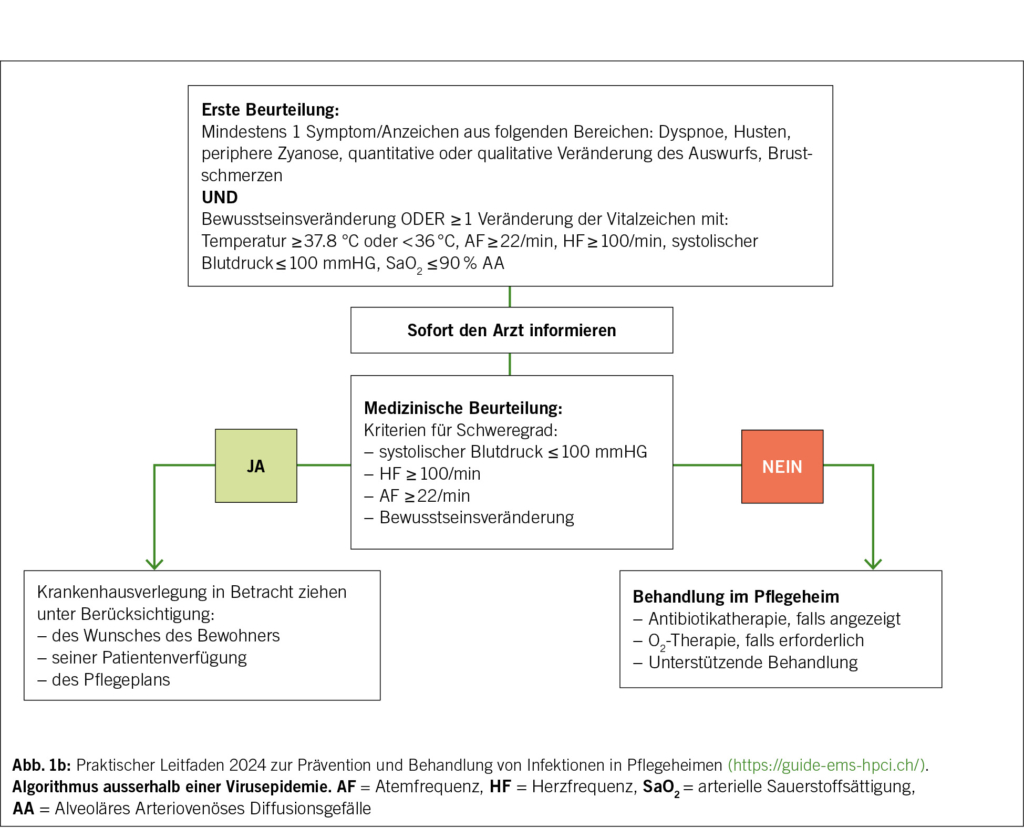
Ein Teil der Schweizer Pflegeheime (in der Westschweiz, im Kanton Bern und im Tessin) profitiert von lokalen Empfehlungen zur Diagnose und empirischen Behandlung häufiger Infektionen (https://guide-ems-hpci.ch/). Eine Studie zur «Qualität der Pflege» in Waadtländer Pflegeheimen hat gezeigt, dass die Verbreitung von Empfehlungen zur empirischen Verschreibung von Antibiotika und die Einrichtung von Qualitätszirkeln, in denen Ärzte, Apotheker und Pflegepersonal zusammenkommen, zu einer Verringerung der Verschreibungen geführt haben (15). Bei Atemwegsinfektionen unterscheiden die Empfehlungen zwischen der Behandlung während und ausserhalb der Grippe- und anderen Atemwegsvirus-Saison (Abb. 1a und 1b). Während einer Virus-Epidemie wird empfohlen, Atemwegsviren zu testen und bei einem positiven Testergebnis nicht sofort eine Antibiotikatherapie zu verschreiben.
Entzündungsbiomarker
Eine kürzlich in niederländischen Pflegeheimen durchgeführte randomisierte kontrollierte Studie zeigte einen signifikanten Rückgang der Antibiotikaverordnungen bei Bewohnern mit Atemwegsinfektionen in Pflegeheimen, die Zugang zu POC-C-reaktivem Protein (CRP) hatten, im Vergleich zu Pflegeheimen der Kontrollgruppe (54 % gegenüber 83 % Verordnungen, p < 0.001) (16). Diese Ergebnisse sind zwar ermutigend, lassen sich jedoch nur schwer auf den Schweizer Kontext übertragen. In der zitierten Studie waren Ärzte vor Ort, um die Bewohner klinisch zu untersuchen, während in unserem Kontext die klinische Beurteilung der Bewohner in Pflegeheimen hauptsächlich vom Pflegepersonal durchgeführt wird und die Verschreibungsentscheidungen oft telefonisch von den Ärzten getroffen werden.
Screening auf Atemwegsviren
Ein zweites Beispiel für einen POC-Test ist das Screening auf Atemwegsviren. Obwohl es sich um molekulare Tests handelt, deren Ergebnis in der Regel innerhalb von 1 bis 2 Stunden vorliegt, werden sie derzeit in Labors ausserhalb der Pflegeheime durchgeführt, was die Ergebnisermittlung für eine Entscheidung in Echtzeit verzögert. Eine Metaanalyse hat gezeigt, dass der systematische Einsatz molekularer Schnelltests für Atemwegsviren in Notaufnahmen die Verschreibung von Antibiotika nicht reduziert (17). Die Auswirkungen dieser Tests in Pflegeheimen wurden jedoch nicht bewertet, und SARS-CoV-2-Tests wurden in dieser Studie nicht untersucht.
Daten aus französischsprachigen Schweizer Pflegeheimen
Faktoren im Zusammenhang mit Verschreibungen bei Atemwegsinfektionen
In einer Kohorte von 114 Bewohnern mit einer Infektion der unteren Atemwege (18) erhielten 55 % Antibiotika, was einer relativ geringen Verschreibungsrate im Vergleich zum Durchschnitt in europäischen Einrichtungen (53 bis 80 %) entspricht (2). Unter den mit Antibiotika behandelten Bewohnern wies die Mehrheit (74 %) keine radiologischen Anzeichen einer Lungenentzündung auf, was auf eine unangemessene Verschreibung hindeutet.
Mehrere Faktoren standen im Zusammenhang mit der Verschreibung von Antibiotika: (i) ein Frailty-Score ≥ 7 beim Bewohner, (ii) eine Sauerstoffsättigung < 92 %, was den Schweregrad der Infektion widerspiegelt, (iii) das Fehlen einer biologischen Untersuchung einschliesslich CRP und/oder eines Blutbildes und (iv) institutionelle Merkmale, wie z. B. eine Einrichtung in einem städtischen Gebiet oder die Anwesenheit eines männlichen Arztes. Die Durchführung eines PCR-Tests auf Atemwegsviren war der einzige Schutzfaktor gegen unangemessene Verschreibungen.
Diese Studie legt nahe, dass diagnostische Tests, insbesondere Blutuntersuchungen und virale PCR-Tests, die Verschreibung von Antibiotika, insbesondere unangemessenen Antibiotika, reduzieren könnten. Dennoch werden sie in der Praxis nur selten eingesetzt: In dieser Kohorte erhielten nur 44 % der Bewohner einen Virustest und 14 % einen Bluttest. POC-Tests scheinen eine geeignete Lösung zu sein, und ihre Verwendung könnte als Instrument zur Antibiotikastewardship gefördert werden.
Entwicklung eines Score zur Vorhersage einer Lungenentzündung
In derselben Kohorte, die seit der ersten Analyse um 92 Bewohner gewachsen ist (insgesamt 206), wurde ein Entscheidungsindex entwickelt, der Vitalparameter und Entzündungsbiomarker, die am Point-of-Care verfügbar sind, kombiniert, um das Vorliegen einer Lungenentzündung vorherzusagen (SGAIM 2025, Abstract 254). Dieser Score basiert auf fünf Variablen, die vom Pflegepersonal leicht zu erfassen sind: Alter ≥ 80 Jahre [1 Punkt], Body-Mass-Index <18.5 kg/m2 [2 Punkte], Herzfrequenz >100/min [1 Punkt], Atemfrequenz ≥ 22/min [1 Punkt] und CRP > 60 mg/L [2 Punkte], was insgesamt 0 bis 7 Punkte ergibt. Es wurden drei Risikostufen definiert: gering (0–1), mittel (2) und hoch (3–7). Der Score zeigte eine gute diagnostische Leistung für die Gruppen mit geringem und hohem Risiko (Sensitivität 86 %, Spezifität 74 %, positiver prädiktiver Wert 71 %, negativer prädiktiver Wert 89 %). Er könnte als Leitfaden für die Verschreibung dienen: keine Antibiotika für Bewohner mit einem niedrigen Score, Antibiotika für diejenigen mit einem hohen Score und eine medizinische Beurteilung vor der Entscheidung für Bewohner mit einem mittleren Score. Obwohl er ein vielversprechendes Potenzial für die Verschreibung hat, ist eine randomisierte kontrollierte Studie erforderlich, um seine klinische Sicherheit und seine Auswirkungen auf die Verschreibung zu bestätigen (Tab. 2).
Screening auf Atemwegsviren
Eine retrospektive Beobachtungsstudie, die zwischen 2021 und 2023 in 45 Pflegeheimen im Kanton Waadt (ca. 2400 Betten) durchgeführt wurde, untersuchte den Zusammenhang zwischen (i) dem Screening auf SARS-CoV-2, (ii) einem positiven SARS-CoV-2-Test und der Verschreibung von Antibiotika (SGAIM 2025, Abstract 257). Während das Screening an sich nicht mit der Verschreibung in Verbindung stand, war ein positives SARS-CoV-2-Ergebnis mit einer Verringerung der Antibiotikaverordnung verbunden. Im Durchschnitt sind 3.5 positive Tests erforderlich, um eine Verschreibung zu vermeiden. Dies deutet darauf hin, dass SARS-CoV-2-Tests in einem Umfeld mit hoher Prävalenz dazu beitragen könnten, die Verschreibung von Antibiotika zu reduzieren. Diese Ergebnisse stehen im Einklang mit den lokalen Empfehlungen zur Behandlung von Atemwegsinfektionen während einer Virusepidemie (Abb. 1, Tab. 2).
Lungenultraschall
Die Diagnose einer Lungenentzündung basiert auf einer radiologischen Untersuchung, aber eine Röntgenaufnahme des Brustkorbs ist in der Praxis in Pflegeheimen nur schwer durchführbar. In der oben genannten Kohorte von Bewohnern mit Atemwegsinfektionen wurden nur 3 % der Bewohner dieser Untersuchung unterzogen (18). Die Lungenultraschalluntersuchung, die auch von der Schweizerischen Gesellschaft für Infektionskrankheiten empfohlen wird, stellt eine interessante Alternative dar, die mehrere Vorteile vereint: eine gute diagnostische Leistungsfähigkeit bei älteren Menschen (19) und die Verfügbarkeit von tragbaren Sonden, die mit Tablets und Smartphones kompatibel sind (20, 21). Die Lungenultraschalluntersuchung kann am Bett des Patienten durchgeführt werden, wodurch Transportwege vermieden werden und sie zu einer Bildgebungsmethode der Wahl in Pflegeheimen werden könnte. Um die Einführung dieses Instruments in einer Umgebung mit Anwendern ohne Vorkenntnisse zu fördern, hat sich gezeigt, dass einfach durchzuführende Techniken zur Untersuchung des Brustkorbs genauso wirksam sind wie eine gezielte Untersuchung auf pathologische Anzeichen (ESCMID 2025, Poster P3146). Darüber hinaus scheint die KI-gestützte Bildinterpretation sehr vielversprechend zu sein und das Potenzial zu haben, den Einsatz von Ultraschall durch Kliniker zu erleichtern (22) (Tab. 2).
Fazit
Der unsachgemässe Einsatz von Antibiotika in Pflegeheimen, insbesondere bei Atemwegsinfektionen, ist ein grosses Problem für die öffentliche Gesundheit, da er die Antibiotikaresistenz fördert und die Bewohner vermeidbaren Nebenwirkungen aussetzt. Trotz der strukturellen Zwänge, die diesen Einrichtungen eigen sind, bieten gezielte Strategien wie angepasste Empfehlungen, POC-Tests, einfache Entscheidungshilfen oder Lungenultraschalluntersuchungen vielversprechendes Potenzial, um die Relevanz der Verschreibungen bei Atemwegsinfektionen zu verbessern. Wir benötigen mehr Evidenz in diesem wenig erforschten Bereich der Gesundheitsversorgung, um geeignete, sichere und wirksame Strategien umsetzen zu können. Es ist daher notwendig, diese innovativen Ansätze in prospektiven Studien zu validieren, um sie in Antibiotika-Stewardship-Programme integrieren und die Verschreibung von Antibiotika optimieren zu können, ohne die Lebensqualität der Bewohnerinnen und Bewohner zu beeinträchtigen.
Dr. med. Alexia Roux 1
Dr. med. Nicola De Pasquale 1
M. Marc Jeanneret 1
Dr. med. Diem-Lan Vu 2, 3
Dr. med. Anne Niquille 4, 5
Dr. med. Eve Rubli Truchard 6
Dr. med. Tosca Bizzozzero 7
Dr. med. Emmanouil Glampedakis 8
Prof. Dr. med. Virginie Prendki 9,10
Prof. Dr. med. Noémie Boillat-Blanco 1
1 Infectious Diseases Service, Lausanne University Hospital and University of Lausanne, Lausanne
2 Communicable disease unit, Division of General cantonal physician, Geneva Directorate of Health, Geneva
3 Paediatric Infectious Diseases Unit, Department of Woman, Child and Adolescent, University Hospitals of Geneva, Geneva
4 Institute of Pharmaceutical Sciences of Western Switzerland, University of Geneva, University of Lausanne, Geneva
5 Department of ambulatory care, Unisanté, Center for Primary Care and Public Health, University of Lausanne, Lausanne
6 Geriatric Medicine and Geriatric Rehabilitation Division, Lausanne University Hospital and University of Lausanne, Lausanne
7 Department of Internal Medicine and Geriatrics, Morges Hospital, Morges
8 Cantonal Unit for Infection Control and Prevention, Public Health Service, Lausanne
9 Division of Infectious Diseases, Geneva University Hospitals, Geneva, Switzerland
10 Division of Internal Medicine for the Aged, Department of Rehabilitation and Geriatrics, Geneva University Hospitals
Copyright
Aerzteverlag medinfo AG
Übersetzung aus la gazette médicale 07/25 (noch nicht erschienen)
Infectious Diseases Service, Lausanne University Hospital and University of Lausanne, Lausanne
Infectious Diseases Service, Lausanne University Hospital and University of Lausanne, Lausanne
Infectious Diseases Service, Lausanne University Hospital and University of Lausanne, Lausanne
Die Autorenschaft hat keine Interessenskonflikte im Zusammenhang mit diesem Artikel deklariert.
1. Prestinaci F, Pezzotti P, Pantosti A. Antimicrobial resistance: a global multifaceted phenomenon. Pathogens and Global Health. 3 oct 2015;109(7):309‑18.
2. Huang Y, Wei WI, Correia DF, Ma BHM, Tang A, Yeoh EK, et al. Antibiotic use for respiratory tract infections among older adults living in long-term care facilities: a systematic review and meta-analysis. Journal of Hospital Infection. janv 2023;131:107‑21.
3. Dyar OJ, Pagani L, Pulcini C. Strategies and challenges of antimicrobial stewardship in long-term care facilities. Clinical Microbiology and Infection. janv 2015;21(1):10‑9.
4. Héquet D, Kessler S, Rettenmund G, Lemmenmeier E, Qalla-Widmer L, Gardiol C, et al. Healthcare-associated infections and antibiotic use in long-term care residents from two geographical regions in Switzerland. Journal of Hospital Infection. nov 2021;117:172‑8.
5. Mullish BH, Williams HR. Clostridium difficile infection and antibiotic-associated diarrhoea. Clinical Medicine. juin 2018;18(3):237‑41.
6. Lawes T, Lopez-Lozano JM, Nebot CA, Macartney G, Subbarao-Sharma R, Wares KD, et al. Effect of a national 4C antibiotic stewardship intervention on the clinical and molecular epidemiology of Clostridium difficile infections in a region of Scotland: a non-linear time-series analysis. The Lancet Infectious Diseases. févr 2017;17(2):194‑206.
7. Daneman N, Bronskill SE, Gruneir A, Newman AM, Fischer HD, Rochon PA, et al. Variability in Antibiotic Use Across Nursing Homes and the Risk of Antibiotic-Related Adverse Outcomes for Individual Residents. JAMA Intern Med. 1 août 2015;175(8):1331.
8. Sloane PD, Zimmerman S, Nace DA. Progress and Challenges in the Management of Nursing Home Infections. Journal of the American Medical Directors Association. janv 2020;21(1):1‑4.
9. Montoya A, Cassone M, Mody L. Infections in Nursing Homes. Clinics in Geriatric Medicine. août 2016;32(3):585‑607.
10. Hwang S, Kwon KT. Core Elements for Successful Implementation of Antimicrobial Stewardship Programs. Infect Chemother. 2021;53(3):421.
11. Falcone M, Paul M, Yahav D, Orlando G, Tiseo G, Prendki V, et al. Antimicrobial consumption and impact of antimicrobial stewardship programmes in long-term care facilities. Clinical Microbiology and Infection. mai 2019;25(5):562‑9.
12. Nguyen HQ, Tunney MM, Hughes CM. Interventions to Improve Antimicrobial Stewardship for Older People in Care Homes: A Systematic Review. Drugs Aging. avr 2019;36(4):355‑69.
13. Crespo-Rivas JC, Guisado-Gil AB, Peñalva G, Rodríguez-Villodres Á, Martín-Gandul C, Pachón-Ibáñez ME, et al. Are antimicrobial stewardship interventions effective and safe in long-term care facilities? A systematic review and meta-analysis. Clinical Microbiology and Infection. oct 2021;27(10):1431‑8.
14. Wu JH, Langford BJ, Daneman N, Friedrich JO, Garber G. Antimicrobial Stewardship Programs in Long-Term Care Settings: A Meta-Analysis and Systematic Review. J American Geriatrics Society. févr 2019;67(2):392‑9.
15. Plüss-Suard C, Niquille A, Héquet D, Krähenbühl S, Pichon R, Zanetti G, et al. Decrease in Antibacterial Use and Facility-Level Variability After the Introduction of Guidelines and Implementation of Physician-Pharmacist-Nurse Quality Circles in Swiss Long-term Care Facilities. Journal of the American Medical Directors Association. janv 2020;21(1):78‑83.
16. Boere TM, Van Buul LW, Hopstaken RM, Van Tulder MW, Twisk JWMR, Verheij TJM, et al. Effect of C reactive protein point-of-care testing on antibiotic prescribing for lower respiratory tract infections in nursing home residents: cluster randomised controlled trial. BMJ. 21 sept 2021;n2198.
17. Brendish NJ, Schiff HF, Clark TW. Point-of-care testing for respiratory viruses in adults: The current landscape and future potential. Journal of Infection. nov 2015;71(5):501‑10.
18. Roux A, Vu DL, Niquille A, Rubli Truchard E, Bizzozzero T, Tahar A, et al. Factors associated with antibiotics for respiratory infections in Swiss long-term care facilities. Journal of Hospital Infection. nov 2024;153:90‑8.
19. Ticinesi A, Lauretani F, Nouvenne A, Mori G, Chiussi G, Maggio M, et al. Lung ultrasound and chest x-ray for detecting pneumonia in an acute geriatric ward. Medicine. juill 2016;95(27):e4153.
20. Baribeau Y, Sharkey A, Chaudhary O, Krumm S, Fatima H, Mahmood F, et al. Handheld Point-of-Care Ultrasound Probes: The New Generation of POCUS. Journal of Cardiothoracic and Vascular Anesthesia. nov 2020;34(11):3139‑45.
21. Haji-Hassan M, Lenghel LM, Bolboaca SD. Hand-Held Ultrasound of the Lung: A Systematic Review. Diagnostics. 31 juill 2021;11(8):1381.
22. Chu D, Liteplo A, Duggan N, Hutchinson AB, Shokoohi H. Artificial Intelligence in Lung Ultrasound. Curr Pulmonol Rep. 6 mars 2024;13(2):127‑34.